1��ѡ���� �����ĸ��������ڲ�ͬ�����²���ĺϳɰ���Ӧ�����ʣ����������
A��v(H2)="=0.1" mol��(L��min)
B��v(N2)==0.1mol��(L��min)
C��v(NH3)==0.15mol��(L��min)
D��v(N2)==0.02mol��(L��s)
�ο��𰸣�D
���������ͬһ����ѧ��Ӧ���ò�ͬ�����ʱ�ʾ�䷴Ӧ����ʱ����ֵ���ܲ�ͬ������ʾ����������ͬ�ġ������ڱȽϷ�Ӧ���ʿ���ʱ��Ӧ�û������ͬһ�����ʱ�ʾ��Ȼ�����ֱ�ӱȽ�������ֵ��С����������֮������Ӧ��ѧ������֮�ȿ�֪���������������ʾ����ֱ���0.1mol��(L��min)��0.3mol��(L��min)��0.225mol��(L��min)��3.6mol��(L��min)�����Դ�ѡD��
�����Ѷȣ���
2��ѡ���� ������̶�Ϊ2 L���ܱ������У�A��B��C��D������������ʵ���n(mol)��ʱ��t(min)�ı仯�����ͼ��ʾ�������й�˵������ȷ���ǣ�?��
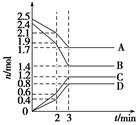
A���÷�Ӧ�Ļ�ѧ����ʽΪ4A��5B?6C��4D
B��ǰ2 min��B��ʾ�ķ�Ӧ����ԼΪ0.002 1 mol��L��1��s��1
C��2 minʱ����������ĸı�����������¶Ȼ�����˴���
D���÷�ӦΪ���ȷ�Ӧ
�ο��𰸣�D
����������������ʵ���֮�ȵ��ڻ�ѧ����ʽ��ϵ���ȣ�A��B���ʵ�������Ϊ��Ӧ�C��D���ʵ�������Ϊ������ʷ�Ӧ����ʽΪ(2.5��1.7)A��(2.4��1.4)B (0��1.2)C��(0��0.8)D������Ϊ4A��5B
(0��1.2)C��(0��0.8)D������Ϊ4A��5B 6C��4D����A��ȷ�����ݷ�Ӧ���ʹ�ʽ���㣺
6C��4D����A��ȷ�����ݷ�Ӧ���ʹ�ʽ���㣺 ��
��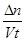 ��
��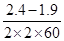 ��0.002 1 mol��L��1��s��1����B��ȷ�������¶Ȼ���������ʹ��Ӧ���ʼӿ죬��C��ȷ�����жϸ÷�Ӧ����ЧӦ����D����
��0.002 1 mol��L��1��s��1����B��ȷ�������¶Ȼ���������ʹ��Ӧ���ʼӿ죬��C��ȷ�����жϸ÷�Ӧ����ЧӦ����D����
�����Ѷȣ�һ��
3������� ��֪п��ϡ���ᷴӦΪ���ȷ�Ӧ,ijѧ��Ϊ��̽���䷴Ӧ�����е����ʱ仯,����ˮ�������ռ���Ӧ�ų�������,ʵ���¼����:
����ʱ��(min)
| 1
| 2
| 3
| 4
| 5
|
�������(mL)
| 30
| 120
| 280
| 350
| 370
|
�ٷ�Ӧ��������(��0~1 min��1~2 min��2~3 min��3~4 min��4~5 min)ʱ���Ϊ��������,ԭ��?����?
�ڷ�Ӧ������С��ʱ���Ϊ��������,ԭ����?��
�ο��𰸣���4�֣���2~3 min�����ڷ�Ӧ����,��Һ�¶�����,��Ӧ���ʼӿ졡
��4~5 min������Ũ�Ƚ���,���·�Ӧ���ʼ���
�����������0��1��l��2��2��3��3��4��4��5min��ʱ�����������������ֱ�Ϊ30��90��160��70��20�����Կ�����Ӧ����������2��3min��п��ϡ���ᷴӦΪ���ȷ�Ӧ���淴Ӧ�Ľ��У��¶�Խ��Խ�ߣ���Ӧ���ʼӿ죬�ʴ�Ϊ��2��3min����÷�Ӧ�Ƿ��ȷ�Ӧ����ʱ�¶ȸߣ�
�����ŷ�Ӧ�Ľ��У�����Ũ��Խ��ԽС����Ӧ����Խ��Խ�����ʴ�Ϊ��4��5min��
���������⿼��ѧ��Ӱ�컯ѧ��Ӧ���ʵ����أ��ѶȲ����ǵ÷ֲ����ס�
�����Ѷȣ�һ��
4��ѡ���� ��һ���¶�ʱ����1mol A��2mol B�����ݻ�Ϊ5 L��ij�ܱ������з������·�Ӧ��A��s����2B��g�� C��g����2D��g������5min���������B��Ũ�ȼ�����0.2mol��L��1����������������ȷ���ǣ�?��
C��g����2D��g������5min���������B��Ũ�ȼ�����0.2mol��L��1����������������ȷ���ǣ�?��
A����5min�ڸ÷�Ӧ��C��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ
0.02mol����L��min����1
B����5minʱ��������D��Ũ��Ϊ0.2mol��L��1
C���ÿ��淴Ӧ�淴Ӧ�Ľ��У�������ѹǿ������
D��5minʱ�����������ܵ����ʵ���Ϊ3mol
�ο��𰸣�D
����������������⣬���Լ���v��B����0.04mol����L��min����1����v��C����0.02mol����L��min����1��A��ȷ��5minʱ��c��C����0.1mol��L��1����c��D����0.2mol��L��1��B��ȷ���÷�ӦΪ�������ʵ������ӵķ�Ӧ���淴Ӧ�Ľ��У�������ѹǿ����C��ȷ��5minʱ����n��B����0.2mol��L��1��5 L��1mol����n��C����0.5mol����n��D����1mol�������������ʵ���Ϊ2mol��1mol��0.5mol��1mol��2.5mol��D˵������
�����Ѷȣ�һ��
5��ѡ���� ���ĸ���ͬ��������,�ڲ�ͬ�������½��кϳɰ���Ӧ��N2 + 3H2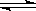 2NH3��������������ͬʱ���ڲ�õĽ���ж�,���ɰ��ķ�Ӧ�ٶ������ǣ�?
2NH3��������������ͬʱ���ڲ�õĽ���ж�,���ɰ��ķ�Ӧ�ٶ������ǣ�?
A��V(NH3) =" 0.1" mol/(L�qmin)
B��V(N2) =" 0.1" mol/(L�qmin)
C��V(N2) =" 0.2" mol/(L�qmin)
D��V(H2) =" 0.3" mol/(L�qmin)
�ο��𰸣�C
���������ͬһ����ѧ��Ӧ���ò�ͬ�����ʱ�ʾ�䷴Ӧ����ʱ��������ֵ���ܲ�ͬ������ʾ����������ͬ�ģ����ԱȽϷ�Ӧ���ʿ���ʱ��Ӧ�ø�������֮������Ӧ�Ļ�ѧ������֮���Ȼ������ͬһ�����ʱ�ʾ��Ȼ�����ֱ�ӱȽ�������ֵ�����Ը��ݷ�Ӧ�ķ���ʽ��֪�������Ҫ����������ʾ��Ӧ���ʣ���ֱ���0.15mol/(L��min)��0.3mol/(L��min)��0.6 mol/(L��min)��0.3mol/(L��min)�����Դ�ѡC��
�����������Ǹ߿��еij�����������ͣ������е��Ѷ�����Ŀ��飬���������ǿ����ע�ض�ѧ������֪ʶ���̺�ѵ����ͬʱ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ����ּ�ڿ���ѧ��������û���֪ʶ���ʵ������������������Ҫע������ڽ��з�Ӧ���� ��ת��ʱ����Ҫע�ⵥλ��ͳһ��
�����Ѷȣ�һ��