1��ѡ���� �����й�Ũ������Ũ����������У���ȷ���ǣ�?��
A�������¶���������������
B��¶���ڿ����У���������Һ������������
C�������¶�����ͭ�Ͽ췴Ӧ
D��¶���ڿ����У���������Һ������������
�ο��𰸣�
 A
A
��������������£�����Ũ�����Ũ�����лᷢ���ۻ������ѡ��A��ȷ��Ũ�����ӷ�������¶���ڿ�������Һ���������٣���Ũ���������ˮ�ԣ���Һ�����������ӵģ�ѡ��B��D����ȷ��ͭ��Ũ���ᷴӦ��Ҫ���ȣ�C����ȷ����ѡA��
�����Ѷȣ�һ��
2��ʵ���� ��16�֣����������(Na2S2O3)������Ҫ����������Σ��׳ơ������������������մ�������ˮ���������Ҵ�������֯��Ư�ס������������й㷺Ӧ�á�
ijУ��ѧ�о���ѧϰС���������ѧϰ��˼�룬ͨ��ʵ��̽��Na2S2O3�Ļ�ѧ���ʡ�
����Ʒ�Ʊ���ʵ�����г����������ƺ�����Ʊ�Na2S2O3��5H2O��д����Ӧ�Ļ�ѧ����ʽ????��
��ӦҺ����ɫ�����ˡ�Ũ���ᾧ�����ˡ�ϴ�ӡ����T�ò�Ʒ�����þ������Ҵ�ϴ�ӵ�Ŀ����???��
��������⡿Na2S2O3�Ƿ���Na2SO4�߱����Ƶ����������أ�
����٣�?��
����ڣ���Һ�����ԣ��Ҳ����ᷴӦ��
����ۣ���ԭ�ԣ����ܱ�������������
������̽����������������ڡ��ۣ����ʵ�鷽����
?
| ʵ�����
| ʵ�������
Ԥ��ʵ������
| ������ͣ���
���ӷ���ʽ��ʾ��
|
�����
| ???������ֽ�����ɫ������?
| ��ҺpH=8
| ?
|
��pH=2��������
�μ�Na2S2O3��Һ
| ?
| 2S2O32- +2H+�T�T S��+SO2��+H2O
|
�����
| ��������ˮ�еμ�����Na2S2O3��Һ
| ��ˮ��ɫ��dz
| ?
|
?
��ʵ����ۡ�
Na2S2O3�����ᷴӦ�����л�ԭ�ԣ���Na2SO4�Ļ�ѧ���ʲ����ơ�
���������ۡ�
��1����ͬѧ��̽��������ۡ���Ӧ�����Һ�еμ���������Һ���۲쵽�а�ɫ�������������ݴ���Ϊ��ˮ�ɽ�Na2S2O3����������Ϊ�÷����Ƿ���ȷ��˵�����ɣ�?��
��2�����������һ��ʵ�鷽����֤��Na2S2O3���л�ԭ�ԡ����ʵ�鷽���ǣ�?��
�ο��𰸣�
����Ʒ��ȡ��Na2SO3 + S + 5H2O �T�TNa2S2O3��5H2O?��ȥ���������ʣ����ٲ�Ʒ���ܽ����
��������⡿��BaCl2��Һ��Ӧ�г�������
������̽�����ò�����պȡNa2S2O3��Һ����ε�pH��ֽ�����룬�е���ɫ��������ɫ�̼�����ζ�������? S2O32-��4Cl2��5H2O=2SO42-��8Cl����10H��
���������ۡ�
��1������ȷ������ˮ�б����ͺ���Cl��
��2��������Na2S2O3��Һ�е�����ˮ��Ȼ������Ȼ�����Һ�����۲쵽��ɫ��������������������ܽ⣬��˵��Na2S2O3�ܱ���ˮ����
�������������Ʒ��ȡ������ȷ��Ӧ����Na2SO3��S ����������Na2S2O3��5H2O���ɿ�����д����ѧ��Ӧ����ʽ������֪����������ˮ���������Ҵ�����˵���Ҵ��������dz�ȥ���ʡ�������ġ�
��������⡿���������Ȼ�����Ӧ���ɰ�ɫ����������Na2S2O3��BaCl2��Һ��Ӧ�г������ɣ�
������̽������������ˮ��Ĺ��ɣ�������ˮ�⣬������ˮ�⣬Խ��Խˮ�⣬˭ǿ��˭�ԣ�Na2S2O3Ϊ
ǿ�������Σ�ˮ��ʼ��ԣ���PH��ֽ����Һ��PH��
��pH=2�������еμ�Na2S2O3��Һ����������ƺ����ᷴӦ���ɶ���������������ʣ�Na2S2O3+H2SO4=Na2SO4+S��+SO2��+H2O��
����������ԭ��Ӧ��ʵ�ʵ�ʧ�����غ㣬S2O32-��2SO42-��8e-��Cl2��2CI-��2e-������4molCl2����1molS2O32-���õ�8molCl-��2molSO42-�����ݵ���غ㣬��������Ӧ��10molH+������ԭ���غ㷴Ӧ����Ӧ��5molH2O�����ӷ���ʽΪS2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+��
���������ۡ���1����ˮ�ijɷ��к��������ӣ����Ժ�AgNO3��Һ��Ӧ������ɫ������
��2��Na2S2O3����ˮ����������������ӣ����������ʱҪ�ų�̼������Ӻ�����������ӵĸ��ţ����Լ����������ữ���Ȼ�����Һ������а�ɫ������������֤��������������ӣ���֮��û�С�
���������ʵļ��飬Ҫ���������и�����Ϣ�������⡢������⣬��Ŀ�Ѷ��еȣ�
�����Ѷȣ�һ��
3��ѡ���� ������ʵ��Ũ������ֳ�������(������)��Ӧ��ϵ��ȷ����(����)
A���ڿ����г��ھ��õ�Ũ���ᣬ��Һ��������(��ˮ��)
B���ڼ���������ͭ��Ũ���ᷴӦ(�����ԡ�����)
C��������Ũ���ᷴӦ���к���״��̿����(��ˮ��)
D��Ũ�������������ijЩ����(���ӷ���)
�ο��𰸣�B
���������Ũ���������ˮ�ԣ����Գ��ڷ��ã���Һ���������ӡ���Ũ�����ͭ�ķ�Ӧ�У�������ͭ��SO2��ˮ���ɣ������ڷ�Ӧ��Ũ������ֳ������Ժ����ԡ�C����Ũ�������ˮ�ԣ�D����Ũ�������ˮ�ԡ�������ȷ�Ĵ���B��
�����Ѷȣ���
4������� ������Һ�п��ܺ��� ��
��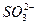 ��S2-��Cl-��Br-��I-��
��S2-��Cl-��Br-��I-��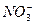 ��Na+��Mg2+�����ӡ�
��Na+��Mg2+�����ӡ�
��1����������ˮ����Һ����ɫ����ػ�ɫ�������ֻ��ǣ�����Һ��һ������__________��
��2�����������ᱵ��Һ���а�ɫ�������ɣ��ټ������ᣬ�����ٲ����ܽ⣬ԭ��Һ��һ������__________��
��3���������Ȼ�����Һ������Ļ����Һ�������ɡ����ȼ���ˮ��Ȼ���ټ����Ȼ�����Һ�����ᣬ�а�ɫ�������ɣ���ԭ��Һ��һ������__________��
��4�����������������������ɣ�������������ҺҲ�������ɣ���ԭ��Һ������������ֻ������__________��
�ο��𰸣���1��Br-��S2-��Na+?(2) ��
��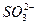 ��Na+
��Na+
(3)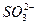 ��Na+?(4)Na+��
��Na+?(4)Na+��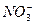
������������Ӵ��ڵ���������������Լ�������������
��1��������ˮ����Һ����ɫ��Ϊ�ػ�ɫ�����ֻ��ǣ���Һ��һ������I-��I-��Br2����Ϊ���ʣ�2I-+Br2====I2+2Br-,����Һ��Ϊ�ػ�ɫ��
���ֻ���������S2-������Ϊ����S���ֳ�����S2-+Br2====2Br-+S��������Ҳһ������S2-��
��Ϊ�������Ӿͱ�������֮��Ӧ�������ӣ��ʱ���Na+��
��2���������ᱵ�а�ɫ�������ɣ��ּ������ᣬ�����ٲ����ܽ⣬����Һ�бغ��� �����ɵ�BaSO4������ˮ���������Ҳһ������
�����ɵ�BaSO4������ˮ���������Ҳһ������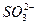 ������BaSO3������������ˮ���������ᡣ
������BaSO3������������ˮ���������ᡣ
ͬ������Һ�бغ������ӡ�����Na2SO4��Na2SO3��MgSO4������ˮ����MgSO3����ˮ�������γɳ�����Mg2+��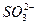 ���ܴ������棬�ʴ���Һ�бغ�Na+��
���ܴ������棬�ʴ���Һ�бغ�Na+��
��3��������Һ�м����Ȼ���������Ļ����Һ���������ɡ��ȼ�����ˮ��Ȼ���ټ����Ȼ�����Һ�����ᣬ�а�ɫ��������������Һ�бغ�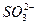
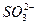
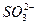 ����Ϊ�����������²���������BaSO3�ij�������������ˮ��
����Ϊ�����������²���������BaSO3�ij�������������ˮ��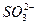 ������Ϊ
������Ϊ ��
��
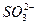 +Cl2+H2O====
+Cl2+H2O==== +2H++2Cl-
+2H++2Cl-
���ټ����Ȼ�����Һ�����Ὣ������������İ�ɫ����BaSO4������Һ�е�������ӦΪNa+,��ΪMg2+��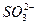
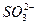 ���ܴ������档
���ܴ������档
��4��������Ba(OH)2��Һ����������Һ���� ��
��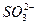 ��Mg2+��������AgNO3����������Һ����Cl-��Br-��I-��
��Mg2+��������AgNO3����������Һ����Cl-��Br-��I-��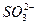 ��
�� �����ӣ�������Һֻ���ܴ���Na+��
�����ӣ�������Һֻ���ܴ���Na+��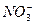 ��
��
�����Ѷȣ���
5��ѡ���� �������ӷ���ʽ�У���ȷ���ǣ�?��
A������������ˮ��Ӧ��Na+2H2O====Na++2OH-+H2��
B��̼���Ͷ�������Һ��CaCO3+2CH3COOH====Ca2++2CH3COO-+H2O+CO2��
C����Ca(ClO)2��Һ��ͨ����CO2���壺Ca2++2ClO-+CO2+H2O====CaCO3��+2HClO
D��������ͭ��Һ�е���Ba(OH)2��Һ��Ba2++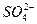 ====BaSO4��
====BaSO4��
�ο��𰸣�B
���������A�������ӷ���ʽû����ƽ��C����Ӧ������Ca(HCO3)2,������CaCO3;D�������ӷ���ʽӦ���ǣ�Cu2++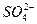 +Ba2++2OH-====Cu(OH)2��+BaSO4��������B��ȷ��
+Ba2++2OH-====Cu(OH)2��+BaSO4��������B��ȷ��
�����Ѷȣ���