| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ����ɡ�ԭ���ԭ��������Ԥ�⣨2017�����°棩(��)
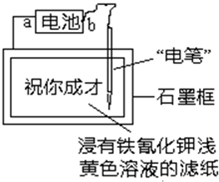 �ο��𰸣�A��aΪ��صĸ�����bΪ��ص���������A���� ��������� �����Ѷȣ��� 4��ѡ���� ��ͼ��ʾ������Ȧ����Ȧ�ĺ��Ӵ�����һ�����߽�������ʢˮ���ձ��У�ʹ֮ƽ�⣻С�ĵ����ձ����� ����CuSO4��Һ��Ƭ�̺�ɹ۲쵽�������� �ο��𰸣�D ��������� �����Ѷȣ�һ�� 5��ѡ���� �ռ�ʵ���ҡ��칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ�أ�RFC����RFC��һ�ֽ�ˮ��⼼��������ȼ�ϵ�ؼ������ϵĿɳ�ŵ�ء���ͼΪRFC����ԭ��ʾ��ͼ���й�˵����ȷ���ǣ�?�� �ο��𰸣�D ��������������װ��ͼ��֪�����װ������ӵ�Դ��Ϊ���أ��ұ�װ����ԭ��ء������У�b�缫����ӵ�Դ��������������bΪ������ʧ���ӷ���������Ӧ��4OH--4e-�T2H2O+O2����a�缫����ӵ�Դ�ĸ�����������aΪ�������õ����ӷ�����ԭ��Ӧ��2H++2e-�TH2����ȼ�ϵ������������Һ�����װ��ͼ֪��dΪ����ʧ���ӷ���������Ӧ��H2-2e-�T2H+��c�缫Ϊ�����õ����ӷ�����ԭ��Ӧ��O2+4H++4e-�T2H2O��A��������������֪������0��1mol����ת��ʱ��a������1��12L H2����״���£�������B�� b���Ϸ����ĵ缫��Ӧ�ǣ�4OH--4e-�T2H2O+O2��������C�� d���Ϸ����ĵ缫��Ӧ�ǣ�H2-2e-�T2H+������D��cΪԭ��ص����������������������� c���Ͻ��л�ԭ��Ӧ��B�е�H+����ͨ����Ĥ����A����ȷ�� �����Ѷȣ�һ�� |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ���ܽᡶ�����ĸ�ʴ.. | |
| �����Ŀ |