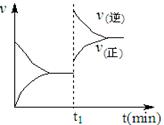
1、选择题 下图为某化学反应速率―时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是(?)
A.2SO2 (g)+O2 (g)  2SO3 (g) ;△H<0
2SO3 (g) ;△H<0
B.H2 (g)+I2 (g)  2HI (g) ;△H>0
2HI (g) ;△H>0
C.4NH3 (g)+5O2 (g)  4NO(g)+6H2O (g) ;△H<0
4NO(g)+6H2O (g) ;△H<0
D.C (s)+H2O (g)  CO (g)+H2 (g) ;△H>0
CO (g)+H2 (g) ;△H>0
2、填空题 某条件下,在2 L密闭容器中发生如下反应2NO2(g) 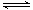 2NO(g)+O2(g)
2NO(g)+O2(g)
在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol・L-1)随时间(min)的变化如图所示。请回答下列问题:
在2L密闭容器内,800℃时反应:2NO2(g) 2NO(g)+O2(g)体系中,n (NO2)随时间的变化如表:
2NO(g)+O2(g)体系中,n (NO2)随时间的变化如表:
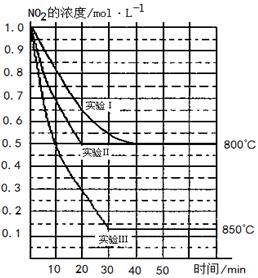
⑴实验Ⅱ隐含的反应条件是
⑵写出该反应的平衡常数表达式: K= 。
该反应是________(填“吸” 或“ 放”)热反应。
⑶若实验Ⅰ中达平衡后,再向密闭容器中通入2 mol由物质的量之比为1:1组成的NO2与O2混合气体(保持温度不变),则平衡将 移动。
⑷若将上述第⑶题所得的平衡混和气体通入足量的NaOH溶液中,使气体被完全吸收。
生成的产物及其物质的量为 。
⑸NO2、NO是重要的大气污染物,近年来人们利用NH3在一定条件下与之反应而将其转
化为无害的参与大气循环的物质,该反应的化学方程式为 。
(任写一个)
3、选择题 在密闭容器中,反应N2(g)+3H2(g)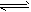 2NH3(g);ΔH<0, 达到甲平衡。在仅改变某一条件后,达到乙平衡,改变的这一条件是
2NH3(g);ΔH<0, 达到甲平衡。在仅改变某一条件后,达到乙平衡,改变的这一条件是
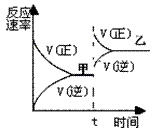
[? ]
A.增大压强
B.升高温度
C.增大N2的浓度
D.加入适当催化剂
4、填空题 反应mA+nB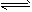 pC在某温度下达到平衡。 pC在某温度下达到平衡。
(1)若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是___________。
(2)若C为气体,且m + n = p,在加压时化学平衡发生移动,则平衡必定向______方向移动。
(3)如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为_____态。
5、填空题 (14分)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)  CH3OH(g)下表为不同温度下的平衡常数(K) CH3OH(g)下表为不同温度下的平衡常数(K)
温度
| 250℃
| 300℃
| 350℃
| K
| 2.041
| 0.270
| 0.012
|
(1)该反应的平衡常数表达式K= ,ΔH 0(填“>”、“<”或“=”)。
(2)将1 mol的H2和 1 mol 的 CO充入 1 L 恒容密闭反应器中,达到平衡后,容器内的压强为开始时的60%,求CO的平衡转化率(写出计算过程)。
(3)300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是
(填字母)。
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡时c(H2)/ c(CH3OH)减小
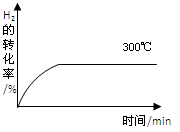
(4)其他条件相同时,在上述三个温度下分别发生该反应。300℃时,H2的转化率随时间的变化如图所示,请补充完成350℃时H2的转化率随时间的变化示意图。
|