1������� ��֪��������Խ���γ�ԭ���ʱԽ���ŵ硣�������ͼװ�ã��ش��������⣺?
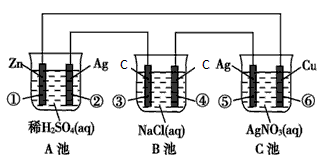
��1����װ�������ǣ�A��________��B��______��
��2��д���缫�Ϸ����ķ�Ӧ����_____________����___________����_____________��
��3������·����2 mol��������ʱ���ټ��������仯______g�����������仯______g��
��4����Ӧ����һ��ʱ���A��B��C�����е������ҺŨ�Ȳ������________��
�ο��𰸣���1��ԭ��ء������ء���
��2��Zn-2e-===Zn2+����2Cl--2e-===Cl2������2Ag-2e-===2Ag+������Ag-e-===Ag+��
��3��65����216��
��4��C��
���������
�����Ѷȣ�һ��
2������� ��ˮ��������Դ�ı��⣬����ˮɹ�Ρ��ǻ�ȡʳ�ε���Ҫ��Դ��ʳ�μ���һ���������Ʒ��Ҳ��һ����Ҫ�Ĺ�ҵԭ�ϡ���ʳ��Ϊԭ�Ͽ��Եõ����ֲ�Ʒ����ҵ����Ҫͨ����ⱥ���Ȼ�����Һ�ķ�������������ơ�
��1��������ӦʽΪ?������õ缫��Ӧ����ķ����ǣ�?��
��2���������������Ϲ��ռ�������22��4 Lʱ����״���£����������������ȫ���ռ��������·��ͨ�����ӵĸ���Ϊ?��
��3������Ȼ���ϡ��Һ�����Ʊ���84������Һ����ͨ��ʱ��������������Һ��ȫ���գ���������������Һ����һ�����ʣ���д����Ӧ�Ļ�ѧ����ʽ��?����һ������ʽ��ʾ����
�ο��𰸣���1��2Cl--2e-==Cl2��? ,��ʪ��ĵ���KI��ֽ����������������ֽ����ɫ��֤��������Cl2��
��2��NA ,��3��NaCl+H2O  ?NaClO+H2�� ��
?NaClO+H2�� ��
�����������1����ⱥ���Ȼ�����Һ��������ӦΪ��2Cl--2e-==Cl2�������������ķ����ǽ�ʪ��ĵ���KI��ֽ����������������ֽ����ɫ��֤��������Cl2����2����ⱥ���Ȼ�����Һ��������ӦΪ��2Cl--2e-==Cl2����������ӦΪ��2H��+2e�� H2�����������������Ϲ��ռ�������22��4 Lʱ�����·��ͨ�����ӵĸ���ΪNA����3����������֪������Ȼ���ϡ��Һ�����Ʊ���84������Һ������Ϊ�������ƺ���������ѧ����ʽΪNaCl+H2O
H2�����������������Ϲ��ռ�������22��4 Lʱ�����·��ͨ�����ӵĸ���ΪNA����3����������֪������Ȼ���ϡ��Һ�����Ʊ���84������Һ������Ϊ�������ƺ���������ѧ����ʽΪNaCl+H2O  ?NaClO+H2�� ��
?NaClO+H2�� ��
�����Ѷȣ�һ��
3��ѡ���� �ö��Ե缫���CuSO4��NaCl�Ļ����Һ����ʼʱ���������������������ʷֱ��ǣ�������
A��H2��Cl2
B��Cu��Cl2
C��H2��O2
D��Cu��O2
�ο��𰸣��ö��Ե缫���NaCl��CuSO4�Ļ����Һ��
��Һ��Cl-��OH-��SO42-�������ƶ���Cl-�ŵ�������ǿ����2Cl--2e-�TCl2����
��Һ��Cu2+��H+��Na+�������ƶ���Cu2+�ŵ�������ǿ����Cu2++2e-�TCu��
���������������Ϸֱ�����������ΪCu��Cl2��
��ѡB��
���������
�����Ѷȣ�һ��
4��ѡ���� ��ͼ�ǵ�ⱥ��ʳ��ˮ��װ�ã������й��ж���ȷ����

A�����ʱ������ �������������õ�������
�������������õ�������
B������������������Һ�У�����KI��Һ����Һ���ػ�ɫ
C������������������Һ�е����̪��Һ����Һ����ɫ
D�����һ��ʱ���ȫ�����Һת�Ƶ��ձ��У���ֽ������Һ������
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
5��ѡ���� ��ʯī�缫���100mL 0.100mol/L CuSO4��0.200mol/L NaCl�Ļ����Һ������ʱ����������ȫ���ݳ������һ��ʱ��������ռ���224mL����ʱ������һ���ռ������������ǣ���������������Ϊ��״���²ⶨ��
A��112mL
B��224mL
C��336mL
D��448mL
�ο��𰸣�C
��������������Ϸ����ķ�ӦΪ��Cu2++2e-=Cu��2H++2e-=H2��������������ӦΪ2Cl--2e-=Cl2����4OH--4e-=2H2O+O2���������ռ�224ml���壬��ת�Ƶ���Ϊ��0.01��2+0.01��2=0.04mol������������0.01mol������0.005mol��������336ml��
�����Ѷȣ�һ��