| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ���ȫ��ԭ���ԭ�������߲��ԣ�2017�����°棩(��)
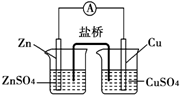 �ο��𰸣�A��ԭ��ع���ʱ��пΪ������ͭΪ���������Ӵ�п�缫ͨ������������ͭ�缫����A���� ��������� �����Ѷȣ�һ�� 2���ж��� ��10�֣��������վñ������ɫ�����������������������������ԭ���ԭ�����С���?�⡱ ��?�䴦������Ϊ����һ��Ũ�ȵ�ʳ����Һ����һ���������У��ٽ���ڵ�����������Һ�У�����һ��ʱ���ɫ����ȥ�����ָ������Ҳ�����ʧ���Իش� �ο��𰸣���1��������������� �����������1���γ�ԭ�����Ҫ����ʵ��磬���NaCl��������������á� �����Ѷȣ��� 3��ѡ���� ��һ�������һ��Ũ�ȵ�ϡ���������п��Ӧ����ȡһ�������������Ҫ��߷�Ӧ���ʶ��ֲ��ı������������������ �ο��𰸣�D ����������� �����Ѷȣ�һ�� 4��ѡ���� ���з�Ӧ������������Ƴ�ԭ��ص��� �ο��𰸣�A ��������� �����Ѷȣ��� 5��ѡ���� ��ͼ����ʢ��ϡ?H2SO4?���ձ��з����õ������ӵĵ缫X��Y�����·�е���������ͼ��ʾ�����ڸ�װ�õ�����˵����ȷ���ǣ������� |

�ο��𰸣�A������ͼƬ֪��װ����ԭ��أ����·�е��Ӵ�X�缫����Y�缫����������������෴����Y�����·��X����A����
B��ԭ����нϻ��õĽ������������ϲ����õĽ�����ķǽ����������������缫�ֱ�ΪFe��̼������YΪ̼����XΪFe����B����
C��X�Ǹ����������Ϸ���������Ӧ��Y�������������Ϸ�����ԭ��Ӧ����C����
D��ԭ����нϻ��õĽ������������ϲ����õĽ�����ķǽ�������������ԭ�����X�Ǹ�����Y�����������������缫���ǽ����������ǵĻ��˳��ΪX��Y����D��ȷ��
��ѡD��
���������
�����Ѷȣ���
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ����ɡ����ʵļ���.. | |
| �����Ŀ |