1、填空题 已知A、B、C、D、E、F均为短周期主族元素,原子序数依次增大,它们的原子半径和最高正化合价或最低负化合价如下表所示
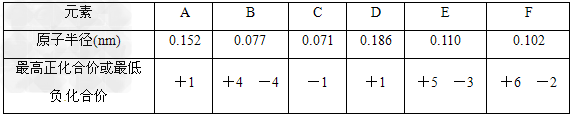
(1)写元素符号:A________,D________,F________.
(2)A的单质可以在常温下与氮气反应,写出反应的化学方程式:___________________,产物的化学键类型为___________________.
(3)写出D与F形成的化合物水解的离子方程式:_________________________________.
参考答案:(1)Li;Na;S
(2)6Li+N2===2Li3N;离子键
(3)S2-+H2O HS-+OH-
HS-+OH-
本题解析:
本题难度:一般
2、推断题 D、E、X、Y、Z是周期表中的前20号元素,且原子序数逐渐增大.它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形?(V形)、直线形.
回答下列问题:
(1)Y的最高价氧化物的化学式为_________________________;
(2)上述5种元素中,能形成酸性最强的含氧酸的元素是________________;
(3)D和Y形成的化合物,其分子的空间构型为____________;
(4)D和X形成的化合物,其化学键类型属________,其晶体类型属________;
(5)金属镁和E的单质在高温下反应得到的产物是__________,此产物与水反应生成两种碱,该反应的化学方程式是___________________________________________________;
(6)试比较D和X的最高价氧化物熔点的高低____________________________________.
参考答案:(1)SO3
(2)Cl
(3)直线形
(4)共价键;原子晶体
(5)Mg3N2;Mg3N2+6H2O==3Mg(OH)2↓+2NH3↑
(6)SiO2的熔点高于CO2
本题解析:
本题难度:一般
3、选择题 下列各组微粒中,属于同位素的是( ? )
①H2O和D2O②O2和O3③CO和CO2④CO和C2H4⑤ 和
和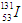 ⑥16O2和18O2⑦12C和13C.
⑥16O2和18O2⑦12C和13C.
A.①⑥
B.②③④
C.⑤⑦
D.②⑥
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列递变规律正确的是( )
A.酸性:HClO4>H3PO4>H2SO4
B.原子半径由大到小顺序:K>Ca>Mg>Na>Al
C.碱性:NaOH>Mg(OH)2>Ca(OH)2
D.氧化性:F2>Cl2>Br2>I2
参考答案:A.非金属性Cl>S>P,则最高价氧化物的水化物的酸性为HClO4>H2SO4>H3PO4,故A错误;
B.电子层越多,原子半径越大,同周期从左向右原子半径在减小,原子半径由大到小顺序为K>Ca>Na>Mg>Al,故B错误;
C.金属性Ca>Na>Mg,最高价氧化物的水化物的碱性为Ca(OH)2>NaOH>Mg(OH)2,故C错误;
D.非金属性F>Cl>Br>I,则氧化性为F2>Cl2>Br2>I2,故D正确;
故选D.
本题解析:
本题难度:一般
5、选择题 下列各组元素属于p区的是
A.Na、N、P
B.O、S、Ar
C.Fe、Ar、Cl
D.H、Mg、Al
参考答案:B
本题解析:
本题难度:一般