1、填空题 (11分)已知2NO2(g) N2O4(g) ΔH(298K)=-52.7kJ・mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
N2O4(g) ΔH(298K)=-52.7kJ・mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
Ⅰ.该小组的同学取了两个烧瓶A和B,分别加入相同浓度的NO2与N2O4的混合气体,中间用夹子夹紧,并将A和B浸入到已盛有水的两个烧杯中(如图所示),然后分别向两个烧杯中加入浓硫酸和NH4NO3固体。

请回答:
(1)A中的现象 ,B中的现象 ;
(2)由此可知,降低温度,该化学平衡向 (填“正”或“逆”)反应方向移动;
(3)该化学反应的浓度平衡常数表达式为 ,升高温度,该反应中NO2的转化率将 (填“增大”、“减小”或“不变”)。
Ⅱ.在三支容积均为30cm3针筒中分别抽入10cm3NO2气体,将针筒前端封闭。
(1)将第二支针筒活塞迅速推至5cm3处,此时气体的颜色变深,一段时间后气体颜色又变浅了,但仍比第一支针筒气体的颜色深。
①推进针筒后颜色变深的原因是 ;
②一段时间后气体颜色又变浅的原因是 ;
③由此实验得出的结论是 。
(2)将第三支针筒活塞快速拉至20cm3处,该同学观察到的现象是 ;
在此过程中,该反应的化学平衡常数将 (填“增大”、“减小”或“不变”,下同),NO2的转化率将 。
参考答案: (1)气体颜色加深 气体颜色变浅
(2)正(1分)
(3) 减小
减小
Ⅱ.(1)①气体的体积减小,NO2浓度增大,气体的颜色加深
②增大压强,减小气体的体积,平衡向正反应方向移动
③增大压强,化学平衡向气态物质系数减小的方向移动
(2)气体的颜色先变浅,一段时间后又变深,但仍比第一支针筒气体的颜色浅
不变 减小
本题解析:(1)A中温度升高,平衡逆移,生成更多的二氧化氮气体,因此A中的颜色加深。而B中则刚好相反。
(2)降低温度,平衡向放热反应的方向移动。
(3)平衡常数表达式 。升高温度,平衡逆移,故NO2的转化率变小。
。升高温度,平衡逆移,故NO2的转化率变小。
Ⅱ.(1)①推进针筒,使得气体体积减少,浓度增大,因此颜色加深。
②一段时间后,由于压强增大,平衡正移,因此颜色会变浅。
③此实验中主要是对压强的改变,因此可以得出的结论即为压强对平衡移动的影响。
(2)第三支针筒活塞快速拉至20cm3处,则此时体积增大,浓度减小,颜色变浅;而体积增大,压强减小,平衡逆移,故一段时间后,气体的颜色加深,且NO2的转化率变小。而对于平衡常数则不变。
考点:化学平衡
点评:本题以NO2与N2O4的相互转换为载体,考查了压强对化学平衡移动的影响。
①增大压强,平衡向气体体积减小的方向移动。
②对于由气体参与的反应,增大压强,反应速率增大,但平衡不一定发生移动。
③化学平衡常数只与温度和化学方程式有关,与平衡移动无关。
本题难度:一般
2、选择题 对于可逆反应N2(g)+3H2(g) 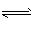 2NH3(g);△H<0,下列研究目的和示意图相符的是
2NH3(g);△H<0,下列研究目的和示意图相符的是
[?]
A.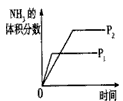 压强对反应的影响(P2>P1)?
压强对反应的影响(P2>P1)?
B.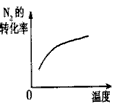 温度对反应的影响
温度对反应的影响
C.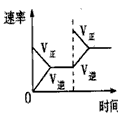 平衡体系增加N2 对反应的影响
平衡体系增加N2 对反应的影响
D.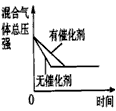 催化剂对反应的影响
催化剂对反应的影响
参考答案:C
本题解析:
本题难度:一般
3、选择题 在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g) zC(g)平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断不正确的是 ( )
zC(g)平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断不正确的是 ( )
A.x+y