1ЎўСЎФсМв ¶аБт»ҜДЖNa2Sx(xЎЭ2)ФЪҪб№№ЙПУлNa2O2ЎўFeS2ЎўCaC2өИУРПаЛЖЦ®ҙҰЎЈNa2SxФЪјоРФИЬТәЦРҝЙұ»NaClOСх»ҜОӘNa2SO4Ј¬¶шNaClOұ»»№ФӯОӘNaClЈ¬·ҙУҰЦРNa2SxУлNaClOөДОпЦКөДБҝЦ®ұИОӘ1©U16Ј¬ФтxөДЦөКЗ
AЈ®5
BЈ®4
CЈ®3
DЈ®2
ІОҝјҙр°ёЈәA
ұҫМвҪвОцЈәёГМвІЙУГөзЧУКШәгҪвМвЎЈNa2SxөДS»ҜәПјЫОӘ-2/xЈ¬УРЈәЈЁ6+2/xЈ©x=2ЎБ16Ј¬x=5
ұҫМвДС¶ИЈәјтөҘ
2ЎўјтҙрМв ДіН¬С§ОӘБЛСйЦӨFe3+КЗ·сДЬСх»ҜH2SO3ЙъіЙБЛSO42-Ј¬ЛыУГ50mL0.1mol/LFeCl3ИЬТәОьКХЦЖИЎSO2ЖшМеөДОІЖшәуЈ¬ҪшРРТФПВКөСйЈә
ЈЁ1Ј©јмСйОьКХТәЦРөДSO42-Јә?Ј¬ЦӨГчFe3+ДЬ№»°СH2SO3Сх»ҜіЙSO42-Ј®
ЈЁ2Ј©ЗлЕдЖҪІўНкіЙЙПКц·ҙУҰЦРөД»ҜС§·ҪіМКҪЈә
2FeCl3+SO2+?ЁT?+H2SO4+?Ј¬·ҙУҰЦРөДСх»ҜІъОпКЗ?ЈЁРҙ»ҜС§КҪЈ©Ј®
ЈЁ3Ј©ОьКХТәЦРіэБЛә¬УРH+ЎўCl-ЎўSO42-ТФНвЈ¬¶ФЖдЛьіЙ·ЭЈЁFe3+ЎўFe2+ЎўH2SO3Ј©өДҝЙДЬЧйәПҪшРРМҪҫҝЈә
ўЩМбіцјЩЙиЈ®?јЩЙи1ЈәИЬТәЦРҙжФЪFe3+ЎўFe2+Ј»?јЩЙи2ЈәИЬТәЦРҙжФЪ?
ўЪЙијЖ·Ҫ°ёЎўҪшРРКөСйЈ¬СйЦӨјЩЙиЈ®ЗлРҙіцКөСйІҪЦиТФј°ФӨЖЪПЦПуәНҪбВЫЈЁҝЙІ»МоВъЈ©Ј®ПЮСЎКөСйКФјБәНТЗЖчЈәКФ№ЬЎўөО№ЬЎў0.1moL?L-1KMnO4Ўў0.1moL?L-1KSCNИЬТәЎўЖ·әмПЎИЬТәЈ®
| КөСйІҪЦи | ФӨЖЪПЦПуәНҪбВЫ
ІҪЦи1ЈәУГКФ№ЬИЎСщЖ·ИЬТә2Ў«3mLЈ¬ФЩУГөО№ЬИЎ?
ИфіцПЦСӘәмЙ«Ј¬ФтјЩЙи1іЙБўЈ»ИфОҙіцПЦСӘәмЙ«Ј¬ФтјЩЙи1І»іЙБўЈЁ»тјЩЙи2іЙБўЈ©
ІҪЦи2Јә?
?
?
?
ІҪЦи3Јә
ІОҝјҙр°ёЈә
ұҫМвҪвОцЈә
ұҫМвДС¶ИЈәТ»°г
3ЎўМоҝХМв ФЪВИСх»Ҝ·ЁҙҰАнә¬CNЈӯөД·ПЛ®№эіМЦРЈ¬ТәВИФЪјоРФМхјюПВҝЙТФҪ«Зи»ҜОпСх»ҜіЙЗиЛбСО(Жд¶ҫРФҪцОӘЗи»ҜОпөДЗ§·ЦЦ®Т»)Ј¬ЗиЛбСОҪшТ»ІҪұ»Сх»ҜОӘОЮ¶ҫОпЦКЎЈ
(1)Діі§·ПЛ®ЦРә¬KCNЈ¬ЖдЕЁ¶ИОӘ650 mg/LЎЈПЦУГВИСх»Ҝ·ЁҙҰАнЈ¬·ўЙъИзПВ·ҙУҰ(ЖдЦРNҫщОӘЈӯ3јЫ)ЈәKCNЈ«2KOHЈ«Cl2 KOCNЈ«2KClЈ«H2OЎЈұ»Сх»ҜөДФӘЛШКЗ___________ЎЈ KOCNЈ«2KClЈ«H2OЎЈұ»Сх»ҜөДФӘЛШКЗ___________ЎЈ
(2)Н¶Ил№эБҝТәВИЈ¬ҝЙҪ«ЗиЛбСОҪшТ»ІҪСх»ҜОӘөӘЖшЎЈЗлЕдЖҪПВБР»ҜС§·ҪіМКҪЈ¬ІўұкіцөзЧУЧӘТЖ·ҪПтәНКэДҝЈәKOCNЈ«KOHЈ«Cl2 CO2Ј«N2Ј«KClЈ«H2O CO2Ј«N2Ј«KClЈ«H2O
(3)ИфҙҰАнЙПКц·ПЛ®20 LЈ¬К№KCNНкИ«ЧӘ»ҜОӘОЮ¶ҫОпЦКЎЈЦБЙЩРиТәВИ?gЎЈ
ІОҝјҙр°ёЈә(1)Мј(»тC)
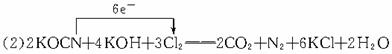
(3)35.5
ұҫМвҪвОцЈәұҫМвҪбәПә¬CNЈӯөД·ПЛ®ҙҰАнЈ¬ҝјІйСх»Ҝ»№Фӯ·ҙУҰөД»щұҫёЕДоЎўЕдЖҪЎўұкіцөзЧУЧӘТЖөД·ҪПтәНКэДҝЈ¬ёщҫЭ·ҪіМКҪҪшРР¶ЁБҝјЖЛгЈ¬КфЦРөИМвЎЈәОЦЦФӘЛШјЫМ¬ЙэёЯЛӯјҙұ»Сх»ҜЈ¬І»ДС·ЦОцЎЈТӘЕдЖҪ·ҪіМКҪЈ¬Н¬СщҙУФӘЛШјЫМ¬өДЙэҪөЎўөзЧУөГК§КШәгҝјВЗЎЈұкөзЧУЧӘТЖ·ҪПтәНКэДҝҝЙУГөҘПЯЗЕ»тЛ«ПЯЗЕұнКҫЈ¬ө«ұШРлЗш·ЦБҪХЯЈ¬өЪ(3)МвҝЙёщҫЭБҪёц·ҪіМКҪХТіцKCNУлCl2өДЧЬБҝ№ШПөЗуіцЎЈ
(1)ФЪKCNЈ«2KOHЈ«Cl2 KOCNЈ«2KClЈ«H2O·ҙУҰЦРЈ¬ВИФӘЛШјЫМ¬ҪөөНЈ¬HЎўNЎўOЎўKЛДЦЦФӘЛШөДјЫМ¬Г»ұдЈ¬Ц»УРМјФӘЛШөДјЫМ¬ЙэёЯЈ¬№Кұ»Сх»ҜөДОӘМјФӘЛШЎЈ KOCNЈ«2KClЈ«H2O·ҙУҰЦРЈ¬ВИФӘЛШјЫМ¬ҪөөНЈ¬HЎўNЎўOЎўKЛДЦЦФӘЛШөДјЫМ¬Г»ұдЈ¬Ц»УРМјФӘЛШөДјЫМ¬ЙэёЯЈ¬№Кұ»Сх»ҜөДОӘМјФӘЛШЎЈ
(2)Сх»Ҝ»№Фӯ·ҪіМКҪөДЕдЖҪЈ¬КЧПИТӘХТЧјұдјЫФӘЛШЈ¬ФЩАыУГ»ҜәПјЫЙэҪө·ЁЕдЖҪЈ¬·ҙУҰОпKOCNЦРNөДјЫМ¬ЙэёЯЈ¬KOCNОӘ»№ФӯјБЈ¬ВИЖшОӘСх»ҜјБЎЈ
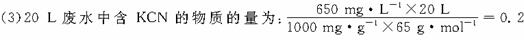
molЈ¬УЙБҪІҪ·ҙУҰөД»ҜС§·ҪіМКҪөГіц№ШПөКҪЈә2KCN~5Cl2Ј¬ЛщТФРиВИЖшЈә0.2 molЎБ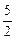 ="0.5" molЈ¬јҙ35.5 gЎЈ ="0.5" molЈ¬јҙ35.5 gЎЈ
ұҫМвДС¶ИЈәјтөҘ
4ЎўСЎФсМв ФЪИЫИЪKOHЦРҙуЖшЦРөДСхҝЙҪ«ёхМъҝуFeCr2O4ЦРFeәНCrөД»ҜәПјЫ¶јЧӘ»ҜОӘ+6јЫЈ¬Сх»Ҝ 1 mol FeCr2O4ФЪАнВЫЙПРиТӘ¶аЙЩДҰ¶ыСхЖш
AЈ®2mol
BЈ®2.5mol
CЈ®3mol
DЈ®4mol
ІОҝјҙр°ёЈәB
ұҫМвҪвОцЈә 1 mol FeCr2O4 ЦРFe+2ЎъFe +6,? Ўь4? 2Cr+3 Ўъ2 Cr+6?Ўь6?ЙэёЯЧЬКэОӘ10
2O0Ўъ2 O-2? Ўэ 4?ИфЙэҪөКэөИ?Фт O2Ри2.5mol
ұҫМвДС¶ИЈәТ»°г
5ЎўСЎФсМв ФЪ2KMnO4 +16HCl ="==" 2KCl +2MnCl2 + 5Cl2Ўь+8?·ҙУҰЦР
AЈ®Cl2КЗ»№ФӯІъОп
BЈ®ҙҰ¶ФУҰөДОпЦКОӘH2O
CЈ®Сх»ҜјБУл»№ФӯјБОпЦКөДБҝЦ®ұИОӘ1ЎГ8
DЈ®Иф1mol KMnO4ІОјУ·ҙУҰЈ¬ЧӘТЖөДөзЧУөДОпЦКөДБҝКЗ5mol
ІОҝјҙр°ёЈәBD
ұҫМвҪвОцЈәҝјІйСх»Ҝ»№Фӯ·ҙУҰөД»щұҫЦӘК¶ј°ЕдЖҪЈ»
УЙФӯЧУКШәгҝЙЦӘЈ¬?ҙҰ¶ФУҰөДОпЦКОӘH2OЈ»
·ҙУҰЦРГМФӘЛШИ«ІҝУЙ+7јЫҪөЦБ+2јЫЈ¬Иф1mol KMnO4ІОјУ·ҙУҰЈ¬өГөҪөДөзЧУөДОпЦКөДБҝКЗ5molЈ¬KMnO4ОӘСх»ҜјБЈ¬MnCl2 ОӘ»№ФӯІъОпЈ»¶шHCl ЦРөДІҝ·ЦВИФӘЛШУЙЎӘ1јЫЙэЦБ0јЫЈ¬К§өзЧУЈ¬ұ»Сх»ҜЈ¬HClЧц»№ФӯјБЈ¬Сх»ҜІъОпОӘCl2Ј»ҝЙјыЈ¬Сх»ҜјБУл»№ФӯјБОпЦКөДБҝЦ®ұИОӘ2ЎГ10Ј¬јҙ1ЎГ5Ј»
№Кҙр°ёОӘBD
ұҫМвДС¶ИЈәјтөҘ
|