1��ѡ���� ���и������ӣ���ָ��������һ���ܴ����������
A���������þ�ܲ���H2����Һ�У�Na+��Fe3+��SO42-��NO3-
B����ˮ�������C(OH-)=1��10-13mol/L����Һ�У�Fe2+��NH4+��ClO-��Cl-
C��C(OH-)=1��10-3mol/L����Һ�У�K+��SO42-��Cl-��CO32-
D����ʹpH��ֽ�����ɫ����Һ�У�S2-��SO32-��Na+��SO42-
�ο��𰸣�C
������������Ӽ����������ѧ��Ӧ�����ܴ������棬��֮���ԡ��������þ�ܲ���H2����Һ��˵����Һ�����ԣ���������Һ�в���������������A���ܴ������档B��˵������Һ��ˮ�ĵ��뱻���ƣ���Һ���������ԣ�Ҳ�����Լ��ԣ�����Լ��ԣ���Fe2+��NH4+���ܴ������档��������ԣ���Fe2+����ClO-�ᷢ��������ԭ��Ӧ������ѡ��B������һ�����ܴ������档C����Һ�Լ��ԣ����Դ������档D����Һ�����ԣ�S2-��SO32-����������ԭ��Ӧ������SO2�͵���S�����ܴ������档��ѡC��
�����Ѷȣ�һ��
2��ѡ���� Fe3+��SO42-��Al3+��X�������������ʵ���֮��2��4��1��1����������ͬһ��Һ�У�X�����ǣ�������
A��Na+
B��OH-
C��CO32-
D��Cl-
�ο��𰸣���Fe3+��SO42��Al3+��X�������������ʵ���֮��2��4��1��1��
����Һ�ʵ����Կ�֪��Fe3+��Al3+���������������SO42���ĵ������
��X���Ӵ��ĸ������Ϊx����
3��2+3��1=2��4+x��1�����x=1��
��XΪ��1����λ����ɵ������ӣ���OH-��Fe3+��Al3+������ɳ��������ܹ�����ͬһ��Һ��
��X����ΪCl-���ʴ�Ϊ��D��
���������
�����Ѷȣ���
3��ѡ���� ���и�������������Һ�д���������ǣ�������
A��Ba2+��H+��SO42-��CO32-
B��Na+��H+��Cl-��NO3-
C��Mg2+��H+��Cl-��OH-
D��Na+��NH4+��Cl-��OH-
�ο��𰸣�A��Ba2+��SO42-��Ӧ���ɳ�����H+��CO32-��Ӧ���������ˮ�����ܴ������棬��A����
B������֮�䲻�����κη�Ӧ���ɴ������棬��B��ȷ��
C��Mg2+��H+��OH-���ܴ������棬��C����
D��NH4+��OH-��Ӧ�����ܴ������棬��D����
��ѡB��
���������
�����Ѷȣ���
4������� ��15�֣���֪Cr(OH)3�ڼ��Խ�ǿ����Һ�н�����[Cr(OH)4]�D�����Ļ������ж�������+6�۸���ǿ�����ԣ��䶾����+3�۸����Ե�100������ˣ�����Ժ����ķ�ˮ���д������ɲ������»�ԭ���������Խ�������FeSO4�Ƚ�+6�۸���ԭ��+3�۸���
�����������£�
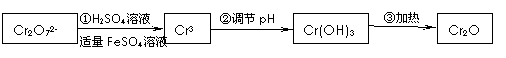
�й�������ȫ������pH���±���
�����
| Fe2+
| Fe3+
| Cr3+
|
��ȫ����Ϊ��Ӧ���������pH
| 9.0
| 3.2
| 5.6
|
��1��д��Cr2O72�D��FeSO4��Һ�����������·�Ӧ�����ӷ���ʽ���� ��������������������
��2����ԭ+6�۸�����ѡ�����µ������������Լ�������ţ���
A���������������� B����м������ ����C����ʯ�ҡ����� ������D������������
��3���ں�����ˮ�м���FeSO4���ٵ���pH��ʹFe3+��Cr3+�����������������
�ڲ������е���pHӦ��2�ν��У���1��Ӧ�ȵ�����Һ��pH��ΧԼ��������������ţ���ѣ���2��Ӧ������Һ��pH��ΧԼ��������������ţ����
A��3��4������ ��B��6��8������ ����C��10��11������������ D��12��14
���ڵ�����Һ������Լ�Ϊ����������������������������ţ���
A��Na2O2����������B��Ba(OH)2��������C��Ca(OH)2���������� D��NaOH
�ο��𰸣���15�֣���1��Cr2O72�D+ 6 Fe2+ + 14H+��2Cr3+ + 6Fe3+ + 7H2O
��2��BD?��3��A? B? D
�����������
�����Ѷȣ�һ��
5��ѡ���� ���и������ӣ�������Һ�д����������
A? H��?Na��?CO32�� Cl��? B?Ba2�� Na��?Cl�� SO42��
C? K��? H��? SO42��?OH��? D? Ag��? Al3��? NO3��?H��
�ο��𰸣�D
�����������
�����Ѷȣ�һ��