1��ѡ���� �������ӷ�Ӧ����ʽ����д��ȷ����
A.̼������Һ�м�������?CO32-+2H+=H2O+CO2��
B.ϡ�����м�������?2Fe+6H+=2Fe3++3H2��
C.̼����м�������?CO32-+2H+=H2O+CO2��
D.����������Һ�м�������?H++OH-=H2O
�ο��𰸣�A
���������������A��̼���ƺ����ᷴӦ�����Ȼ��ơ�������̼��ˮ��
B��ϡ���������Ӧ�����Ȼ�������������
C��̼�����������ˮ�ij�����
D���������������ᷴӦ�������ᱵ������ˮ��
���A��̼���ƺ����ᷴӦ�����Ȼ��ơ�������̼��ˮ����Ӧ�����ӷ���ʽΪ��CO32-+2H+=H2O+CO2������A��ȷ��
B��ϡ���������Ӧ�����Ȼ���������������Ӧ�����ӷ���ʽΪ��Fe+2H+=Fe2++H2������B����
C��̼�����������ˮ�ij����� ��Ӧ�����ӷ���ʽΪ��CaCO3+2H+=H2O+CO2��+Ca2+����C����
D���������������ᷴӦ�������ᱵ������ˮ����Ӧ�����ӷ���ʽΪ��Ba2++SO42-+2H++2OH-=2H2O+BaSO4������D����
��ѡA��
���������⿼�������ӷ���ʽ����дԭ���ע�����⣬��Ҫ�������ܽ��Ե��жϣ���Ӧԭ����ʵ�ʣ����ջ����ǹؼ�����Ŀ�ϼ�
�����Ѷȣ�����
2��ѡ���� 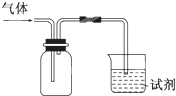 ��ͼװ�ÿ������ռ�SO2����֤��ijЩ��ѧ���ʣ�����˵����ȷ����
��ͼװ�ÿ������ռ�SO2����֤��ijЩ��ѧ���ʣ�����˵����ȷ����
A.A
B.B
C.C
D.D
�ο��𰸣�B
���������������A����������ʹ���������Һ�����ֵ��Ƕ�������Ļ�ԭ�ԣ�
B����������ʹƷ����ɫ�����ֶ��������Ư���ԣ�
C���������������������ܷ�Ӧ��������������
D����Ϊ���������Ư����һ����ѡ���ԣ�����Ư��ʯ��ȣ����������ԣ����������˵û��Ư���ԣ�
���A�����Ը�������ܽ�����������ˮ��Һ�����������ᣬ������ԭΪ��ɫ�Ķ��������ӣ������Ը�����ص������Ե����֣��������ֵ��Ƕ�������Ļ�ԭ�ԣ���A����
B��ʹƷ����Һ��ɫ��������Ӧ���������ɲ��ȶ��Ļ�������Ⱥ��ָֻ�Ϊԭ���ĺ�ɫ�������˶��������Ư���ԣ���B��ȷ��
C����������Ϊ����������ܸ��������Ʒ�Ӧ�����������ƺ�ˮ��������������C����
D����������ʹ��ɫʯ����Һ������ɫ�����������ԣ����������˵û��Ư���ԣ���Ϊ���������Ư����һ����ѡ���ԣ�����Ư��ʯ��ȣ���D����
��ѡB��
���������⿼�������������ʣ���������Ϊ������������������������ͨ�ԣ�����������Ư���ԡ�ǿ��ԭ�Ե��������ԣ����������Ư����ѡ���ԣ�
�����Ѷȣ�һ��
3��ѡ���� �����ʵ����������л�����ȫȼ�գ�����CO2����������
A.CH4
B.C2H6
C.C3H6
D.C6H6
�ο��𰸣�D
�����������������������ʵ�������ȵ������£��л�����̼ԭ����Խ�࣬��ȫȼ�����ɵ�CO2��Խ�࣬������л���Ļ�ѧʽ��֪��Dѡ����̼ԭ������࣬���ɵ�CO2��࣬��ѡD��
���㣺�����л����ȼ�յ��йؼ���
�����������Ǹ߿��ж�����ͣ������е��Ѷȵ����⣬���������ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������Ĺؼ������ú�ԭ���غ㣬���Ҫ�ر�ע�����Ҫ����������ʵ�����ȣ�����������ȣ�Ȼ����������йط���ʽ������ü��ɡ�
�����Ѷȣ�����
4��ѡ���� �������ӷ���ʽ��д��ȷ����
A.�����Ȼ�ͭ��Һ��Ӧ?Al+Cu2+�TAl3++Cu
B.��NaAlO2?��Һ��ͨ�����CO2?AlO2-+CO2+2H2O�TAl��OH��3��+HCO3-
C.���������Һ��ͨ��SO2����? Ca2++2C1O-+SO2+H2O�TCaSO3��+2HClO
D.�����ʯ��ˮ�м��������̼��������Һ? Ca2++2OH-+2HCO3-�TCaCO3��+2H2O+CO32-
�ο��𰸣�BD
���������������A�����ӷ���ʽ�ĵ�ɲ��غ㣻
B��̼�������ǿ��������������϶�����̼�ǹ���������̼��������ӣ�
C�����������ǿ�������ܰѶ�����������Ϊ���
D����ʽ�κͼӦ�����ٵ�ȫ����Ӧ�����ӷ���ʽ�����������и����Ӻ����������ӱ�����ϻ�ѧʽ����ɱ�1��2��
���A�������Ȼ�ͭ��Һ��Ӧ�����ӷ���ʽΪ2Al+3Cu2+�T2Al3++3Cu����A����
B����NaAlO2?��Һ��ͨ�����CO2�����ӷ���ʽΪAlO2-+CO2+2H2O�TAl��OH��3��+HCO3-����B��ȷ��
C�����������Һ��ͨ��SO2���壬�ܰѶ�����������Ϊ���ᣬ���ӷ���ʽΪ2C1O-+SO2+H2O�TSO42-+2H++2Cl-����C����
D�������ʯ��ˮ�м��������̼��������Һ�����ӷ�ӦΪCa2++2OH-+2HCO3-�TCaCO3��+2H2O+CO32-����D��ȷ��
��ѡBD��
���������⿼�������ӷ���ʽ����дԭ���ע�����⣬��Ҫ�������ӷ���ʽ�ĵ���غ㣮ԭ���غ㣬����ͬ���ﲻͬ���ؼ��Ǵ������ǿ�����Ե��жϣ�
�����Ѷȣ���
5��ѡ���� ��һ��������þ��ͭ��ɵĻ�����������ϡ�����У�������ȫ�ܽ⣨���跴Ӧ�л�ԭ����ȫ����NO������Ӧ�����Һ�м��������6mol/L?NaOH��Һ��������ȫ��������ɳ�����������ԭ����������������7.65g����������������ȷ����
A.������ȫ���ܽ�ʱ�ռ���NO�����Ϊ3.36?L
B.�����ɵij����ﵽ�����ʱ���γɳ�����ҪNaOH��Һ�����ΪV=75?mL
C.�μӷ�Ӧ�Ľ�����������һ����9.9?g
D.������ȫ���ܽ�ʱ���μӷ�Ӧ����������ʵ���һ����0.45?mol
�ο��𰸣�B
�����������������һ������þ��ͭ��ɵĻ������뵽ϡHNO3�У�������ȫ�ܽ⣨���跴Ӧ�л�ԭ����ֻ��NO����������Ӧ��3Mg+8HNO3 ��ϡ��=3Mg��NO3��2+2NO��+4H2O��3Cu+8HNO3 ��ϡ��=3Cu��NO3��2+2NO��+4H2O��
��Ӧ�����Һ�м��������6mol/L?NaOH��Һ��������ȫ��������Ӧ��Mg��NO3��2+2NaOH=Mg��OH��2��+2NaNO3��Cu��NO3��2+2NaOH=Cu��OH��2��+2NaNO3������Ϊ������þ��������ͭ�����ɳ�����������ԭ�Ͻ����������7.65g����������þ��������ͭ����������������Ϊ7.65g�������������ʵ���Ϊ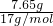 =0.45mol����þ��ͭ���ܵ����ʵ���Ϊ0.225mol��
=0.45mol����þ��ͭ���ܵ����ʵ���Ϊ0.225mol��
A�����ݵ���ת���غ����NO���ʵ�����������岻һ���DZ�״���жϣ�
B�������ɵij����ﵽ�����ʱ����Һ������ΪNaNO3��������غ��֪n��NaNO3��=2n������ͭ+����þ�������������غ���n��NaOH��=n��NaNO3�����ٸ���V= ���㣻
���㣻
C��þ��ͭ���ܵ����ʵ���Ϊ0.225mol��������������������ĺ����йأ�
D�����ݵ�Ԫ���غ�n��HNO3��=2n������ͭ+����þ��+n��NO����
��𣺽�һ������þ��ͭ��ɵĻ������뵽ϡHNO3�У�������ȫ�ܽ⣨���跴Ӧ�л�ԭ����ֻ��NO����������Ӧ��3Mg+8HNO3 ��ϡ��=3Mg��NO3��2+2NO��+4H2O��3Cu+8HNO3 ��ϡ��=3Cu��NO3��2+2NO��+4H2O��
��Ӧ�����Һ�м��������6mol/L?NaOH��Һ��������ȫ��������Ӧ��Mg��NO3��2+2NaOH=Mg��OH��2��+2NaNO3��Cu��NO3��2+2NaOH=Cu��OH��2��+2NaNO3������Ϊ������þ��������ͭ�����ɳ�����������ԭ�Ͻ����������7.65g����������þ��������ͭ����������������Ϊ7.65g�������������ʵ���Ϊ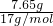 =0.45mol����þ��ͭ���ܵ����ʵ���Ϊ0.225mol��
=0.45mol����þ��ͭ���ܵ����ʵ���Ϊ0.225mol��
A�����ݵ���ת���غ��֪���ɵ�NO���ʵ���Ϊ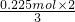 =0.15mol����Ϊ��״���£�����NO�����Ϊ0.15mol��22.4L/mol=3.36L����NO��һ�����ڱ�״������A����
=0.15mol����Ϊ��״���£�����NO�����Ϊ0.15mol��22.4L/mol=3.36L����NO��һ�����ڱ�״������A����
B�������ɵij����ﵽ�����ʱ����Һ������ΪNaNO3��������غ��֪n��NaNO3��=2n������ͭ+����þ��=0.225mol��2=0.45mol�����������غ���n��NaOH��=n��NaNO3��=0.45mol���ʴ�ʱ����������Һ�����Ϊ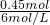 =0.075L=75mL����B��ȷ��
=0.075L=75mL����B��ȷ��
C��þ��ͭ���ܵ����ʵ���Ϊ0.225mol���ٶ�ȫΪþ������Ϊ0.225mol��24g/mol=5.4g����ȫΪͭ������Ϊ0.225mol��64g/mol=14.4g�����Բμӷ�Ӧ�Ľ�������������m��Ϊ5.4g��m��14.4g����C����
D�����ݵ�Ԫ���غ�n��HNO3��=2n������ͭ+����þ��+n��NO��=0.225mol��2+0.15mol=0.6mol����D����
��ѡB��
������������Ҫ���������йؼ��㣬�漰þͭ�����ᷴӦ�����ɵ������������Ʒ�Ӧ���ۺϿ���ѧ���ĵ�ʧ�����غ㡢�����غ���ۺ����úͽ�������������������һ�����������ĺ��⣬�ѶȽϴ�
�����Ѷȣ�һ��