1、选择题 COCl2俗称光气,是有毒气体。在一定条件下,可发生的化学反应为:
COCl2(g) ?CO(g)+Cl2(g) ΔH<0 下列有关说法正确的是( )
?CO(g)+Cl2(g) ΔH<0 下列有关说法正确的是( )
A.在一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
B.当反应达平衡时,恒温恒压条件下通入Ar,能提高COCl2的转化率
C.单位时间内生成CO和Cl2的物质的量之比为1∶1时,反应达到平衡状态
D.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
参考答案:B
本题解析:A:催化剂只能等倍数的增大正逆反应速率,但平衡不会移动,即不会改变反应的转化率;B:在应达平衡时,恒温恒压条件下通入Ar,反应混合物质浓度同倍数减小,相当于减压,平衡右移,故能提高COCl2的转化率;C:任何时间内生成CO和Cl2的物质的量之比均为1∶1,并不能说明反应达到平衡状态。D:升温,平衡向吸热反应方向移动,即左移,平衡常数将减小。
本题难度:一般
2、选择题 在容积可变的密闭容器中,2?mol?N2和8?mol?H2在一定条件下反应,达到平衡时,H2的转化率为25%,则平衡时氨气的体积分数接近于
[? ]
A.5%?
B.10% ?
C.15%?
D.20%
参考答案:C
本题解析:
本题难度:一般
3、选择题 可逆反应N2O4 2NO2△H>0在密闭容器中反应,达到平衡状态,要使混合气体颜色加深,可采取的方法是?①减小压强 ②缩小体积③升高温度④增大N2O4的浓度?(?)?
2NO2△H>0在密闭容器中反应,达到平衡状态,要使混合气体颜色加深,可采取的方法是?①减小压强 ②缩小体积③升高温度④增大N2O4的浓度?(?)?
A.②③④
B.①②③
C.①③④
D.①②③④
参考答案:A
本题解析:由题意要使气体的颜色加深,需改变条件使平衡向正反应方向进行,所以A对;减小压强需增大容器体积,气体颜色会变浅,所以错误。
本题难度:一般
4、选择题 在一定温度下,将1 mol N2和3 mol H2放入恒容密闭容器中,达到平衡时,测得NH3为0.8 mol,如果此时再加入1 mol N2和3 mol H2,达到新平衡时,NH3的物质的量
A.等于0.8 mol
B.等于1.6 mol
C.大于0.8 mol小于1.6 mol?
D.大于1.6 mol
参考答案:C
本题解析:再加入1 mol N2和3 mol H2,相当于增大压强,平衡向逆反应方向移动,反应物的转化量降低,所以最终平衡时氨气的物质的量小于1.6mol,但大于0.8mol,所以选项C正确,答案选C。
本题难度:一般
5、选择题 一定温度下,对可逆反应A(g)+2B(g)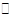 3C(g)的下列叙述中,能说明反应已达到平衡的是
3C(g)的下列叙述中,能说明反应已达到平衡的是
A.单位时间内消耗a mol A,同时生成3a mol C
B.当3v(B)正="2" v(C)逆
C.容器内的压强不再变化
D.混合气体的物质的量不再变化
参考答案:B
本题解析:当化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变,注意该反应是一个反应前后气体体积不变的可逆反应。
A、同为正反应速率,故错;CD、反应前后气体的体积不变,故容器内的压强、混合气体的物质的量一直不变,故错。故选B。
点评:本题考查化学平衡状态的判断,题目难度不大,本题注意化学平衡的特征,只有反应前后改变的物理量才能作为判断平衡状态的依据。
本题难度:简单