1、选择题 降低下列溶液的pH,而难溶电解质的溶解度保持不变的是
A.Al(OH)3
B.PbCl2
C.Ag3PO4
D.ZnCO3
参考答案:B
本题解析:降低溶液的pH,Al(OH)3、Ag3PO4、ZnCO3的溶解平衡均正向移动,溶解度增大,甚至全部溶解,而PbCl2并没有受影响,答案为B
本题难度:一般
2、填空题 工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
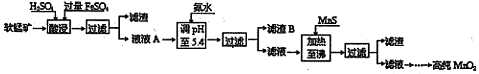
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表。

回答下列问题:
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的离子方程式为?。
(2)调节pH时不用氢氧化钠原因是:?,理论上,调节pH的最小值为?,滤渣B的主要成分是?。
(3)加入MnS的目的是除去?杂质。
(4)碱性锌锰电池中,MnO2参与的电极反应方程式为?。回收废旧碱性锰电池中的锰,可向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止,其主要反应为:2MnO(OH)+MnO2 +2H2C2O4 +3H2SO4=3MnSO4 +4CO2 ↑+6H2O,该方法的优点是?。
参考答案:(1)MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O
(2)使Al(OH)3溶解、使Mn2+沉淀? 5.2 Fe(OH)3、 Al(OH)3
(3)Cu2+? Zn2+
(4)MnO2+H2O+e-=MnOOH+OH-(或2MnO2+H2O+2e-=Mn2O3+2OH-)?工艺流程简单;生成CO2和H2O不影响MnSO4纯度;反应过程无有毒有害物质生成,不造成二次污染;废物资源化等。
本题解析:(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4的离子方程式为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O。(2)调节pH时不用氢氧化钠是因为若使用NaOH溶液,溶液因过量而使Al(OH)3溶解、使Mn2+沉淀 。(3)加入MnS的目的是除去杂质离子Cu2+ 和 Zn2+ 。(4)碱性锌锰电池中,MnO2参与的电极反应方程式为MnO2+H2O+e-=MnOOH+OH-;回收废旧碱性锰电池中的锰,可向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止,其主要反应为:2MnO(OH)+MnO2 +2H2C2O4 +3H2SO4=3MnSO4 +4CO2 ↑+6H2O,其优点是工艺流程简单,反应生成的CO2和H2O不影响MnSO4纯度;反应过程没有毒有害物质生成,不造成二次污染;废物资源化等。2参与的反应、废旧电池的Mn的回收、利用的方法及优点等知识。
本题难度:困难
3、选择题 CaF2的Ksp=5.3×10-9 mol3/L3,在F-浓度为3.0mol/L的溶液中,Ca2+可能的最高浓度是(?)
A.1.8×10-9 mol/L
B.1.9×10-10 mol/L
C.5.9×10-10 mol/L
D.5.9×10-9 mol/L
参考答案:D
本题解析:由Ksp=[Ca2+]・[F-]2=5.3×10-9 mol3/L3,[Ca2+]= =
=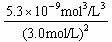 =5.9×10-9 mol/L。
=5.9×10-9 mol/L。
本题难度:一般
4、选择题 下列说法中正确的是? ( )
A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大
B.AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小
Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小
C.AgCl悬浊液中加入KI溶液,白色沉淀变成黄色,证明此条件下Ksp(AgCl)>Ksp(AgI)
D.硬水中含有较多的 Ca2+、Mg2+、HCO3―、SO42―,加热煮沸可以完全除去其中的Ca2+、Mg2+
参考答案:C
本题解析:A项中Ca(OH)2的溶解度随温度的升高而降低,溶液中c(OH-)减小,故所得溶液的pH减小,A错误;B项中加入NaCl,增大了Cl-的浓度,平衡左移,同时Na+的浓度增大,因此溶液中离子的总浓度不会减小,B错误;根据沉淀的转化理论可知,C正确;加热煮沸只能使部分Ca2+、Mg2+除去,但不可能完全除去,D错误。
本题难度:一般
5、填空题 酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式。SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备路线如下:

回答下列问题:
(1)SnCl2用盐酸而不用水直接溶解的原因是
加入锡粉的作用是
(2)反应I生成的沉淀为SnO,写出该反应的化学方程式:
(3)检验沉淀已经“洗涤”干净的操作是: (3分)
(4)反应Ⅱ硫酸的作用之一是控制溶液的pH。若溶液中c(Sn2+)=1.0mol・L―1,则室温下应控制溶液pH 。(已知:Ksp[Sn(OH)2]=1.0×10―26)
(5)酸性条件下,SnSO4还可用作双氧水的去除剂,试写出所发生反应的离子方程式:
。
(6)潮湿环境中,镀锡铜即使锡层破损也能防止形成铜绿,请结合有关的原理解释其原因:
。
参考答案:(1)抑制Sn2+水解, 防止Sn2+被氧化 (2)SnCl2 + Na2CO3 =" SnO" + CO2↑+2NaCl(3)取少量最后一次洗涤液于试管中,滴入几滴AgNO3溶液,若无白色沉淀生成,则说明沉淀已洗涤干净(3分)(4)小于1 (2分。若写成≤1给1分) (5)Sn2+ + H2O2 + 2H+ = Sn4+ + 2H2O (6)潮湿环境中,Sn与Cu构成原电池,Sn作为负极,保护正极Cu不被氧化
本题解析:(1)SnCl2易水解生成碱式氯化亚锡,存在平衡Sn Cl2+H2O?Sn(OH)Cl+HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解;Sn2+易被氧化,加入Sn粉除调节溶液pH外,还防止Sn2+被氧化;(2)反应Ⅰ得到沉淀是SnO,Sn元素化合价为变化,属于非氧化还原反应,同时生成气体,该气体为二氧化碳,离子方程式为:Sn2++CO32-
本题难度:困难