1、选择题 短周期元素X、Y、Z和W的原子序数依次增大,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是Z元素形成的单质。已知:甲+乙→丁 +己,甲+丙→戊+己;0.1mol ?l-1 丁溶液的pH为13(250C)。下列说法正确的是:
A.原子半径:W>Z>Y>X
B.Y元素在周期表中的位置为第三周期第IVA族
C.X元素与Y元素形成的原子个数比为1:1的化合物有多种
D.1.0L 0.1mol ?l-1戊溶液中阴离子总物质的量小于0.1 mol
参考答案:C
本题解析:由0.1 mol?L-1丁溶液的pH为13(25℃)可知,丁是一元强碱且其中的金属元素在短周期,甲+乙→丁+己,甲+丙→戊+己;则“己”是氧气,“丁”是氢氧化钠,则甲是Na2O2、乙是水,丙是二氧化碳,戊是碳酸钠,因此X为氢、Y为碳、Z为氧、W为钠元素。A、由以上分析可知:X为氢、Y为碳、Z为氧、W为钠元素,则原子半径大小顺序为:Na>C>O>H,即:W>Y>Z>X,故A错误;B、Y为碳,在周期表中的位置为:第二周期第ⅣA族,故B错误;C、H元素与C元素形成的原子个数比为1:1的化合物有多种,例如乙炔、苯、苯乙烯等,故C正确;D、戊是碳酸钠,在碳酸钠溶液中,CO32-离子水解生成HCO3-离子和OH-离子,所以溶液中阴离子总的物质的量大于0.1mol,故D错误,答案选C。
本题难度:一般
2、选择题 下列各组微粒具有相同的质子数和电子数的是
A.OH-、H2O、F-
B.NH3、NH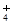 、NH
、NH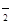
C.H3O+、NH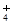 、NH
、NH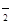
D.HCl、F2、H2S
参考答案:D
本题解析:A中质子数不同,电子数相同。B中质子数不同,电子数相同。C中也是质子数不同,电子数相同。选项D中质子数相同都是18,电子数也相同,也是18。答案选D。
本题难度:一般
3、选择题 能说明Cl的非金属性比S的非金属性强的事实是
A.Cl2与H2反应生成HCl,而S与H2反应生成H2S
B.Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
C.Cl2能与水反应,而S不与水反应
D.Cl原子最外层电子数为7,而S原子最外层电子数为6
参考答案:B
本题解析:略
本题难度:一般
4、填空题 (14分)X、Y、Z三种化合物均由短周期元素组成。已知三种化合物的水溶液的焰色反应均呈黄色,Y和Z均由三种元素组成。请根据题目的要求回答下列问题。
(1)固体化合物X为浅黄色粉末,该化合物中含有化学键为?(填序号)。
A.离子键? B.极性共价键? C.非极性共价键
(2)写出X与二氧化碳反应的化学方程式?。
(3)下表为Y和Z实验的部分内容
序号
| 主要实验步骤及实验现象
|
①
| 在Y的无色溶液中,加入稀硫酸,放置。产生浅黄色沉淀和无色有刺激性气味的气体。该气体可使品红溶液褪色。
|
②
| 在Z的无色溶液中,滴加的盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀。
|
③
| 将实验②最终得到的混合物加热蒸发、灼烧,最终得到固体。
|
写出含0.1 mol Z的溶液与20 mL 5mol/L的盐酸反应的离子方程式:
?
实验③加热蒸发、灼烧得到的最终产物主要是?和?。
(4)写出Y与稀硫酸反应的离子方程式?。
参考答案:(1)AC;(2)2Na2O2 + 2CO2 = 2Na2CO3 + O2↑;
(3)AlO2―+ H+ + H2O = Al(OH)3↓;NaCl和Al2O3;
(4)S2O32―+2H+=S↓+SO2↑+H2O
本题解析:根据焰色反应可知均为钠盐,固体化合物X为过氧化钠,Y 为Na2S2O3,Z为NaAlO2?。2Na2O2 + 2CO2 = 2Na2CO3 + O2↑;AlO2―+ H+ + H2O = Al(OH)3↓;S2O32―+2H+=S↓+SO2↑+H2O。
本题难度:一般
5、选择题 某元素X所形成的分子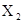 共有3种,其相对分子质量依次为158、160、162,其三种分子的物质的量之比是7:10:7则下列结论正确的是?(? )
共有3种,其相对分子质量依次为158、160、162,其三种分子的物质的量之比是7:10:7则下列结论正确的是?(? )
A.X有三种同位素
B.其中一种同位素的原子质量数为81
C.质量数为79的同位素,其原子质量分数为50%
D.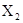 的平均相对分子质量为159
的平均相对分子质量为159
参考答案:B
本题解析:根据X元素可以形成3种分子可知,X应该有2种同位素。根据分子的相对分子质量可知,同位素的质量数分别是79和81。又因为三种分子的物质的量之比是7:10:7,所以两种同位素原子的个数之比是1:1的,则质量数为79的同位素,其原子质量分数小于50%,X的平均相对分子质量是80,则分子的平均相对分子质量是160,因此正确的答案选B。
点评:该题是中等难度的试题,试题综合性强,在注重对学生基础性知识考查与训练的同时,侧重对学生能力的培养。该题的关键是借助于数学中的排列组合得出含有2种同位素原子,然后在根据元素相对原子质量的计算依据,并结合题意灵活运用即可,有助于培养学生的逻辑思维能力和抽象思维能力。
本题难度:简单