|
高考化学知识点总结《二氧化硫》考点强化练习(2017年押题版)(二)
2017-11-11 03:50:15
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
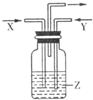
1、选择题 下列各组物质中,气体X和气体Y同时通人盛有溶液z的洗气瓶中(如图),一定没有沉淀生成的
| X | Y | Z
A
NO2
SO2
BaCl2
B
NH3
CO2
Al(SO4)3
C
NH3
CO2
CaCl2
D
CO2
SO2
CaCl2
|
( )
A.A
B.B
C.C
D.D
| 
参考答案:D
本题解析:
本题难度:一般
2、选择题 下列关于二氧化硫的叙述中错误的是?
[? ]
A.在高温下二氧化硫可被催化氧化成三氧化硫
B.二氧化硫可使品红溶液褪色
C.二氧化硫既具有氧化性又具有还原性
D.二氧化硫与水反应生成硫酸
参考答案:D
本题解析:
本题难度:简单
3、填空题 某教师在课堂上用右图所示的装置来验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质.请答下列问题:
(1)通过试管乙中发生的______
现象说明了铜和浓硫酸发生了化学反应,
并且该现象还能说明产生的气体具有______性.
(2)写出试管甲中所发生反应的化学方程式,并标明电子转移方向和数目______.
(3)试管乙口部浸有碱液的棉花的作用是______,此防范措施也说明产生的气体是______(填“酸性”、“中性”或“碱性”)气体,______(填“有”或“无”)毒性.
(4)SO2的排放是造成酸雨的主要因素,某同学通过实验探究,得出酸雨pH随时间的增加而减小的结论.为进一步研究酸雨的成分,该同学取某一时段的这种雨水V?L,加入0.5mol/L的Ba(OH)2溶液至不再产生沉淀时,恰好消耗40.00mL?Ba(OH)2溶液.请计算:
①该雨水中共溶解SO2的体积是______mL(标准状况).
②若生成沉淀物的质量为4.50g,则沉淀物的组成为______(填写化学式).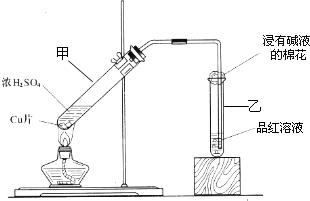
参考答案:(1)金属铜和浓硫酸发生反应生成硫酸铜、水和二氧化硫,生成的二氧化硫能使品红褪色,说明二氧化硫具有漂白性,故答案为:品红溶液褪色;漂白;
(2)金属铜和浓硫酸发生反应生成硫酸铜、水和二氧化硫Cu+2H2SO4?△?.?CuSO4+SO2↑+2H2O,化合价的升高值=化合价的降低值=转移电子数=2,电子转移情况如下:
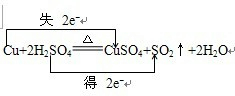
,故答案为:

;
(3)二氧化硫有毒,属于酸性氧化物,能和碱反应生成盐和水,在装置口处浸有碱液的棉花可以和二氧化硫反应,故答案为:吸收SO2;酸性;有;
(4)①二氧化硫和氢氧化钡的反应方程式为:SO2+Ba(OH)2=BaSO3↓+H2O,设该雨水中共溶解SO2的体积是x,则
? SO2 +Ba(OH)2=BaSO3↓+H2O
? 1? 1
?x22.4L/mol?0.5 mol/L×0.04L
则x22.4=0.02,解得x=0.448L=448mL,故答案为:448;
②0.5mol/L、40.00mL?的Ba(OH)2溶液和二氧化硫反应,如果全部转化为亚硫酸钡,根据钡原子守恒,则生成亚硫酸钡的质量为:0.02mol×217g/mol=4.34g,如果全部转化为硫酸钡,根据钡原子守恒,则生成硫酸钡的质量为:0.02mol×233g/mol=4.66g,4.34g<4.50g<4.66g,所以沉淀物的组成为BaSO3和BaSO4,故答案为:BaSO3和BaSO4.
本题解析:
本题难度:一般
4、填空题 黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2 8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是______________(填元素符号)。
(2)上述冶炼过程产生大量SO2。下列处理方案中合理的是______________(填代号)。
a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制NaSO3 d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可I-将氧化为I2:S2O82-+2I-==2SO42-+I2
通过改变反应途径,Fe2+、Fe3+均可催化上述反应。试用离子方程式表示Fe3+对上述反应催化的过程
________________________,___________________________。(不必配平)
参考答案:(1)Cu、O
(2)bc
(3)Fe3++I-→Fe2++I2;S2O82-+Fe2+→SO42-+Fe3+
本题解析:
本题难度:一般
5、选择题 将等物质的量的SO2和Cl2混合后通入含有品红和Ba(NO3)2的混合溶液里,发生的现象是?
①溶液很快褪色 ②溶液不褪色?③有沉淀生成 ④溶液仍然透明? ?
[? ]
A、仅①和④ ?
B、仅①和③ ?
C、仅②和③ ?
D、仅②和④?
参考答案:B
本题解析:
本题难度:简单
| 