1������� ��������������ӭ�������ֱ�������ֲ�ͬ��ɫ�ĵ��ʣ�����֮��������γ�����ͼ��ʾ�İ����廷�죬A��B��C��D��E��F��G��H�����ཻ�������Ԫ����ɵĻ����
��֪����ɫ�ġ�������Һ̬O2����ɫ�ġ������ǹ�̬�ǽ������ʣ�1mol?G����1mol������ǡ�÷�Ӧ����1mol?H��F����Һ����A��Ӧ������M����N��E����Һ��C�������տ��Ƶ�A���˷�Ӧ�ǹ�ҵ����ȡ��M�Ļ�����Ӧ����ش��������⣺
��1����������______����������ͬ����������______��
��2��д��F����Һ��A��Ӧ������M����N��E����Һ�Ļ�ѧ����ʽ��______���÷�ӦΪ������ԭ��Ӧ����ԭ����Ϊ______��
��3����ҵ����CΪ����ԭ�ϣ���ȡ��M�����Ĺ�ҵβ��ֱ���ŷŵ������л���ɻ�����Ⱦ��������β�����Եõ�һ�ֻ��ʣ�д���÷��ϵĻ�ѧʽ��______��
��4����֪��P��s��+
Cl2��g��=PCl3��g������H=-287.7kJ/mol��P��s��+Cl2��g��=PCl5��g������H=-498.7kJ/mol����PCl5��g���ֽ�����PCl3��g����Cl2��g����Ӧ���Ȼ�ѧ����ʽΪ��______��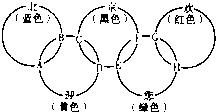
�ο��𰸣��ɵ��ʵ���ɫ��֪��ΪFe����ΪP��ӭΪS����ΪCl2��C�������տ��Ƶ�A��AΪSO2��BΪSO3��P��Cl2��Ӧ������PCl3��PCl5��1mol?G����1mol������ǡ�÷�Ӧ����1molH����GΪPCl3��HΪPCl5��Fe��ClԪ�ؿ����FeCl2��FeCl3�����и���F����Һ��A��Ӧ������M����N��E����Һ��˵��FΪFeCl3��EΪFeCl2��S��Fe�����FeS2��FeS����ҵ����FeS2Ϊԭ���������ᣬ
��1�������Ϸ�����֪�������������������Ǻ��ף���Ӧ��ͬ���������ǰ��ף��ʴ�Ϊ���������ף�
��2��FeCl3���������ԣ�SO2���л�ԭ�ԣ����߷���������ԭ��Ӧ��
��Ӧ�ķ���ʽΪ2FeCl3+SO2+2H2O�TH2SO4+2HCl+2FeCl2���ɻ��ϼ۵ı仯��֪��ԭ��ΪFeCl2��
�ʴ�Ϊ��2FeCl3+SO2+2H2O�TH2SO4+2HCl+2FeCl2��FeCl2��
��3��S��Fe�����FeS2��FeS����ҵ����FeS2Ϊԭ���������ᣬ��CΪFeS2�����ɵ�SO2����Ⱦ���������ð������������յõ���NH4��2SO4���ʴ�Ϊ����NH4��2SO4��
��4����֪����P��s��+32Cl2��g��=PCl3��g����H=-287.7kJ/mol��
��P��s��+52Cl2��g��=PCl5��g����H=-498.7kJ/mol��
���ø�˹���ɣ�����-�ڿɵ�PCl5��g���TCl2��g��+PCl3��g����H=��-287.7kJ/mol��-��-498.7kJ/mol��=+211.0kJ/mol��
�ʴ�Ϊ��PCl5��g���TCl2��g��+PCl3��g����H=+211.0kJ/mol��
���������
�����Ѷȣ�һ��
2���ƶ��� ��ͼ���漰�����ʾ�Ϊ��ѧ��ѧ�еij������ʣ�����C��D��EΪ���ʣ�EΪ���壬FΪ�д��ԵĻ��������֮��������¹�ϵ����Ӧ�����ɵ�ˮ����Ҫ���������ȥ��
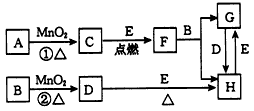
(1)д���������ʵĻ�ѧʽB_________��E___________��
(2)ָ��MnO2����ط�Ӧ�е����ã���Ӧ������_______������Ӧ������________����
(3)����Ӧ�����ڼ��������½��У���A��_________���ѧʽ��������Ӧ�����ڳ��������½��У���A��_________���ѧʽ���������������������µõ���������C���ʣ���Ӧ��ת�Ƶĵ�����֮��Ϊ____________��
�ο��𰸣�(1)HCl��Fe
(2)��������
(3)KClO3��H2O2��2:1
���������
�����Ѷȣ�һ��
3������� ��ѧ������ѧ��Ӧ����ʽΪ��A+B��X+Y+H2O��δ��ƽ����Ӧ������ȥ�������У�A��B�����ʵ���֮��Ϊ1:4����ش�
��1����YΪ����ɫ���壬�÷�Ӧ�����ӷ���ʽΪ??��B���ֳ��Ļ�ѧ������??
��2����AΪ�����ķǽ������ʣ�B����ҺΪijŨ�ᣬ��Ӧ����Ϊ���ȣ��䷴Ӧ�Ļ�ѧ����ʽΪ?
��3����AΪij�����õĽ������ʣ�ʵ���ҳ��ø÷�Ӧ���Ʊ�ij�����γ���������壬�÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ?
��4����AΪ�����Ľ������ʣ�������A��B��Ũ��Һ�С��ۻ�������A������X��Һ�С�
��AԪ����Ԫ�����ڱ��е�λ����?
�ں�amolX����Һ�ܽ���һ����A������Һ�����ֽ��������ӵ����ʵ���ǡ����ȣ���ԭ��X�����ʵ�����?
�ο��𰸣�
��1��MnO2+4H++2Cl�� Mn2++2H2O+Cl2��?���Ժͻ�ԭ��
Mn2++2H2O+Cl2��?���Ժͻ�ԭ��
��2��C+4HNO3(Ũ�� CO2��+4NO2��+2H2O
CO2��+4NO2��+2H2O
��3���漰��ӦΪ��Cu��4HNO3(Ũ)��Cu(NO3)2��2NO2����2H2O ���������뻹ԭ�������ʵ���֮��Ϊ? 2:1
��4���ٵ������ڵڢ���?��0��4a ����2�֡�
�����������1������ɫ����һ��Ϊ��������˷�ӦΪ��MnO2+4H++2Cl�� Mn2++2H2O+Cl2�� ���������Ӧ��������ֳ���������Ϊ�����Ժͻ�ԭ�ԡ�
Mn2++2H2O+Cl2�� ���������Ӧ��������ֳ���������Ϊ�����Ժͻ�ԭ�ԡ�
��2��C+4HNO3(Ũ�� CO2��+4NO2��+2H2O
CO2��+4NO2��+2H2O
��3��2:1
��4���������֪������Ԫ��ΪFe���������ڱ��е�λ��Ϊ���������ڵڢ���?
��? Fe?��? 2Fe3��?��? 3Fe2��
��ʼ��Xmol? 2amol? 0
��Ӧ��bmol? 2bmol ?3bmol
���գ���x-b��mol? (2a-2b)mol? 3bmol
��������ṩ������(2a-2b)= 3b������b=0��4a
��˱���ԭ��Fe3�������ʵ���Ϊ0��8a����ô����ԭ��XΪ0��4amol��
�����Ѷȣ�����
4������� ����ͬѧ��̽��һ���غ�ɫ��״�������Ҫ�ɷ֣���������Ԫ����ɣ������ù�������ϡ�����������A�ų������õ�dz��ɫ��ҺB��A�ڿ����г��ȼ�գ��ֵõ���ɫ�д̼�����ζ������C����������ʹƷ����Һ��ɫ����B��Һ�м������������������Һ�����ȵõ���ɫ������Ȼ�����Ѹ�ٱ�Ϊ����ɫ������Ϊ���ɫ��
��������ʵ������ش�
��1�����غ�ɫ��״�������Ҫ�ɷ��ǣ�д��ѧʽ��______��
��2��������д������������C���ɵ�������ԭ��Ӧ����ʽ��
��______��
��______��
��3����д����ɫ������ɺ��ɫ�����Ļ�ѧ����ʽ��______��
��4�������ɫ��������ϡ�������������Һ�еĽ��������ӣ���ѡ�õ��Լ���______��
�ο��𰸣����ù�������ϡ�����������A�ų������õ�dz��ɫ��ҺB��˵��B�к����Ȼ�������A�ڿ����г��ȼ�գ��ֵõ���ɫ�д̼�����ζ������C����������ʹƷ����Һ��ɫ����C�Ƕ�������A�����⣬��B��Һ�м������������������Һ�����ȵõ���ɫ������Ȼ�����Ѹ�ٱ�Ϊ����ɫ������Ϊ���ɫ����˵��B���������Ȼ��������غ�ɫ��������ᷴӦ�����Ȼ����������⣬����غ�ɫ������FeS��
��1��ͨ�����Ϸ���֪��A�Ļ�ѧʽ��FeS���ʴ�Ϊ��FeS��
��2������������ȼ�����ɶ�������ͭ��Ũ�����ڼ��������·�Ӧ���ɶ������������䷽��ʽ�ֱ�Ϊ��
S+O2?��ȼ?.?SO2��Cu+2H2SO4��Ũ��?��?.?CuSO4+SO2 ��+2H2O��
�ʴ�Ϊ��S+O2?��ȼ?.?SO2��Cu+2H2SO4��Ũ��?��?.?CuSO4+SO2 ��+2H2O��
��3��������������������������������������Ӧ����ʽΪ4Fe��OH��2+O2+2H2O=4Fe��OH��3��
�ʴ�Ϊ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��4�������Ӻ����軯����Һ��Ӧ����������ʹ��Һ��Ѫ��ɫ���ʴ�Ϊ��KSCN��Һ��
���������
�����Ѷȣ�һ��
5������� ��16�֣�A��D��E��X��Y��ԭ��������������Ķ���������Ԫ�ء�����Xԭ���������������ڲ����������3����X��Yͬ�壻A��X��Y�Ȳ�ͬ��Ҳ��ͬ���ڣ�DԪ�ص�ij��ͬλ��ԭ���ڿ��ŷ�������ҪӦ�á�
��1��Y�����ӽṹʾ��ͼΪ?��
��2���ơ�A��X����Ԫ����ɵĻ�����������Ļ�ѧ��������??��
��3������A��E����Ԫ����ɣ������к���18�����ӣ�ֻ���ڹ��۵����������¼���һ����ɫҺ�塣
�ټ���һ�ֶ�Ԫ��� д����һ�����뷽��ʽ��?��
д����һ�����뷽��ʽ��?��
�ڼ��ڼ�����Һ���ܹ���CuO��ԭΪCu2O�� ��֪ÿ1mol�ײμӷ�Ӧ�� 4 mol����ת�ƣ��÷�Ӧ�Ļ�ѧ����ʽΪ��?��
��֪ÿ1mol�ײμӷ�Ӧ�� 4 mol����ת�ƣ��÷�Ӧ�Ļ�ѧ����ʽΪ��?��
��4��������DX��YX2�̵�����Ⱦ��һ�ַ��������ڴ���������ʹ���߷�Ӧ������֮һΪ����Y����֪��Ӧ����1 g Y���嵥��ʱ�ų�8.4 kJ�������˷�Ӧ���Ȼ�ѧ����ʽΪ?��
��5����0.050 mol YX2(g)��0.030 mol X2(g)�����ݻ�Ϊ1 L���ܱ������У���Ӧ�� X2(g) +2YX 2(g) 2YX3(g)��һ�������´ﵽƽ�⡣
2YX3(g)��һ�������´ﵽƽ�⡣
���������������䣬������ϵ��ѹǿ��ƽ�ⳣ��K?�����������С�����䡱����
��ƽ��ʱ���c(X2)=0.010 mol��L��1���������·�Ӧ��ƽ�ⳣ��K=?��YX2��ƽ��ת����Ϊ?��
�ο��𰸣���16�֣�
��1��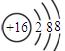 ��1�֣�
��1�֣�
��2�����Ӽ������ۼ���2�֣�
��3����N2H4 +H2O N2H5++ OH�� ��2�֣�
N2H5++ OH�� ��2�֣�
��N2H4 +4CuO��N2��+2Cu2O+2H2O?��3�֣�
��4��2CO(g)+SO2(g)=2CO2(g)+S(s)?��H="�C268.8" kJ��mol��1 ��3�֣�
��5���ٲ��䣨1�֣�
��1.6��103 ?80%��0.8����2�֣���4�֣�
�����������
�����Ѷȣ���