1、简答题 “北、京、欢、迎、您”分别代表五种不同颜色的单质,它们之间相互交叉形成了如图所示的奥运五环旗,A、B、C、D、E、F、G、H是由相交叉的两环元素组成的化合物.
已知:蓝色的“北”是液态O2,红色的“欢”是固态非金属单质,1mol?G可与1mol“您”恰好反应生成1mol?H,F的溶液可与A反应生成酸M、酸N和E的溶液,C高温煅烧可制得A,此反应是工业上制取酸M的基础反应.请回答下列问题:
(1)“京”是______,“欢”的同素异形体是______.
(2)写出F的溶液与A反应生成酸M、酸N和E的溶液的化学方程式:______,该反应为氧化还原反应,还原产物为______.
(3)工业上以C为基础原料,制取酸M产生的工业尾气直接排放到大气中会造成环境污染,处理该尾气中以得到一种化肥,写出该肥料的化学式:______.
(4)已知:P(s)+
Cl2(g)=PCl3(g);△H=-287.7kJ/mol,P(s)+Cl2(g)=PCl5(g);△H=-498.7kJ/mol.则PCl5(g)分解生成PCl3(g)和Cl2(g)反应的热化学方程式为:______.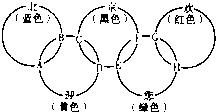
2、推断题 如图所涉及的物质均为中学化学中的常见物质,其中C、D、E为单质,E为固体,F为有磁性的化合物。它们之间存在如下关系(反应中生成的水及次要产物均巳略去)
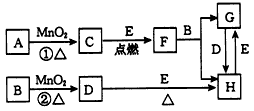
(1)写出下列物质的化学式B_________,E___________。
(2)指出MnO2在相关反应中的作用:反应①中是_______剂,反应②中是________剂。
(3)若反应①是在加热条件下进行,则A是_________(填化学式);若反应①是在常温条件下进行,则A是_________(填化学式);如在上述两种条件下得到等质量的C单质,反应中转移的电子数之比为____________。
3、填空题 中学常见化学反应方程式为:A+B→X+Y+H2O(未配平,反应条件略去),其中,A、B的物质的量之比为1:4。请回答:
(1)若Y为黄绿色气体,该反应的离子方程式为??,B体现出的化学性质有??
(2)若A为常见的非金属单质,B的溶液为某浓酸,反应条件为加热,其反应的化学方程式为?
(3)若A为某不活泼的金属单质,实验室常用该反应来制备某种能形成酸雨的气体,该反应中氧化剂与还原剂的物质 的量之比为?
(4)若A为常见的金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中。
①A元素在元素周期表中的位置是?
②含amolX的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X的物质的量是?
4、简答题 明明同学欲探究一块棕黑色块状固体的主要成分(仅由两种元素组成).将该固体溶于稀盐酸后,有气体A放出,并得到浅绿色溶液B.A在空气中充分燃烧,又得到无色有刺激性气味的气体C,该气体能使品红溶液褪色.向B溶液中加入过量的氢氧化钠溶液,可先得到白色沉淀,然后沉淀迅速变为灰绿色,最后变为红褐色.
根据上述实验现象回答:
(1)该棕黑色块状固体的主要成分是(写化学式)______.
(2)请另外写出两个有气体C生成的氧化还原反应方程式:
①______.
②______.
(3)请写出白色沉淀变成红褐色沉淀的化学方程式:______.
(4)将红褐色沉淀溶于稀盐酸后,欲检验溶液中的金属阳离子,可选用的试剂是______.
5、填空题 (16分)A、D、E、X、Y是原子序数依次增大的短周期主族元素。其中X原子最外层电子数是内层电子总数的3倍;X、Y同族;A与X、Y既不同族也不同周期;D元素的某种同位素原子在考古方面有重要应用。
(1)Y的离子结构示意图为?。
(2)钠、A和X三种元素组成的化合物,其所含的化学键类型有??。
(3)甲由A、E两种元素组成,分子中含有18个电子,只存在共价单键。常温下甲是一种无色液体。
①甲是一种二元弱碱, 写出其一级电离方程式:?。
写出其一级电离方程式:?。
②甲在碱性溶液中能够将CuO还原为Cu2O, 已知每1mol甲参加反应有 4 mol电子转移,该反应的化学方程式为:?。
已知每1mol甲参加反应有 4 mol电子转移,该反应的化学方程式为:?。
(4)处理含DX、YX2烟道气污染的一种方法,是在催化剂作用下使两者反应,产物之一为单质Y。已知反应生成1 g Y固体单质时放出8.4 kJ热量,此反应的热化学方程式为?。
(5)将0.050 mol YX2(g)和0.030 mol X2(g)放入容积为1 L的密闭容器中,反应: X2(g) +2YX 2(g) 2YX3(g)在一定条件下达到平衡。
2YX3(g)在一定条件下达到平衡。
①若其他条件不变,增大体系的压强,平衡常数K?(填“增大”、“减小”或“不变”)。
②平衡时测得c(X2)=0.010 mol・Lˉ1。该条件下反应的平衡常数K=?,YX2的平衡转化率为?。