1、选择题 下列装置能达到实验目的是
A..验证Cu与稀硫酸在通电下能反应
B.在钥匙上镀铜
C..构成原电池
D..用于测定中和热
参考答案:AD
本题解析:分析:A.Cu作阳极,可被氧化;
B.在钥匙上镀铜,铜应作阳极;
C.没有形成闭合回路;
D.装置在保温桶中进行,可起到防止热量散失的作用.
解答:A.验证Cu与稀硫酸在通电下能反应,Cu作阳极,可被氧化,阴极发生还原反应生成氢气,故A正确;
B.在钥匙上镀铜,阳极发生氧化反应,铜应作阳极,故B错误;
C.没有形成闭合回路,不能形成原电池,故C错误;
D.装置在保温桶中进行,可起到防止热量散失的作用,可用于测定中和热,故D正确.
故选AD.
点评:本题考查较为综合,涉及原电池、电解及其应用以及中和热的测定,侧重于化学实验方案的评价,题目难度不大,注意把握电解质和原电池的工作原理.
本题难度:简单
2、选择题 t℃时,甲、乙两个烧杯中各盛有100g(密度为1.10g?cm-3)相同浓度的KCl溶液.现将甲烧杯中的溶液蒸发掉35.0gH2O,恢复到t℃时,析出KCl固体5.0g;乙烧杯中的溶液蒸发掉45.0gH2O,恢复到t℃时,析出KCl固体10.0g.下列说法正确的是
A.原溶液的质量分数为20%
B.t℃时,KCl的溶解度为50.0g
C.原溶液的物质的量浓度为3.0mol?L-1
D.乙烧杯中剩余KCl溶液的质量分数大于甲烧杯中剩余KCl溶液的质量分数
参考答案:B
本题解析:分析:甲乙两烧杯中的溶液由不饱和转变成饱和溶液溶剂相差10.0g,溶质相差5.0g,5.0g溶质溶解在10g溶剂中所形成的溶液为饱和溶液.由此可知该温度下的溶解度为50.0g.根据溶解度可求出原溶液的溶质为25.0g,所以原溶液的质量分数为25%,代入可知浓度为c=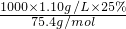 =3.7mol?L-1,两烧杯中剩余溶液均为饱和溶液,质量分数相等.
=3.7mol?L-1,两烧杯中剩余溶液均为饱和溶液,质量分数相等.
解答:A.设原100gKCl溶液中含溶质KCl的质量为xg,根据饱和溶液中的溶解度计算公式得下列关系式:
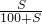 =
=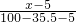 =
= ,解得x=25 g,所以原KCl溶液的质量分数为
,解得x=25 g,所以原KCl溶液的质量分数为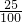 ×100%=25%,故A错误;
×100%=25%,故A错误;
B.据题意得,蒸发35.0g水析出KCl固体5.0g,蒸发45.0g水析出KCl固体10.0g,推断出蒸发10.0g水析出KCl固体5.0 g,故100g水中溶有50g KCl固体得到饱和溶液,即KCl的溶解度为50g,故B正确;
C.原溶液的质量分数为25%,代入可知浓度为c=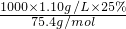 =3.7mol?L-1,故C错误;
=3.7mol?L-1,故C错误;
D.甲、乙烧杯中蒸发水后均有KCl固体析出,说明均已达到饱和,此时质量分数相伺,故D错误.
故选B.
点评:本题考查溶解度的有关问题,考查学生的思维能力,题目难度中等,注意根据根据溶液和溶质质量变化计算溶液的质量分数和溶解度为解答该题的关键.
本题难度:困难
3、选择题 用NA表示阿伏加德罗常数的值.下列叙述中不正确的是
A.1L?0.5?mol?L-1的MgCl2溶液,含有Cl-数为?NA
B.标准状况下,11.2?L?CCl4中含有的分子数目为0.5NA
C.常温常压下,18?g?H2O中含有的原子总数为3NA
D.质量为32g的O3和O2的混合物中含有的氧原子数为2NA
参考答案:B
本题解析:分析:A.根据N(Cl-)=2n(MgCl2)VNA计算;
B.四氯化碳是液体;
C.1molH2O中含有的原子为3mol;
D.利用n=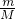 及O2和O3混合气体中分子都是只由氧原子构成来分析氧原子数.
及O2和O3混合气体中分子都是只由氧原子构成来分析氧原子数.
解答:A.N(Cl-)=2n(MgCl2) NA=2C(MgCl2)VNA=2×0.5mol?L-1×1L×NA=NA,故A正确;
B.四氯化碳是液体,标准状况下,11.2?L?CCl4的物质的量不是0.5mol,故B错误;
C.18?g?H2O的物质的量是1mol,含有的原子总数为3NA,故C正确;
D.因混合气体中分子都是只由氧原子构成,则氧原子的物质的量为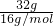 =2mol,氧原子数为2mol×NA=2NA,故D正确.
=2mol,氧原子数为2mol×NA=2NA,故D正确.
故选B.
点评:本题考查阿伏加德罗定律及其推论,题目难度中等,本题注意阿伏加德罗定律只适用于气体,另外在标准状况下,Vm=22.4L/mol,其它条件下也有可能为22.4L/moL.
本题难度:一般
4、实验题 (6分)⑴写出下图石油的蒸馏装置中所指仪器的名称:

a._________?___? b._________?
⑵指出右图石油的蒸馏装置中的错误之处:
①缺铁圈和?
②缺?(防液体暴沸)
③?
④?
参考答案:(1)蒸馏烧瓶?冷凝管?(每空1分)(2)①石棉网(1分)?②碎瓷片(1分)?③温度计的水银球上端没有与支管口相平;(1分)④冷凝水的方没有下进上出。(1分)
本题解析:略
本题难度:简单
5、选择题 下列有关实验原理、装置、操作或结论的描述中,不正确的是(夹持仪器略去未画)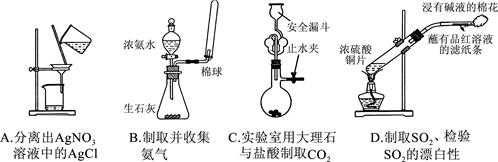
参考答案:B
本题解析:B.氨气密度比空气小,采用向下排空气法来收集,导管口此时应向上深入试管。
本题难度:简单