1������� ��14�֣�������ͼ��ʾװ�ÿ������һϵ��ʵ�飨ͼ�мг�װ������ȥ��
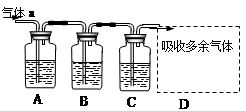
��ش��������⣺
��.������a��Cl2��װ��A��B��C�е��Լ�����Ϊ�� FeCl2��Һ������KI��Һ��ʯ����Һ��
װ��
| A
| B
| C
| D
|
�Լ�
| FeCl2��Һ
| ����KI��Һ
| ʯ����Һ
| ?
?
|
����
| ��Һ��dz��ɫ��Ϊ�ػ�ɫ
| ?
?
| ?
?
| ?
|
���ӷ���ʽ
| ?
?
| ?
?
| ?
| ?
?
|
II��������a��SO2��װ��A��B��C�е��Լ�����Ϊ��Ʒ����Һ�����Ը��������Һ�������ᣨ�����ˮ��Һ����
װ��
| A
| B
| C
|
�Լ�
| Ʒ����Һ
| ���Ը��������Һ
| �����ˮ��Һ
|
����
| ?
| ��ɫ��ȥ
| ?
|
����SO2������
| ?
| ?
| ������
|
��1��д��C�з�����Ӧ�Ļ�ѧ����ʽ?��
��2��Dװ����������������Һ������SO2��Ϊ�˷�ֹ������Ӧ��ѡ������װ���е�?������ţ���
�ο��𰸣���14�֣�
װ��
A
B
C
D
�Լ�
?
?
?
NaOH��Һ
����
?
��Һ����
�ȱ�����ɫ
?
���ӷ���ʽ
Cl2+ 2Fe2+ = 2Fe3+ +2Cl-
Cl2+2I��=I2 +2Cl-??
?
Cl2+2OH��= Cl�� +ClO��+2H2O
?
װ��
A
B
C
�Լ�
?
?
?
����
?��ɫ��ȥ?
?
��������ɫ����?
����SO2������
?Ư����?
?��ԭ��?
?
�����ϱ���ÿ��1�֣�
��1��SO2 + 2H2S ="=3S��+" 2H2O��2�֣�
��2���٢ۣ�2�֣�
���������������a��Cl2��װ��A��B��C�е��Լ�����Ϊ�� FeCl2��Һ������KI��Һ��ʯ����Һ���������Ȼ�������Ӧ�����Ȼ������͵⻯�ط�Ӧ���ɵⵥ�ʣ���ʹʯ���ȱ�����ɫ��β��Ҫ���������������ա�������a��SO2��װ��A��B��C�е��Լ�����Ϊ��Ʒ����Һ�����Ը��������Һ�������ᣨ�����ˮ��Һ����Ʒ�����ɫ�����Ը������Ҳ����ɫ������������ɻ�ɫ������
�����������Ͷ����������������Ҫ�ر�ע����ǣ���������ˮ�����ɵĴ��������ǿ�����ԣ���ʹ��ɫ������ɫ���ٻָ������������ǻ����Ե�Ư����ʹ������ɫ���ָܻ���
�����Ѷȣ�һ��
2��ʵ���� ?ૼ״���ૼ������л��ϳ��еij����Լ�������ૼ�ȩ�Ʊ�����ʵ��ԭ��Ϊ��
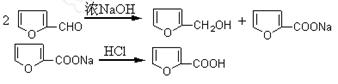
�Ʊ��������£�����50mL�ձ��з���3.28mL(0.04mol)ૼ�ȩ�����ñ�ˮ��ȴ����ȡ1.6gNaOH��������ˮ�У��ڽ����µμ���������ˮ��Һ��ૼ�ȩ�С�����8��12������������40min������Ӧ������������ˮʹ��ǡ����ȫ�ܽ⣬��������ȡ��Һ����������ȡ������ˮ����þ���������ˮԡ����ȥ���ѣ�Ȼ�������ռ�169��172����ֵ�1.4g��Ʒ������������ȡ���ˮ��Һ�������μ�Ũ���ᵽpH=3�����裬��ȴ���ᾧ�����ˡ�������������ˮϴ�ӣ���ɺ��ռ��ֲ�����ᴿ��þ���Ʒ1.5g��
��1����ʵ���У��������Ʊ�������������ˮ������ˮ��������Ҫ��Ӱ��__________���ʡ�
��2����ʵ����Ҫ�����������40min����Ŀ����______________________________��
��3����ȡʱ���õ�����Ҫ�������ʵ�������__________�����˵��ŵ���______________________________________________________________________��
��4��ૼ���ֲ�Ʒ�ᴿ�ķ�����________________________________________��
��5����ʵ����ૼ���IJ���Ϊ________________________________________ ��
�ο��𰸣���1��ૼ���
��2�������������н��еķ�Ӧ����ʱ���ֽ���ʹ���ֽӴ�����֤��Ӧ��ȫ��
��3����Һ©�������˺�ϴ���ٶȼӿ죬ĸҺ�;���������ȫ���Ҳ�Ʒ���
��4���ؽᾧ?��5��67%��ÿ�վ�2�֣�
���������
��1��ૼ���
��2�������������н��еķ�Ӧ����ʱ���ֽ���ʹ���ֽӴ�����֤��Ӧ��ȫ��
��3����Һ©�������˺�ϴ���ٶȼӿ죬ĸҺ�;���������ȫ���Ҳ�Ʒ���
��4���ؽᾧ?
��5��������Ӧ�õ�0.02molૼ���,���ԣ�ૼ���IJ���Ϊ��1.5g/��0.02mol��112g/mol����100%=67%
�����Ѷȣ�һ��
3��ѡ���� ����������ռ�������ȷ���ǣ�������
A��Cl2����������ˮ���ռ�Ҳ�����ſ������ռ���
B��NO2����������ˮ���ռ�Ҳ�����ſ������ռ���
C��NO����������ˮ���ռ�Ҳ�����ſ������ռ���
D��O2����������ˮ���ռ�Ҳ�����ſ������ռ���
�ο��𰸣�A��Cl2�Ϳ�������Ӧ���ܶȱȿ������Բ����ſ������ռ���������������ˮ����������ˮ���ռ�����A����
B��NO2�Ϳ����в���Ӧ���ܶȱȿ������Բ����ſ������ռ�����NO2����ˮ��Ӧ����������ˮ���ռ�����B����
C��NO�Ϳ����е�������Ӧ�����ܶȱȿ��������ܲ����ſ������ռ�����NO������ˮ��������ˮ���ռ�����C����
D��O2�Ϳ�������Ӧ���ܶȱȿ������Բ����ſ������ռ���O2������ˮ����������ˮ���ռ�����D��ȷ��
��ѡ��D��
���������
�����Ѷȣ���
4������� �������ƣ�NaClO2����һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ�����ڼ��Ի������ȶ����ڡ�ijͬѧ�������Ϻ��������NaClO2����Ҫ�������¡�
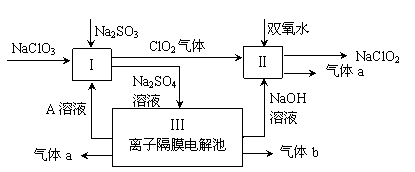
��1��˫��ˮ�ĽṹʽΪ��?�����з�����Ӧ�Ļ�ԭ�����������������ѧʽ����
��2�����з�Ӧ�����ӷ���ʽ������������?������ ��
��3��A�Ļ�ѧʽ���������������� ��װ�â���A���������������� ����������
��4��ClO2��һ�ָ�Чˮ�������������������ƺ�ϡ����Ϊԭ���Ʊ���
��д���÷�Ӧ�Ļ�ѧ����ʽ����������������
���о�����������Ӧ��ʼʱ����Ũ�Ƚϴ��������������Cl2�������ӷ���ʽ���Ͳ���Cl2��ԭ��������������?����
��5��NaClO2���ʿɷֽ�ΪNaClO3��NaCl��ȡ����������ǰ���NaClO2�����������Һ���ֱ�������FeSO4��Һ��Ӧʱ������Fe2+�����ʵ���������?(����ͬ������ͬ�����ж�)
�ο��𰸣���14�֣���1��H-O-0-H? Na2SO3������2�֣�����
��2��2ClO2 + H2O2 + 2OH��= 2ClO2��+ O2��+ 2H2O��2�֣�
��3��H2SO4����������2�֣�
��4��5NaClO2 + 4HCl =" 5NaCl" + 4ClO2��+ 2H2O������2�֣���
ClO2��+ 3Cl��+ 4H+ = 2Cl2+ 2H2O��2�֣�
��5����ͬ��2�֣�
�����������H2O2��������ԭ�Ӽ��γ�һ�����õ��Ӷԣ��ṹʽΪ��H�DO�DO�DH����ӦI��2ClO3�D��SO32�D��2H��=2ClO2��SO42�D��H2O������SO32�D��S��+4�۱��+6�ۣ�����ԭ�������Ϊ��H�DO�DO�DH��Na2SO3�����ƴ�ͼ�ж�����Ӧ��ΪClO2��H2O2,��������������ΪNaClO2��ClO2����������H2O2�����ɨD1�۱�ɨD2��2ClO2 + H2O2 + 2OH��= 2ClO2��+ O2��+ 2H2O���ʴ𰸣�2ClO2 + H2O2 + 2OH��= 2ClO2��+ O2��+ 2H2O���Ǣ�������2H2O�D4e�D=4H�� ��O2��,aΪO2,������4H2O��4e�D=4OH�D?��2H2��,?bΪH2�� A�Ļ�ѧʽ��H2SO4, װ�â���A���������������𰸣�H2SO4��������Cl�DŨ�ȴ�ʱ����ԭ����ǿ�������ɵ�ClO2������5NaClO2 + 4HCl =" 5NaCl" + 4ClO2��+ 2H2O��ClO2��+ 3Cl��+ 4H+ = 2Cl2+ 2H2O����Ϊ��5NaClO2 + 4HCl =" 5NaCl" + 4ClO2��+ 2H2O��ClO2��+ 3Cl��+ 4H+ = 2Cl2+ 2H2O����ClO2�D��ClO3�D��Fe2�� ��Ӧ���ն����Cl�D������ǰ��ת�Ƶĵ�������ͬ����������Fe2+�����ʵ�����ͬ���𰸣���ͬ��
�����Ѷȣ���
5��ʵ���� �����������һ����Ҫ�Ĺ�ҵԭ�ϣ��л���ѧ��ͨ��������Ӧ��ˮ�ⷴӦ��ԭ�������Խ��б���������ĺϳɺ�������Ӧ���й����ʵ��������ʼ��±���ʾ��
?
| ������
| �״�
| ���������
|
�۵�/��
| 122.4
| -97
| -12.3
|
�е�/��
| 249
| 64.3
| 199.6
|
�ܶ�/g.cm-3
| 1.2659
| 0.792
| 1.0888
|
ˮ����
| ��
| ����
| ����
|
����������ĺϳɺ��ᴿ
��ص�ʵ�鲽��Ϊ:
��һ�����������ļ״��ͱ������ϼ��ȷ���������Ӧ
�ڶ�����ˮϴ�ᴿ
�������������ᴿ
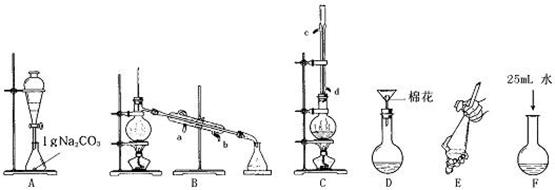
��1�������Ǻϳɺ��ᴿ���й�װ��ͼ����д���ϳɺ��ᴿ����������IJ���˳������ĸ��?��
��2��Cװ���г���װ��15g�������20mL�����ļ״����Ҫ?��? ___ ��
��3��Cװ���������ܵ�������?��Aװ���й���Na2CO3������?��
�����������������Ӧ
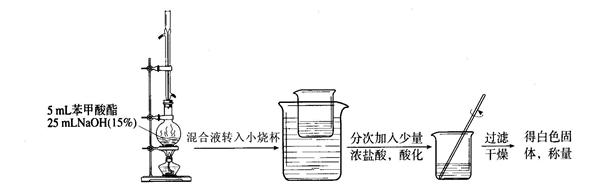 ? G? H? I
? G? H? I
��4����˵��Gװ���з�Ӧ��ȫ��������?��
��5���ڢ��еõ���ɫ���������Ϊ5g�����跴ӦI�ͷ�Ӧ���У������ᴿ��Ч��Ϊ66.7%,��Ũ���ᱽ���������ɰ�ɫ�����ת����Ϊ80%��������Ӧ�б������ת����ΪX�����������ת��Ч��Ϊ100%����X==?��
�ο��𰸣���1��CFEADB��3�֣�?��2��Ũ���ᣬ?��ʯ�������Ƭ����
��3������������ϴȥ����������й�������?��4�����ֲ�?��5��62.5%
�����������
�����Ѷȣ�һ��