1、实验题 (16分)(1)小明在做“研究温度对反应速率的影响”实验时,他取了两只试管,均加入4mL 0.01mol/L的KMnO4酸性溶液和2mL 0.1mol/L H2C2O4(乙二酸)溶液,振荡,A试管置于热水中,B试管置于凉水中,记录溶液褪色所需的时间。
①需要用 来酸化KMnO4溶液,褪色所需时间tA tB(填“>”、“=”或“<”)。
②写出该反应的离子方程式 。
(2)实验室有瓶混有泥沙的乙二酸样品,小明利用这个反应的原理来测定其含量,操作为:
①配制250 mL溶液:准确称量5.0g乙二酸样品,配成250mL溶液。
②滴定:准确量取25.00mL所配溶液于锥形瓶中,加少量酸酸化,将0.1000 mol・L-1 KMnO4溶液装入 (填“酸式”或“碱式”)滴定管,进行滴定操作。在实验中发现,刚滴下少量KMnO4溶液时,溶液迅速变成紫红色。将锥形瓶摇动一时间后,紫红色慢慢消失;再继续滴加时,紫红色就很快褪色了。请解释原因: 。当____ ,证明达到滴定终点。
③计算:再重复上述操作2次,记录实验数据如下。
序号
| 滴定前读数(mL)
| 滴定后读数(mL)
|
1
| 0.00
| 20.10
|
2
| 1.00
| 20.90
|
3
| 0.00
| 22.10
|
则消耗KMnO4溶液的平均体积为 mL,已知H2C2O4的相对分子质量为90,则此样品的纯度为 。
④误差分析:下列操作会导致测定结果偏高的是__________。
A 未用标准浓度的酸性KMnO4溶液润洗滴定管
B 滴定前锥形瓶有少量水
C 滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D不小心将少量酸性KMnO4溶液滴在锥形瓶外
E.观察读数时,滴定前仰视,滴定后俯视
2、选择题 下列说法错误的是
A.在C(s) +H2O(g) 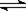 CO(g) + H2(g)反应体系中,增加碳的量不能迅速提高正反应速率
CO(g) + H2(g)反应体系中,增加碳的量不能迅速提高正反应速率
B.钾的金属性比钠强,所以钾与水的反应比钠的反应剧烈
C.在压强相同条件下,结构相似的CH4、SiH4、GeH4的沸点依次升高,所以结构相似的HF、HCl、HBr、HI的沸点也依次升高
D.面粉厂严禁烟火的原因是面粉粉尘表面积大,与空气接触遇明火极易发生爆炸
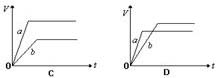
3、选择题 将等质量的a、b两份锌粉装入试管中,分别加入过量的稀硫酸,同时向装a的试管中加入少量CuSO4溶液。右图表示产生氢气的体积V与时间t的关系,其中正确的是(?)
4、填空题 向2.0L恒容密闭容器中充人1.0mol PCl5,在温度为T时发生如下反应
PCl5(g)  PCl3(g)+C12(g)?
PCl3(g)+C12(g)?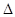 H=124kJ・mol-1。反应过程中测定的部分数据见下表:
H=124kJ・mol-1。反应过程中测定的部分数据见下表:
时间t/s
| 0
| 50
| 150
| 250
| 350
|
n(PCL3)/mol
| 0
| 0.16
| 0.19
| 0.2
| 0.2
|
?
回答下列问题
(1)反应在前50 s的平均速率v(PCI5)=________。
(2)温度为T时,该反应的化学平衡常数=________。
(3)要提高上述反应的转化率,可采取的措施有________。
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a=________。
(5)在热水中,五氯化磷完全水解,生成磷酸(H3 PO4),该反应的化学方程式是________。
若将0.01 mol PCI5投入l L热水中,再逐滴加入AgNO3溶液,先产生的沉淀是________ [已知Ksp(Ag3 PO4)="1.4" x 1 0-16,Ksp(AgCl)="1.8" x 10-10]。
(6)一定条件下,白磷溶于硝酸溶液产生一种氮氧化合物气体,该气体与白磷的物质的量之比为20:3,反应的化学方程式为____________________________。
5、选择题 下列措施能减慢化学反应速率的是( )
A.烧煤时将煤块粉碎
B.将食物贮藏在冰箱中
C.用过氧化氢溶液制氧气时添加少量二氧化锰粉末
D.用相同质量的锌粉替代锌粒与同浓度同体积的盐酸反应制氢气