1、选择题 对于原子序数为?116?号的元素X,下列叙述正确的是( )
A.X是非金属元素
B.X的最高价氧化物的化学式为:XO3
C.X的钠盐的化学式为:Na2X
D.X的最高价氧化物的水化物为强酸
参考答案:B
本题解析:
本题难度:简单
2、选择题 X、Y是第2或第3周期中的两种元素,它们可形成离子化合物XmYn,且离子均有稀有气体原子的电子结构.若X的原子序数为a,则Y的原子序数不可能为( )
A.a+8-m-n
B.a-8+m-n
C.a+16-m-n
D.a-m-n
参考答案:X、Y是第2或第3周期中的两种元素,它们可形成离子化合物XmYn,则X为金属元素,离子为Xn+,Y为非金属元素,离子为Ym-,离子均有稀有气体原子的电子结构,
①若离子的核外电子数目相同,设Y的原子序数为x,则a-n=x+m,即x=a-n-m;
②若金属离子在同周期,离子的核外电子数目相差8,则a-n+8=x+m,即x=a+8-m-n;
③若金属离子在第2周期,阴离子在第3周期,离子的核外电子数目相差16,即x=a+16-m-n;
显然不可能为a-8+m-n,
故选B.
本题解析:
本题难度:简单
3、简答题 (附加题)A、B、C、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子化合物;B与Z的最外层电子数之比为2:3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红.
请回答下列问题:
(1)Z的原子结构示意图为______;元素C在周期表中的位
置是______,A与B所形成的化合物BA4的电子式为______;
(2)化合物Y2X2属于离子化合物,含有的化学键是______,该化合物中阳离子与阴离子的个数比为______;
(3)化合物A2X和A2Z中,沸点较高的是______(填化学式);
(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物反应可以生成Z单质和一种10电子化合物,反应的化学方程式为______
______;
(5)用电子式表示化合物Y2X的形成过程______
______;
(6)已知X2和ZX2合成ZX3的化学方程式为:2ZX2(g)+X2(g)

2ZX3(g),在一定温度下的定容容器中,下列事实不能说明该反应已经达到平衡的标志的是______;
A.ZX3的生成速率与ZX3的分解速率相等
B.单位时间内生成1mol?X2,同时生成2mol?ZX2
C.容器内ZX2、X2、ZX3的浓度之比为2:1:2
D.容器中各组分的含量不在随时间变化而变化
E.容器中气体的压强不在随时间变化而变化
(7)写出元素C的最高价氧化物对应水化物与元素C的气态氢化物反应的化学方程式______.
参考答案:A、B、C、X、Y和Z是原子序数依次递增的短周期元素,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红,Y2X2为Na2O2,则X为O元素,则Y为Na元素;A与X可形成10个电子化合物,A与Y同主族,则A为H元素;X与Z同主族,则Z为S元素;B与Z的最外层电子数之比为2:3,则B元素的最外层电子数为4,A与B可形成10个电子化合物,B为C元素,原子序数C介于碳元素与氧元素之间,则C为氮元素.
故A应为H元素,B为C元素,C为氮元素,X为O元素,Y为Na元素,Z为S元素.
(1)Z为S元素,核电核数为16,原子核外有3个电子层,最外层电子数为6,则原子结构示意图为
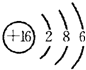
;C为氮元素,原子核外有2个电子层,最外层电子数为5,处于周期表第二周期ⅤA族;
化合物BA4为CH4,为共价化合物,电子式为
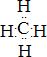
.
故答案为:

;第二周期ⅤA;
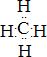
;
(2)Y2X2为Na2O2,为离子化合物,钠离子与过氧根离子之间形成离子键,过氧根离子中氧原子之间为非极性共价键.钠离子与过氧根离子之比为2:1.
故答案为:离子键和非极性键;?2:1.
(3)O原子半径较小,非金属性较强,H2O存在氢键,沸点在同主族元素中形成的氢化物最高.
故答案为:H2O.
(4)A与X和A与Z形成的18电子化合物分别为H2O2、H2S,其中H2O2具有氧化性,H2S具有还原性,二者发生氧化还原反应生成S和H2O,反应的化学方程式为H2O2+H2S=S↓+2H2O.
故答案为:H2O2+H2S=S↓+2H2O.
(5)Y2X为Na2O,电子式表示形成过程为
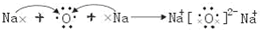
.
故答案为:
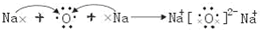
.
(6)A.ZX3的生成速率与ZX3的分解速率相等,说明反应到达平衡,故A正确;
B.单位时间内生成1mol?X2同时生成2molZX2,表示同一方向速率,自始至终都是按此比例进行,不能说明到达平衡,故B错误;
C.平衡时容器内ZX2、X2、ZX3的浓度之比可能为2:1:2,可能不是,与开始浓度与转化率有关,故C错误;
D.随反应进行各组分的含量发生变化,容器中各组分的含量不在随时间变化而变化,说明到达平衡,故D正确;
E.随反应进行,容器内压强降低,容器中气体的压强不在随时间变化而变化,说明到达平衡,故E正确.
故选:BC.
(7)元素C的最高价氧化物对应水化物是HNO3,元素C的气态氢化物是NH3,反应的化学方程式为HNO3+NH3=NH4NO3.
故答案为:HNO3+NH3=NH4NO3.
本题解析:
本题难度:一般
4、填空题 有位于20号元素前,原子序数依次递增的A、B、C、D、E五种元素.A、C元素的电子层数相同;A、E两元素的最外层和次外层电子数相同;A和C可形成化合物AC,D和E可形成ED2;B元素的原子最外层即M层有3个电子.
(1)试写出这五种元素的名称和符号:A______、B______、C______、D______、E______;
(2)写出下列反应的化学方程式①A+C→AC______.②D+E→ED2______.
参考答案:由A,C两元素原子的电子层数相同,所以A,C同周期,又A,B,C,D,E五种元素原子序数依次递增,所以B与A,C是同周期的.由“A,E两元素原子的最外层和次外层电子数分别相同”,可知A在第三周期,E在第四周期.所以B在第三周期,且B元素原子的最外层只有3个电子,所以B是Al.所以A只能为钠或镁,当A是钠时,因为A,C形成化合物AC,所以此时C为氯,则E为钾,而D只能是氩,但“D,E形成化合物E2D”,所以D不可能是氩,所以A只能是镁,C是硫,E是钙,D是氯.
(1)A、B、C、D、E五种元素的名称和符号分别为:镁 Mg、铝 Al、硫 S、氯 Cl、钙 Ca,故答案为:镁 Mg;铝 Al;硫 S;氯 Cl;钙 Ca;
(2)镁和硫反应的方程式为:Mg+S?△?.?MgS,钙和氯气反应方程式:Ca+Cl2?点燃?.?CaCl2,故答案为:Mg+S?△?.?MgS;?Ca+Cl2?点燃?.?CaCl2.
本题解析:
本题难度:一般
5、简答题 A、B、C、D、E五种元素的原子序数依次增大,且均小于18;A原子的最外层比B原子的最外层少2个电子,A原子的最外层电子数是次外层电子数的两倍;A、B、C三种元素能结合成化合物C2AB3,在1mol?C2AB3中共有52mol电子,D元素的单质0.5mol与酸全部反应时,有9.03×1023个电子转移,在B与D形成的化合物,D的质量分数为52.94%,D原子核内有14个中子,每个E原子与氢原子化合时只生成了一个共价单键.试填写下列空白
(1)这五种元素的名称A______B______C______D______E______
(2)C在B中燃烧生成的化合物中化学键有______键和______键(填离?子、极性、非极性)
(3)A、B、C结合成的化合物的化学式是______.
参考答案:(1)A原子的最外层电子数是次外层电子数的两倍,所以A为C,A原子的最外层比B原子的最外层少2个电子,所以B是O,A、B、C三种元素能结合成化合物C2CO3,在1mol?C2AB3中共有52mol电子,其中C和O占了30个电子,所以C的电子数为11,即为Na,D元素的单质0.5mol与酸全部反应时,有9.03×1023个即1.5mol电子转移,所以D元素的化合价为+3价,即为Al,每个E原子与氢原子化合时只生成了一个共价单键,即为HCl,所以E为Cl,故答案为:碳;氧;钠;铝;氯;
(2)钠在氧气中燃烧生成的是过氧化钠,过氧化钠中含有钠离子和过氧根离子之间的离子键、氧原子和氧原子之间的非极性共价键,故答案为:离子;非极性;
(3)C、O、Na元素组成的化合物是碳酸钠,故答案为:Na2CO3.
本题解析:
本题难度:一般