1、选择题 下列有关物质结构和性质的叙述正确的是:
①具有16个质子、16个中子和18个电子的微粒符号可表示为:32 16S2-;
②羟基电子式为: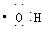 ;
;
③HClO的结构式:H―Cl―O;
④NaHCO3在水中的电离方程式:NaHCO3→Na++H++CO32-;
⑤Na2O的水溶液能导电,这不能说明Na2O是电解质;
⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;
⑦分馏、干馏、裂化都是化学变化
A.①②⑤
B.①④⑥⑦
C.②③④⑥
D.②③⑤⑥⑦
参考答案:A
本题解析:①具有16个质子、16个中子和18个电子的微粒符号可表示为:32 16S2-,正确; ②羟基电子式为: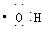 ,正确;③HClO的结构式应为:H―O―Cl; ④NaHCO3在水中的电离方程式应为:NaHCO3→Na++HCO32-,错误; ⑤Na2O的水溶液能导电,这不能说明Na2O是电解质,正确;⑥SiO2既能与氢氟酸反应不能生成盐和水,故SiO2不能是两性氧化物,错误;⑦分馏是物理变化,错误;
,正确;③HClO的结构式应为:H―O―Cl; ④NaHCO3在水中的电离方程式应为:NaHCO3→Na++HCO32-,错误; ⑤Na2O的水溶液能导电,这不能说明Na2O是电解质,正确;⑥SiO2既能与氢氟酸反应不能生成盐和水,故SiO2不能是两性氧化物,错误;⑦分馏是物理变化,错误;
本题难度:一般
2、选择题 下列化学用语表示正确的是
A.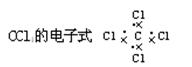
B.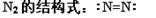
C.镁离子的结构示意图: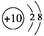
D.甲烷分子的比例模型:
参考答案:D
本题解析:A不正确,因为氯原子还有不参与成键的电子,应该是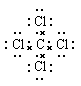 。结构式是用1根短线代替1对电子对,所以氮气的结构式为
。结构式是用1根短线代替1对电子对,所以氮气的结构式为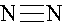 。镁离子的质子数是12,C不正确,所以正确的答案选D。
。镁离子的质子数是12,C不正确,所以正确的答案选D。
本题难度:一般
3、选择题 下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
A.SO2和SiO2
B.CO2和H2
C.NaCl和HCl
D.CCl4和KCl
参考答案:B
本题解析:根据晶体的类型和所含化学键的类型分析,离子晶体含有离子键,可能含有共价键,共价化合物只含共价键,双原子分子或多原子分子含有共价键。A、SiO2是共价键结合的原子晶体,SO2是含有共价键的分子晶体,故A错误;B、CO2和H2都是分子晶体,都只含共价键,故B正确;C、氯化钠是离子晶体含有离子键,氯化氢是分子晶体含有共价键,故C错误;D、四氯化碳是分子晶体,含有共价键,氯化钾是离子晶体,含有离子键,故D错误;故选B。
本题难度:一般
4、选择题 铜与1mol/L的硝酸反应,如果NO3-浓度下降0.2mol/L,则溶液中c(H+)同时下降(溶液体积变化忽略不计)( )
A.0.2mol?L-1
B.0.4mol?L-1
C.0.6mol?L-1
D.0.8mol?L-1
参考答案:铜和稀硝酸反应的离子方程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,设溶液的体积为VL,设溶液中下降的氢离子浓度为C.
则溶液中参加反应的硝酸根离子的物质的量=0.2Vmol,
3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,
? 2mol? 8mol
? 0.2Vmol CVmol
C=8mol×0.2Vmol2mol×VL=0.8mol/L,故选D.
本题解析:
本题难度:一般
5、填空题 (8分)?在氧化还原反应中,氧化剂______电子,发生的反应是_________反应;还原剂________电子,发生的反应是____________反应。铁与氯气反应的方程式为,2Fe+3Cl2====2FeCl3生成物中铁是_______价,铁与盐酸的反应式为________,生成物中铁是________价,事实证明,氯气的氧化性比盐酸的氧化性(填“强”“弱”)____________。
参考答案:(8分)略
本题解析:略
本题难度:简单