1��ѡ���� ��FeI2��FeBr2�Ļ����Һ��ͨ��������������Һ��ijЩ���ӵ����ʵ����仯����ͼ��ʾ���������й�˵���У�����ȷ����
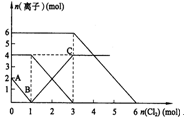
A����ԭ�ԣ�I�� >Fe2+>Br��
B��ԭ�����Һ��FeBr2�����ʵ���Ϊ6mol
C����ͨ��2molCl2ʱ����Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ��
2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-
D��ԭ��Һ�У�n��Fe2+����n��I-����n��Br-��=2��1��3
�ο��𰸣�B
���������
����������ӦΪ��2Fe2��+Br2�T2Fe3��+2Br����2Fe3��+2I���T2Fe2��+I2��
A����Ӧ2Fe2��+Br2=2Fe3��+2Br���У���ԭ��Fe2���Ļ�ԭ��ǿ�ڻ�ԭ����Br�������Ի�ԭ�ԣ�Fe2����Br������Ӧ2Fe3��+2I��=2Fe2��+I2�У���ԭ��I���Ļ�ԭ��ǿ�ڻ�ԭ����Fe2�������Ի�ԭ�ԣ�I����Fe2�������Ի�ԭ��I����Fe2����Br������A��ȷ��
B��ͨ�������������ȱ�������������������ӣ�����������ӣ���ͨ����������Ϊ0��1mol�Ĺ����У������Ӵ����������0�����õ������ӵ����ʵ���Ϊ2mol��ͨ����������Ϊ1��3mol�Ĺ����У��������Ӵ�4mol����0���������������������Ժ����������ӹ�4mol����ͨ����������Ϊ3��6mol�Ĺ����������Ӵ�6mOl����0�����������ӵ����ʵ�����6mol����FeBr2�����ʵ���Ϊ3mol����B����
C����ͨ��2molCl2ʱ��2mol��I����������1mol�����µ�1mol��������2molFe2����Ӧ������Һ�з��������ӷ�Ӧ�ɱ�ʾΪ2Fe2��+2I��+2Cl2=2Fe3��+I2+4Cl������C��ȷ��
D����B��֪�������ӵ����ʵ���Ϊ2mol������������4mol�������ӵ����ʵ�����6mol��n��Fe2������n��I������n��Br����=2��1��3����D��ȷ��
��ѡB��
�����Ѷȣ�һ��
2������� ��嫵ĺ�����һ����ı��⣬�̺���80����Ԫ�أ��ɹ���ȡ���õ���50���֡�
��1�����С��ȼҵ��������ʳ��ˮΪԭ����ȡCl2�����ʣ��йصĻ�ѧ����ʽΪ��?��
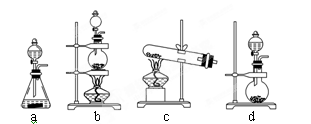
��2��ʵ�����ö���������ȡ�����Ļ�ѧ����ʽΪ��?����������ʵ��ԭ����������װ����ѡ����ʵķ���װ������ʵ������ȡ��������?(��дװ�õ����)��
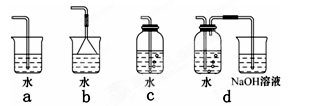
��3��ʵ������ģ��Br����Br2��ת��������ͨ����KBr��Һ�еμ�����������ˮ��ʵ�����ʵ�֡�д��Br����Br2��ת�����ӷ���ʽΪ��?����ˮ���ȶ���Ҫ�������䣬�������������Ʊ���ˮ��װ�����������?��ѡ������ѡ��ı����ĸ����
��4��ʵ�����Ʊ������ķ�Ӧ��������Ũ���½���ֹͣ��Ϊ�ⶨ��Ӧ����Һ�������Ũ�ȣ�̽��С��ͬѧ����������ʵ�飺ȡ100 mL����Һ�����ձ��У����ձ����������������ڵ�����ƽ�ϣ�����ͼ�����ٰ��ѳƺ�50.0 g CaCO3��ĩ�������뵽����Һ�У��ӱ߽���ʹ���ַ�Ӧ���۲�����仯���±���ʾ��
CaCO3����
| δ��CaCO3ʱ
| ��Լ�ķ�֮һʱ
| ��һ��ʱ
| ȫ������ʱ
|
������g
| 318.3
| 325.3
| 334.5
| 359.5
|
����ݴ˷������㣺
��ʵ���в�����CO2��������Ϊ?��
�ڲ���Һ����������ʵ���Ũ��Ϊ (�����ȷ��С�����һλ)?��
�ο��𰸣���1��2NaCl��2H2O 2NaOH��H2����Cl2����2�֣�
2NaOH��H2����Cl2����2�֣�
��2��MnO2��4HCl(Ũ)  MnCl2��2H2O��Cl2����2�֣���b��1�֣�
MnCl2��2H2O��Cl2����2�֣���b��1�֣�
��3��2Br����Cl2��2Cl����Br2��2�֣���d��1�֣� ��4����8.8g��2�֣�����4.0mol/L��3�֣�
�����������1�����ȼҵ������ʳ��ˮΪԭ�ϣ�ͨ����ⷨ��ȡCl2�����ʣ��йصĻ�ѧ����ʽΪ2NaCl��2H2O 2NaOH��H2����Cl2����
2NaOH��H2����Cl2����
��2��ʵ�����ö���������ȡ�����Ļ�ѧ����ʽΪMnO2��4HCl(Ũ)  MnCl2��2H2O��Cl2�������ݷ���ʽ��֪�÷�Ӧ�ǹ�����Һ������Ʊ����壬�����Ҫ����Ҫ�����Ǿƾ��ơ���Һ©������ƿ����ʵ��װ��Ӧ����װ��b������ѡb��
MnCl2��2H2O��Cl2�������ݷ���ʽ��֪�÷�Ӧ�ǹ�����Һ������Ʊ����壬�����Ҫ����Ҫ�����Ǿƾ��ơ���Һ©������ƿ����ʵ��װ��Ӧ����װ��b������ѡb��
��3��������������ǿ�ڵ�����ģ��ܰ��������������ɵ����壬����Br����Br2��ת�����ӷ���ʽΪ2Br����Cl2��2Cl����Br2������������ˮ�����ܽ�Ⱥ�С�����������ж�����Ҫβ������������������������Һ���գ������ȷ�Ĵ�ѡd��
��4���ٸ��������غ㶨�ɿ�֪����Ӧ�в���CO2��������318.3g��50.0g��359.5g��8.8g��
��CO2�����ʵ�����8.8g��44g/mol��0.2mol������ݷ���ʽ��֪
CaCO3��2HCl=CaCl2��H2O��CO2��
2mol? 1mol
0.4mol? 0.2mol
���������Ũ�ȣ�0.4mol��0.1L��4.0mol/L
�����Ѷȣ�һ��
3��ʵ���� ij��ȤС����Ʋ�����������ʵ������ȡ��ˮ��������������ˮ���ʵ�顣
��1��ʵ������������װ���Ʊ���ˮ���밴������������������ķ��������������ӣ�
H��������_____________����ӿڴ��ķ��ţ������ƿ���е��Լ�Ϊ��������������������

��2��д����ʵ������ȡCl2�Ļ�ѧ����ʽΪ��___________________________________
��3��ij��ȤС�����ʵ���ȥ�Ȼ����к���Fe3+��SO42-��Br-���������ӣ��������£�
A���ܽ⣬��������Һ�м����Լ���Fe3+��SO42-������ȫ����У�
B�����ˣ�����Һ�м����������pH��
C������_____����Br-�����������ա���ش����⣺
��3���ٲ���a�У����μ�����Լ���NH3.H2O��_________��_________��
�ڲ���c�м�����Լ���__________________��
��4��ij�о���ѧϰС����KSCN����FeSO4��Һ�е�Fe2+ʱ���������ŨHNO3����Һ����ɫ��졣���ǽ���ɫ��Һ����һ��������Һ�ɺ�ɫͻȻ��Ϊ��ɫ������������ɫ���塣����һ��������ͬѧ�ǽ���������̽����
�۲������ϣݣ�
(SCN)2��Ϊ��±�أ�������±�ص������ƣ�(SCN)2��Cl2��Br2��I2�������ʵ�������ǿ��Ϊ��Cl2��Br2��(SCN)2��I2��
���������ݣ�
�ټ�ͬѧ������FeSO4��HNO3���ã���ͬѧ������______��HNO3���á�
��ʵ����֤�ݣ�
�ڴ�Ҿ������Է�������Ϊ��ͬѧ�ļ��費������������________________________��
�۸�����ͬѧ�ļ��裬���������ʵ�鷽��������֤����ŨHNO3����μ���KSCN��Һ��ʵ�鿪ʼʱ����������һ��ʱ�����Һ�������ɫ����ɫ��ͻȻ���ҷ�Ӧ�����������ݣ��ų�����ɫ���塣������������ͨ�������Ba(OH)2��Һ���������ǣ���ʣ��һ�����壨�ǿ����е���Ҫ�ɷ�֮һ������Ӧ�����Һ�м���BaCl2��Һ������ɫ������
��Ӧ�в����������ǣ�_______________________________
��ʵ����ۣݣ���ͬѧ������ȷ��
��ʵ�鷴˼�ݣ�
����ʵ���֪����SCN-��Ӽ���Fe2+ʱ�����������������HNO3�����ѡ����ˮ�ȣ�ͨ����ʵ��̽����֪������������������Ҫ_______�����������������������
�ο��𰸣���1��H��B��A��C��D��E ��2�֣�����ʳ��ˮ��2�֣�
��2��2NaCl + MnO2 +2 H2SO4 = MnSO4 + Na2SO4 + 2H2O + Cl2�������ȣ� ��2�֣�
��3����BaCl2��1�֣� KOH ��1�֣�
��������������ˮ ��2�֣�
��4����SCN-��1�֣�
��HNO3������û��Fe2+ʣ�� ��1�֣�
��NO2��CO2��N2��3�֣�
��������1�֣�
���������
�������: ��1���Ʊ����������������ӷ���װ�á�����װ�á�����װ�á��ռ���β�����յ�˳�����Ʊ������к���HCl��ˮ�������������壬���������ű���ʳ��ˮ����ȥHCl������Ũ��������ˮ���������������ſ������ռ����ü�����β���������˳������ӦΪH��B��A��C��D��E�����Ը���˳����Ե�֪���ƿ���е��Լ�Ϊ����ʳ��ˮ��
��2������ͼ�еķ���װ�ÿ�֪����ʵ���в������ѻӷ��������Ʊ��ӷ��Ե����ᣬ������������Ʊ������ķ��������Է���ʽΪ2NaCl + MnO2 +2 H2SO4 = MnSO4 + Na2SO4 + 2H2O + Cl2�������ȣ���
��3�����Ȼ����к���Fe3+��SO42-��Br-���������ӣ����м�����Լ���NH3.H2O����ʹFe3+ ������ȥ����ȥSO42- ��Ҫ����Ba2+�Լ���ʹ֮ת��ΪBaSO4������ȥ��Ϊ�˲�����������ʣ�Ӧѡ����������ͬ��BaCl2 ��Ϊ�˰�NH4+��ȥ�����Լ���ǿ��KOH�����Բ���a�����μ�����Լ���NH3.H2O�� BaCl2 ��KOH���ڲ���c�г�ȥ��������Br- �����Լ���������ˮ����Br- ת��Ϊ����Br2��ȥ��
��4���ټ�ͬѧ�Ѿ�������FeSO4��HNO3���� �����Ը����ṩ�����Ͽ��Բ²��ʵ������Ŀ�����SCN-���������õĽ����������ͬѧ������SCN-��HNO3���á�
��������ռ�ͬѧ�ļ��������FeSO4��HNO3����ֻ�ᵼ��Fe2+������ΪFe3+���պ�KSCN����ʹ��Һ��죬�Ҽ����ŨHNO3���������������Һ�Ժ�ɫ���ֱ����ɫ�����Լ�ͬѧ���費������
�۸�����ͬѧ�ļ��裬���ʵ���������ŨHNO3��KSCN��Һ���õĽ�������������е�Ԫ����ɷ�����Ũ�������ɺ���ɫ����NO2��SCN-�в�������ʹBa(OH)2��Һ����������������岻������SO2����ΪSO2���ױ�ǿ����������������ֻ������CO2����S������ΪSO42-�ڷ�Ӧ�����Һ�У����Լ���BaCl2��Һ�ܲ�����ɫ������ʣ��Ŀ�����Ҫ�ɷֵ�������N2�����Բ���������������NO2��CO2��N2 ��
����SCN-��Ӽ���Fe2+ʱ����Ҫ����ǿ��������Fe2+�����Ż������ɫ���ɫ�����Ǹ��������е�ʵ�龭�������ǿ�������������װ���SCN-������ʹ��Һ��ɫ��ʧ�����ɫ�����������ṩ��ʾ������Cl2 ��(SCN)2?��������������ͬ��������SCN- ����ɺ�ɫ��ʧ�����ɫ���������Լ�����������������Ҫ������
�����Ѷȣ�һ��
4��ѡ���� ����ʵ������������������
A��������������ȼ�ղ�����ɫ����
B�����ȵ���˿��������ȼ�գ��������䣬���ɺ�ɫ�������
C�����ȵ�ͭ˿��������ȼ�գ������ػ�ɫ��
D�����ڿ�����ȼ�գ�������ɫ�Ļ��棬���ɵ���ɫ����
�ο��𰸣�B
�������������������ȼ�գ���Ӧ�dz����ң��������ɵIJ��Ǻ�ɫ���壬�Dz��������غ�ɫ���̣�����B������������ȷ��
�����Ѷȣ�һ��
5��ѡ���� ���з���Ӧ����ʱ�����������ɫ�̵��ǣ�������
A������������ȼ��
B��ͭ��������ȼ��
C��������������ȼ��
D������������ȼ��
�ο��𰸣�A������������ȼ�����ɹ����Ȼ��ƣ��۲쵽���̣���A��ѡ��
B��ͭ��������ȼ�����ɹ����Ȼ�ͭ���۲쵽�ػ�ɫ���̣���B��ѡ��
C��������������ȼ����������HCl���ڼ���ƿ�ڹ۲쵽��������C��ѡ��
D������������ȼ�����ɹ����Ȼ������۲쵽����ɫ�̣���Dѡ��
��ѡD��
���������
�����Ѷȣ�һ��