1������� ±�ػ�ѧ�ḻ��ʣ����γ�±���±�ػ������±����ȶ������͵Ļ����
(1)��̬��ԭ�ӵļ����Ų�ʽΪ____��
(2)±�ػ������磺IBr��ICl����±�ص��ʽṹ���ơ��������ơ�Cl2��IBr��ICl�е��ɸߵ��͵�˳��Ϊ
________________��
(3)I3+���ڶ�±�������ӣ�����VSEPRģ���Ʋ�I3+�Ŀռ乹��Ϊ___________��
(4)��̬�������д��ڶ��۷���(HF)2����������_____
(5)��HClO4����HIO4����H5IO6[��д��(HO)5IO]��������ǿ������˳��Ϊ_____________������ţ���
�ο��𰸣�(1)[Ar]3d104s24p5
(2)IBr>ICl>Cl2
(3)V��
(4)HF���Ӽ������
(5)��>��>��
���������
�����Ѷȣ�һ��
2������� ��ͼ��ʾ��һЩ����Ľṹ�����Ƿֱ���NaCl��CsCl���ɱ������ʯ��ʯī�ṹ�е�ijһ�ֵ�ijһ���֣�
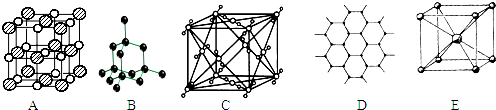
��1�����д������ʯ����______����д�����ĸ��������ÿ��̼ԭ����______��̼ԭ����ӽ��Ҿ�����ȣ�����______���壮
��2�����д���ʯī����______����д�����ĸ��������ÿ����������ռ�е�̼ԭ����ƽ��Ϊ______����
��3�����б�ʾNaCl����______����д�����ĸ����ÿ����������Χ������ӽ��Ҿ�����ȵ���������______����
��4�����б�ʾCsCl����______����д�����ĸ����������______���壬ÿ���������______�������ӽ��ڣ�
�ο��𰸣���1�����ʯ�ǿռ���״�ṹ��ÿ��̼ԭ������4��̼ԭ�ӣ�ԭ�Ӽ��Թ��ۼ����ϣ�����ԭ�Ӿ��壬
�ʴ�Ϊ��B��4��ԭ�ӣ�
��2��ʯī��ƽ���״�ṹ���侧����̼ԭ�ӳ�ƽ�������������У�ÿ����������ռ�е�̼ԭ����ƽ��=1��13��6=2��
�ʴ�Ϊ��D��2��
��3���Ȼ��������Ӿ��壬�乹�������������ӣ�NaCl�����Ǽ�������Ԫ���������Ӽ�ͨ�����Ӽ���ϣ������Ӻ������ӵ���λ������6��ÿ����������Χ������ӽ��Ҿ�����ȵ���������=3��8��12=12��
�ʴ�Ϊ��A��12��
��4���Ȼ�������������ӹ��ɵģ������Ӻ�����ӵ���λ����8����ѡE��
�ʴ�Ϊ��E�����ӣ�8��
���������
�����Ѷȣ�һ��
3������� ��֪X��Y��Z����Ԫ�ص�ԭ������֮�͵���48��X��һ��1:1���⻯������м��ЦҼ����Ц� ����Z�ǽ���Ԫ�أ�Z�ĵ��ʺͻ������й㷺����;����֪Z�ĺ˵����С��28���Ҵ������2 ��δ�ɶԵ��ӡ���ҵ������ZO2��̼�ᱵ������״̬����ȡ������M��M�ɿ���һ�ֺ������Σ���M�������ġ�ѹ�����ܡ���Ӧ���ڳ������ķ���װ�á���X���߷�����M�������С�ظ���λΪ�����壨��ͼ�����߳�Ϊ4.03��10-10m������λ��ΪZ4+��ռ������λ��ΪBa2+��ռ����������λ��ΪO2-��ռ��

(1)Y�����ڱ���λ��________��Z4+�ĺ�������Ų�ʽΪ_______________
(2)X�ĸ����⻯����ӹ���Ϊ____________��X�ڸ��⻯������____��ʽ�ӻ���X��Y�γɵĻ�������۵�Ӧ��____������ڡ����ڡ���X�⻯����۵㡣
(3)���Ʊ�M�Ļ�ѧ��Ӧ����ʽ��____________________��
����M�����У�����Z4+��������������ģ�Ba2+����������Ķ��㣬��O2-�����������____��
����M�����У�Z4+������λ��Ϊ________��
����֪O2-�뾶Ϊ1.40��10-10m����Z4+�뾶Ϊ_________m��
�ο��𰸣�(1)�������ڵڢ�A�壻1s22s22p63s23p6
(2)ֱ���Σ�sp������
(3)��TiO2+BaCO3=BaTiO3+CO2���������ģ���6����6.15��10-13
���������
�����Ѷȣ�һ��
4��ѡ���� �����йؾ���������У��������
A�����ʯ����״�ṹ�У��ɹ��ۼ��γɵ���С̼������6��̼ԭ��
B����NaCl������ÿ��Na��(��Cl��)��Χ������6��Cl��(��6��Na��)
C���������У�����֮��ͨ�����ۼ���ϣ�����Ϊ60��
D�����Ӿ������ۻ�ʱ�����Ӽ����ƻ��������Ӿ����ۻ�ʱ����ѧ�������ƻ�
�ο��𰸣�C
���������A����ȷ��B����ȷ��Na����Cl�D����λ��Ϊ6��D����ȷ�����Ӿ������ۻ�ʱ�����Ӽ���뷢���ı䣬���Ӽ����ƻ��������Ӿ����ۻ�ʱ�����Ӽ����仯������ѧ�������ƻ��������γɵľ����Ƿ��Ӿ��壬��֮��ͨ�����Ӽ���������ϣ�C����ȷ���������ȷ�ģ���ѡC��
�����Ѷȣ�һ��
5��ѡ���� ���й��ھ����˵��һ����ȷ����(?)
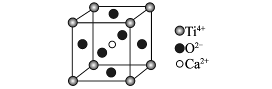
CaTiO3�ľ���ṹģ��(ͼ��Ca2+��O2-��
Ti4+�ֱ�λ������������ġ����ĺͶ���)
A�����Ӿ����ж����ڹ��ۼ�
B��CaTiO3������ÿ��Ti4+��12��O2-����
C��SiO2������ÿ����ԭ����������ԭ���Թ��ۼ�����
D������������۵㶼�ȷ��Ӿ�����۵��
�ο��𰸣�B
�����������Щ��ԭ�ӷ��Ӿ����в����ڹ��ۼ�����ϡ�����幹�ɵľ��壬A�������ھ�����Ti4+λ�ڶ����O2-λ�����ģ�����CaTiO3������ÿ��Ti4+��12��O2-���ڣ�B��ȷ��SiO2���塢Siԭ����4��Oԭ���Թ��ۼ���ϣ�C����������������Щ�ȷ��Ӿ�����۵�ͣ��繯������ΪҺ�壬D����
�����Ѷȣ���