1、选择题 下列叙述正确的是(?)
A.原子晶体中,共价键的键能越大,熔沸点越高
B.分子晶体中,分子间作用力越大,该分子越稳定
C.分子晶体中,共价键键能越大,熔沸点越高
D.某晶体溶于水中,可电离出自由移动的离子,该晶体一定是离子晶体
参考答案:A
本题解析:A、原子晶体中,原子间以极强的共价键结合。共价键越强,结合的越牢固,共价键的键能越大,断裂共价键消耗的能量就越高,熔沸点越高。正确。B、分子晶体中,分子间以分子间作用力结合。分子间作用力越大,破坏分子间作用力使物质融化或汽化消耗的能量就越高。即该晶体的熔沸点越高。错误。C、分子晶体中,共价键键能越大,分子就越稳定。错误。D、某晶体溶于水中,可电离出自由移动的离子,该晶体可能是离子晶体,也可能是分子晶体。错误。
本题难度:一般
2、填空题 NaCl的晶胞如图,已知钠的相对原子质量为23,氯的相对原子质量为35.5,Na+和C1―的核间距为a cm,用NA表示阿伏加德罗常数,则
(1)每个晶胞中平均分摊__?__个Na+,_?___个C1-。
(2)NaCl晶体的密度ρ的表达式为?g?cm-3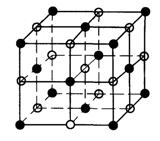
参考答案:(1)4? 4?(各1分)(2)58.5/2a3NA?(3分)
本题解析:(1)由均摊法可知:Na+: =4;C1―:
=4;C1―: =4
=4
(2)晶体包括四个NaCl,其质量为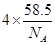 ,体积为
,体积为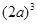 ;
;
则:ρ=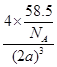 =
=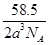
本题难度:一般
3、选择题 硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。如右图是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下面还各有一个镁原子;6个硼原子位于棱柱的侧棱上,则该化合物的化学式可表示为(? )
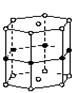
A.MgB
B.Mg3B2
C.MgB2
D.Mg2B3
参考答案:B
本题解析:根据晶胞结构并依据均摊法可知,晶胞含有的镁原子个数是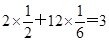 个,硼原子个数是
个,硼原子个数是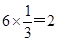 个,所以该化合物的化学式可表示为Mg3B2,答案选B。
个,所以该化合物的化学式可表示为Mg3B2,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。该题的关键是利用好均摊法,然后结合晶胞的结构灵活运用即可,有利于培养学生的逻辑推理能力和空间想象能力。
本题难度:一般
4、选择题 用烧热的钢针去接触涂有薄薄一层石蜡的云母片的反面,熔化了的石蜡呈椭圆形,这是因为(?)。
A.云母是热的不良导体,传热不均匀
B.石蜡是热的不良导体,传热不均匀
C.石蜡具有各向异性,不同方向导热性能不同
D.云母具有各向异性,不同方向导热性能不同
参考答案:D
本题解析:由“熔化的石蜡呈椭圆形”可知云母不同方向的导热性能不同,具有各向异性。
本题难度:简单
5、选择题 下列分子为直线形分子且分子中原子都满足8电子稳定结构( ? )
A.BeF2
B.C2H4
C.SO2
D.CO2
参考答案:D
本题解析:
本题难度:简单