| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《物质的量》试题强化练习(2017年最新版)(四)
参考答案:C 本题解析:A.只知道浓度缺少溶液的体积,所以无法确定溶液中微粒的数目的多少,错误;B.标准状况下,甲苯的状态是液态,不能使用气体摩尔体积,错误;C.常温下,9.2 g NO2和N2O4的混合气体中含有的氮原子数目为0.2 NA,正确;D.1 mol氯气和足量NaOH溶液反应转移的电子数目为NA,错误。 本题难度:一般 2、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是 参考答案:C 本题解析:ClO-能发生水解,A错;苯中没有C=C,B错;3mol NO2与水反应电子转移为什2mol,D错;答案选C。 本题难度:一般 3、选择题 设NA表示阿伏加德罗常数,下列说法不正确的是 参考答案:AD 本题解析:A 错误,体积比为2a∶b 本题难度:一般 4、选择题 下列说法中不正确的是 |
参考答案:B
本题解析:A、在非标准状况下,1 mol O2的体积也有可能是22.4 L,如在273℃,2个大气压条件下,1mol氧气的体积也是22.4L,A正确;B、在温度和压强一定时,气态物质的体积主要由气体分子数目和分子间的距离决定,与分子的大小没有关系,B错误;C、同温同压下,气体的体积之比等于其物质的量之比,C正确;D、同温同压下,相同体积的任何气体所含有的分子数目一定相同,D正确;答案选B。
考点:气体摩尔体积,阿伏加德罗定律及推论
本题难度:一般
5、填空题 如果我们规定12C的相对原子质量为24,且0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),那么下列几种物理量会有变化吗?若有,请说明变化结果。 (1)一个12C原子的质量?(2)阿伏加德罗常数(NA) (3)摩尔质量
(1)一个12C原子的质量?(2)阿伏加德罗常数(NA) (3)摩尔质量 (4)O2的相对分子质量?(5)气体摩尔体积?
(4)O2的相对分子质量?(5)气体摩尔体积? (6)98%(
(6)98%(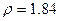 )硫酸的物质的量浓度?(7)44gCO2所含的分子个数
)硫酸的物质的量浓度?(7)44gCO2所含的分子个数
参考答案:(1)不变(2)变为原来的2倍(3)变为原来的2倍(4)变为原来的2倍(5)变为原来的2倍 (6)变为原来的0.5倍(7)不变
本题解析: (1)在规定12C的相对原子质量为24时,实际上是把作为相对原子质量的标准从原来用12C质量的1/12,改为1/24,但是单个碳原子的质量并没有因此而发生改变;
(1)在规定12C的相对原子质量为24时,实际上是把作为相对原子质量的标准从原来用12C质量的1/12,改为1/24,但是单个碳原子的质量并没有因此而发生改变; ( 2)原来是以0.012kg12C所含有的碳原子数作为阿伏加德罗常数(即6.02×1023),现在用0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),很明显0.024kg12C中所含的原子个数是0.012kg12C中所含的原子个数的2倍;故阿伏加德罗常数(NA)变为原来阿伏加德罗常数的2倍(即2×6.02×1023);
( 2)原来是以0.012kg12C所含有的碳原子数作为阿伏加德罗常数(即6.02×1023),现在用0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),很明显0.024kg12C中所含的原子个数是0.012kg12C中所含的原子个数的2倍;故阿伏加德罗常数(NA)变为原来阿伏加德罗常数的2倍(即2×6.02×1023); (3)原来所称摩尔质量,实质上是指1摩尔物质的质量即6.02×1023个微粒集体的质量,当作出了上述规定后,1摩尔所含的粒子数已经变成了原来的2倍,故其质量也就为原来的2倍;
(3)原来所称摩尔质量,实质上是指1摩尔物质的质量即6.02×1023个微粒集体的质量,当作出了上述规定后,1摩尔所含的粒子数已经变成了原来的2倍,故其质量也就为原来的2倍; (4) 原来氧分子的相对分子质量=氧分子的质量/12C质量的1/12,现在氧分子的相对分子质量=氧分子的质量/12C质量的1/24,即作为相对原子质量的标准变为了原来的一半,而氧分子的质量是固定的,故氧分子的相对分子质量变为原来的2倍;
(4) 原来氧分子的相对分子质量=氧分子的质量/12C质量的1/12,现在氧分子的相对分子质量=氧分子的质量/12C质量的1/24,即作为相对原子质量的标准变为了原来的一半,而氧分子的质量是固定的,故氧分子的相对分子质量变为原来的2倍;
 (5)气体摩尔体积是指在一定的温度和压强下, 阿伏加德罗常数个气体分子所占有的体积,由于阿伏加德罗常数已经变成了原来的2倍,气体摩尔体积当然也就是原来的2倍了;
(5)气体摩尔体积是指在一定的温度和压强下, 阿伏加德罗常数个气体分子所占有的体积,由于阿伏加德罗常数已经变成了原来的2倍,气体摩尔体积当然也就是原来的2倍了; (6) 溶质的物质的量浓度(CB)=溶质的物质的量(n)/溶液的体积(V),在单位体积的98%(
(6) 溶质的物质的量浓度(CB)=溶质的物质的量(n)/溶液的体积(V),在单位体积的98%(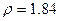 )硫酸中所含溶质――硫酸的质量是不变的
)硫酸中所含溶质――硫酸的质量是不变的
 (7) 不论作为相对原子质量的标准如何变化,单个CO2分子的质量并未变化,故一定质量的CO2所含的分子个数是不会发生变化的。
(7) 不论作为相对原子质量的标准如何变化,单个CO2分子的质量并未变化,故一定质量的CO2所含的分子个数是不会发生变化的。
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《元素周期律.. | |