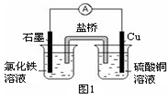
1������� ��1��ͼ1װ�÷�����Ӧ�����ӷ���ʽΪ?��
 ?
?
��2��ͼ2װ���м��ձ�ʢ��100 mL 0.2 mol��L��1��NaCl��Һ�����ձ�ʢ��100 mL 0.5 mol��L��1L��CuSO4��Һ����Ӧһ��ʱ���ֹͣͨ�硣����ձ��е��뼸�η�̪��Һ���۲쵽ʯī�缫�������ȱ�졣
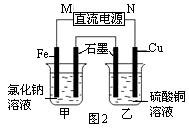
�� ��Դ��M��Ϊ?�������ձ������缫�ĵ缫��ӦΪ?��
�� ���ձ��е�ⷴӦ�Ļ�ѧ����ʽΪ?��
�� ֹͣ��⣬ȡ��Cu�缫��ϴ�ӡ�����������缫���� 0.64 g�����ձ��в����������״�������Ϊ?mL ��
��3��ͼ3�Ǽ״�ȼ�ϵ�أ��������ҺΪKOH��Һ���ṹʾ��ͼ��д�� b���ĵ缫��Ӧʽ?��
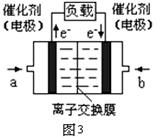
�״�ȼ�ϵ�ص��ܷ�Ӧ��ѧ����ʽ?��
�ο��𰸣���14�֣�
��1��2Fe3+ + Cu = 2Fe2+ + Cu2+��2�֣�
��2���� ����2�֣���? Fe - 2e-= Fe2+��2�֣�
�� 2CuSO4+ 2H2O 2Cu + O2�� + 2H2SO4?��2�֣�? �� 224��2�֣�
2Cu + O2�� + 2H2SO4?��2�֣�? �� 224��2�֣�
��3��O2+4e-+2H2O = 4OH-��2�֣�? 2CH3OH+4KOH+3O2= 2K2CO3 +6H2O��2�֣�
�����������1��Fe3+��Cu����������ԭ��Ӧ�����ӷ���ʽΪ2Fe3+ + Cu = 2Fe2+ + Cu2+��
��2���ٷ�Ӧһ��ʱ���ֹͣͨ�磮����ձ��е��뼸�η�̪���۲쵽ʯī�缫�������ȱ�죬˵����ʯī�缫������OH-���ӣ��缫��ӦΪ��2H2O+2e-�T2OH-+H2����
������ԭ��Ӧ��Ϊ���ص����������ӵ�Դ�ĸ�������M��Ϊ������M��Ϊ������������ӦΪFe-2e-�TFe2+���ʴ�Ϊ������Fe-2e-�TFe2+��
�����ձ��������ͭ��Һ��ʯīΪ�������缫��ӦΪ4OH--4e-�TO2��+H2O��CuΪ�������缫��ӦΪCu2++2e-�TCu�������ܷ�ӦΪ2Cu2++2H2O 2Cu+O2��+4H+��
2Cu+O2��+4H+��
�ʴ�Ϊ��2Cu2++2H2O 2Cu+O2��+4H+��
2Cu+O2��+4H+��
��ȡ��Cu�缫��ϴ�ӡ�����������缫����0.64g��������Cu�����ʵ���Ϊ0.64g/64(g/mol) =0.01mol��ת�Ƶĵ��ӵ����ʵ���Ϊ0.01mol��2=0.02mol��
���ݼ��ձ���������ĵ缫��Ӧ������������������
2H2O+2e-�T2OH-+H2����
2mol?22.4L
0.02mol ?V
V=(22.4l*0.02mol)/2mol=0.224L����224ml���ʴ�Ϊ��224��
��3��B����������ͨ���O2���õ����ӣ��缫��ӦʽΪO2+4e-+2H2O= 4OH-���������ҺΪKOH��Һ�����鷴Ӧ���ɵ�CO2���KOH��Ӧ���ʼ״�ȼ�ϵ�ص��ܷ�Ӧ��ѧ����ʽ2CH3OH+4KOH+3O2= 2K2CO3 +6H2O��
���������⿼��绯ѧ֪ʶ����Ŀ�Ѷ��еȣ�����ʱע��缫���жϺ͵缫��Ӧ����д��ע�����·�и��缫ת�Ƶĵ�����Ŀ��ȣ����÷�Ӧ�ķ���ʽ���㡣
�����Ѷȣ�һ��
2��ѡ���� ��ͼ���ձ���ʢ�к�ˮ������������C�������б���ʴ�ɿ쵽����˳��Ϊ��������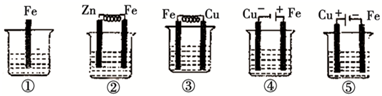
A���ڢ٢ۢܢ�
B���ܢۢ٢ڢ�
C���ݢܢڢ٢�
D���ݢۢڢܢ�
�ο��𰸣���ԭ��ظ����������������Ľ������ٱ���ʴ����ԭ�����������������Ľ�������������������ʴ����˳���ǣ�����������ԭ��ظ�������ѧ��ʴ��ԭ�������������������
������������ѧ��ʴ��
����������������������
����Fe��ʧ���������������ٱ���ʴ��
�����������������ٱ���ʴ��
����������������������
ͨ�����Ϸ���֪��Fe����ʴ�ɿ쵽��˳���Ǣܢۢ٢ڢݣ���ѡB��
���������
�����Ѷȣ�һ��
3��ѡ���� ���Խ���ӦZn+Br2 = ZnBr2��Ƴ����أ�����4���缫��Ӧ
��Br2 + 2e��= 2Br- ��2Br- - 2e��= Br2 ��Zn
�ο��𰸣�
���������
�����Ѷȣ�һ��
4��ѡ���� ����ȼ�ϵ���Բ����缫��KOH��Һ���������Һ���Ըõ�ص�˵����ȷ����
A��������ӦΪO2+2H2O+4e��===4OH��
B����ع���ʱ��������pH����
C����ع���ʱ��Һ�е���������������
D����ص��ܷ�ӦΪ��2H2+O2===2H2O
�ο��𰸣�BD
���������ԭ����и���ʧȥ���ӣ������õ����ӣ����������ڸ���ͨ�룬����������ͨ�롣���ڵ�������������أ������������ķ�ӦʽΪO2+2H2O+4e��===4OH����2H2��4e����4OH��=4H2O�����BD��ȷ��AC����ȷ��ԭ�����Һ�е���������������ѡBD��
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ���ǣ�������
A�����������绯ѧ��ʴ��������Ӧʽ��Fe=Fe2++2e-
B������ȼ�ϵ�صĸ�����Ӧʽ��O2+2H2O+4e-=4OH-
C����ͭ����ʱ�����Դ�����������Ǵ�ͭ
D���ö��Ե缫��ⱥ��ʳ��ˮʱ�������ĵ缫��Ӧʽ��2Cl-=Cl2��+2e-
�ο��𰸣�A�������к�������̼���ڳ�ʪ�Ļ����й���ԭ��أ�����������̼��������������Ӧʽ��Fe=Fe2++2e-����A����
B���ڼ��Ի����£�����ȼ�ϵ�صĸ�������ӦʽΪ��O2+2H2O+4e-=4OH-����B����
C����ͭ����ʱ�����Դ�����������Ǵ�ͭ����C����
D���ö��Ե缫��ⱥ��ʳ��ˮʱ���������������ӷ���ʧ���ӵ�������Ӧ�����������ĵ缫��Ӧʽ��2Cl-=Cl2��+2e-����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��