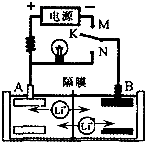
1、实验题 某课外活动小组同学用右图装置进行相关的实验,试回答下列问题。
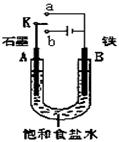
(1)若开始时开关K与a连接,则A极的电极反应式为?。
(2)若开始时开关K与b连接,则总反应的离子方程式为?。在该实验中,下列说法正确的是(填序号)?。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后(设NaCl足量)加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则有0.2 mol电子转移
(3)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是?。
A.C(s) + H2O(g) =" CO(g)" + H2(g) ?△H > 0
B.NaOH(aq) + HC1(aq) =" NaC1(aq)" + H2O(1)? △H < 0
C.2H2(g) + O2(g) = 2H2O(1) ?△H<0
(4)电解原理在化学工业中有着广泛的应用。右图中,a为电解液,X和Y是两块电极板,回答下列问题:
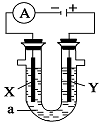
(4)①若X和Y均为惰性电极,a为CuSO4溶液,则电解时的化学反应方程式为?。通过一段时间后,向所得溶液中加入8g CuO粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为?。
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电极反应式为?。
参考答案:(17分)
(1)2H2O + O2↑+4e-=4OH-?(3分)
(2)2Cl- + 2H2O ?电解??2OH- + H2↑ + Cl2↑(3分) ? ②④(2分)
(3)C(2分)
(4)①2CuSO4+2H2O ?电解??Cu+O2↑+2H2SO4(3分) ?0.2mol(2分)
②Cu -2e- = Cu2+ (2分)
本题解析:(1)开始时开关K与a连接,是原电池,铁为负极,发生氧化反应,失去电子生成亚铁离子,故答案为:Fe-2e-=Fe2+;
(2)开关K与b连接,装置为电解池,铁为阴极,发生还原反应,氢离子得到电子生成氢气,电解饱和食盐水生成氢氧化钠、氢气和氯气,电解过程中阳离子向阴极移动,①错误,A生成氯气,能使湿润KI淀粉试纸变蓝,②错误,反应一段时间后加适量HCl气体可恢复到电解前电解质的浓度,③错误,若标准状况下B极产生2.24L氢气,转移0.2mol电子,④正确,故答案为:2H++2e-=H2↑; 2Cl-+2H2O 2OH-+H2↑+Cl2↑;②正确。
2OH-+H2↑+Cl2↑;②正确。
(3)放热反应中,△H<0,形成原电池的反应必须为氧化还原反应,故选C。
(4)①电解CuSO4溶液,生成Cu单质、O2和H2SO4,方程式为2CuSO4+2H2O ?电解??Cu+O2↑+2H2SO4。8g CuO,即0.1mol,根据质量守恒定律,反应的CuSO4为0.1mol,故电解过程中转移的电子的物质的量为0.2mol。
②阳极上失电子,故Y极的电极反应式为Cu -2e- = Cu2+。
点评:本题考查原电池和电解池原理和原电池的设计,解题时要注意分析电极反应及生成物,能设计成原电池的反应必须是放热反应,同时必须是氧化还原反应。
本题难度:一般
2、选择题 关于化学电源的叙述,错误的是
A.化学电源均是根据原电池的工作原理设计的
B. 在干电池中,碳棒只起导电作用,并不参加化学反应
C. 镍镉电池不能随意丢弃的原因是镍、镉的资源有限,价格昂贵
D. 燃料电池是一种高效、环保的新型化学电源
参考答案:C
本题解析:
分析:A、化学电源均是根据原电池的工作原理设计的;
B、在干电池中,碳棒为正极,正极上是二氧化锰得电子的反应;
C、根据废旧电池的污染性来回答;
D、根据燃料电池的特点来回答.
解:A、化学电源均是根据原电池的工作原理设计的,故A正确;
B、在干电池中,碳棒为正极,正极上是二氧化锰得电子的反应,碳棒不参与化学反应,故B正确;
C、因为废旧的镍镉电池有腐蚀性和污染性,不能随意丢弃,故C错误;
D、燃料电池是一种高效、环保的新型化学电源,故D正确.
故选C.
本题难度:一般
3、填空题 23.已知:铅蓄电池总的化学方程式为:Pb+PbO2+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
负极反应为:Cd+2OH--2e-=Cd(OH)2
铅蓄电池使用(放电)一段时间后,其内阻明显增大,电压却几乎不变,此时只有充电才能继续使用。镍镉碱性充电电池使用(放电)到后期,当电压明显下降时,其内阻却几乎不变,此时充电后也能继续使用。回答下列问题:
⑴铅蓄电池在放电时的负极反应为 ,其在充电时阳极反应为 ;
⑵镍镉碱性充电电池在充电时的总反应的化学方程式为 ;
⑶上述两种电池使用一段时间后,一个内阻明显增大,而另一个内阻却几乎不变的主要原因可能是 ;
⑷如果铅蓄电池在放电时回路中有2mol电子转移时,消耗H2SO4 mol。
参考答案:(1)Pb+SO42―-2e―=PbSO4 PbSO4+2H2O-2e―=PbO2+SO42―+4H+
(2)Cd(OH)2+2Ni(OH)2=Cd+2NiO(OH)+2H2O
(3)铅蓄电池放电时离子浓度减小,而镍镉电池放电时离子浓度不变
(4)2
本题解析:略
本题难度:一般
4、选择题 如图是一种锂电池的充、放电示意图.已知放电时该电池的电极反应式为:负极:Li-e-=Li+;?正极:FePO4+Li++e-=LiFePO4则下列说法不正确的是( )
A.该电池的反应式为FePO4+Li
LiFePO4
B.K与N相接时,Li+由A极区迁移到B极区
C.K与M相接时,A是阳极,发生氧化反应
D.本装置充、放电过程中至少存在三种形式的能量转化