1、实验题 (6分)如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。

(1)图中有两处明显的错误是
①?;②?。
(2)A仪器的名称是?,B仪器的名称是?。
(3)实验时A中除加入少量自来水外,还需要加入少量的?,其作用是?。
参考答案:(6分)
(1)①温度计水银球插入太深②冷却水进出口标反了
(2)?蒸馏烧瓶?、?冷凝管?
(3)?沸石(或碎瓷片)?、?防止液体暴沸?每空1分
本题解析:(1)根据装置图可知,在蒸馏是温度计测量的是气体的温度,而不是液体的温度,因此温度计水银球应该放在蒸馏烧瓶的支管出口处;其次,冷却水的方向应该和气体的流向相反,即下口进,上口出。
(2)根据仪器的结构特点可知,A是蒸馏烧瓶,B是冷凝管。
(3)蒸馏时需要加热,所以在A中还需要加入碎瓷片,以防止暴沸。
本题难度:一般
2、选择题 下列根据某无色试液的实验现象所作出的结论中一定不正确的是
A.焰色反应呈黄色,结论:试液中一定含有Na+
B.加入盐酸酸化的氯化钡溶液,、出现白色沉淀,结论:试液中一定含有SO42―
C.与浓氢氧化钠溶液产生使红色石蕊试纸变蓝的气体,结论:该试液一定含NH4+
D.加入碳酸钠溶液产生白色沉淀,结论:试液中可能含氢氧化钙
参考答案:B
本题解析:
A、正确,溶液中钠只能以Na+ 形式存在;B、不正确,还可能是AgCl沉淀;C、正确,NH3的水溶液呈碱性;D、不正确,Ba (OH)2等也可能。
本题难度:简单
3、选择题 下列有关制取蒸馏水的装置和操作的说法中,不正确的是( )
A.蒸馏烧瓶底部必须垫石棉网
B.冷凝管内水的流向是下进上出
C.实验中需在自来水中加几片碎瓷片
D.温度计的水银球应插入蒸馏烧瓶内的自来水中
参考答案:A.蒸馏时为防止蒸馏烧瓶受热不均匀而导致炸裂,蒸馏烧瓶底部必须垫石棉网,故A正确;
B.冷凝管内水的流向是下进上出,可使冷水充满冷凝管,起到充分冷凝的效果,故B正确;
C.为防止暴沸,实验中需在自来水中加几片碎瓷片,故C正确;
D.温度计的水银球应插入蒸馏烧瓶内支管口附近,故D错误.
故选D.
本题解析:
本题难度:简单
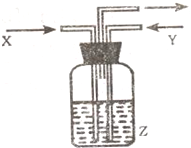
4、选择题 下列各组物质中,气体X和气体Y同时通入盛有溶液Z的洗气瓶中(如图所示),一定没有沉淀生成的是( )
| X | Y | Z
A
SO2
N?O2
BaCl2
B
O2
NH3
Al(NO3)3
C
SO2
C?O2
CaCl2
D
NH3
C?O2
MgSO4
|
A.A
B.B
C.C
D.D