1、选择题 海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
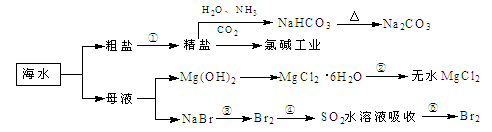
下列有关说法正确的是
A.过程①中除去粗盐中的SO、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.用澄清的石灰水可鉴别NaHCO3和Na2CO3
C.过程②中结晶出的MgCl2・6H2O要在HCl氛围中加热脱水制得无水MgCl2
D.工业上通过电解饱和MgCl2溶液制取金属镁
参考答案:C
本题解析:A、除去粗盐中的SO、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,错误;B、石灰水与NaHCO3和Na2CO3均反应,生成白色沉淀,不能鉴别,错误;C、MgCl2・6H2O水解生成氢氧化镁和氯化氢,加热促进水解,最终得氧化镁,所以为了抑制水解,要在HCl氛围中加热脱水制得无水MgCl2,正确;D、电解饱和MgCl2溶液得到氢氧化镁沉淀,得不到镁单质,错误,答案选C。
本题难度:一般
2、选择题 氯碱工业的产物NaOH与不同物质反应可以生成不同的盐。已知常温下,浓度均为0.1 mol・L-1的4种钠盐溶液的pH如下表:
溶质
| Na2CO3
| NaHCO3
| NaClO
| NaHSO3
|
pH
| 11.6
| 9.7
| 10.3
| 5.2
|
?
下列说法中正确的是
A.向氯水中加入NaHCO3溶液,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,pH最大的是H2SO3溶液
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(H+)>c(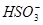 )>c(
)>c(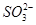 )>c(OH-)
)>c(OH-)
参考答案:A
本题解析:依据Cl2+H2O H++Cl-+HClO结合NaHCO3只与H+反应可知A选项正确;水解程度最大的是Na2CO3,B选项错误;相同浓度时,H2SO3的pH最小,C选项错误;c(
H++Cl-+HClO结合NaHCO3只与H+反应可知A选项正确;水解程度最大的是Na2CO3,B选项错误;相同浓度时,H2SO3的pH最小,C选项错误;c(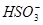 )>c(H+),D选项错误。
)>c(H+),D选项错误。
本题难度:一般
3、选择题 下列说法正确的是
[? ]
A.一定温度下,反应MgCl2(1) ==Mg(1)+ Cl2(g)的 △H>0,△S>0
B.水解反应NH4++H2O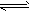 NH3・H2O+H+达到平衡后,升高温度平衡逆向移动
NH3・H2O+H+达到平衡后,升高温度平衡逆向移动
C.铅蓄电池放电时的负极和充电时的阳极均发生还原反应
D.对于反应2H2O2==2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率
参考答案:AD
本题解析:
本题难度:一般
4、选择题 物质的量浓度相同的200mL Ba(OH)2溶液和150mL NaHCO3混合后,最终溶液中离子的物质的量浓度关系正确的是
A.c(OH-)>c(Ba2+)>c(Na+)>c(CO32-)
B.c(OH-)>c(Na+)>c(Ba2+)>C(H+)
C.c(OH-)=c(Ba2+)+c(Na+)+c(H+)
D.c(H+)+c(Na+)+2c(Ba2+)=c(OH-)
参考答案:B
本题解析:为了便于计算,设 Ba(OH)2和 NaHCO3的物质的量分别为4mol和3mol,则
n(OH-)="8mol?" n(Ba2+)="4mol?" n(Na+)="3mol?" n(HCO3-)="3mol?" ;反应后:
n(OH-)="5mol?" n(Ba2+)="1mol?" n(Na+)="3mol?" ,所以选B
本题难度:一般
5、选择题 醋酸钡[(CH3COO)2Ba・H2O]是一种媒染剂,下列是有关0.1mol/L醋酸钡溶液中粒子浓度的比较,其中错误的的是
A.c(Ba2+) >c(CH3COO-)>c(OH-)>c(H+)
B.c(H+)+2c(Ba2+)= c(CH3COO-) +c(OH-)
C.c(H+) = c(OH-)-c(CH3COOH)
D.2c(Ba2+)= c(CH3COO-)+ c(CH3COOH)
参考答案:A
本题解析:A.(CH3COO)2Ba,因为水解是微弱的,c(CH3COO-) >c(Ba2+)>c(OH-)>c(H+),错误;B.电荷守恒,正确;C.质子守恒,正确;D.物料守恒,正确。
本题难度:一般