1、选择题 下列有关实验现象的记录不正确的是
A.钠可以在氯气中燃烧,产生白色的烟
B.红热的铜丝可以在氯气中燃烧,生成棕色的烟
C.纯净的氢气可以在氯气中安静燃烧,发出苍白色火焰
D.氯气作用于干燥的品红试纸,试纸不褪色
参考答案:B
本题解析:考查实验现象的描述。红热的铜丝可以在氯气中燃烧,生成棕黄色的烟,选项B不正确,AC都是正确的。次氯酸具有漂白性,而氯气是没有的,所以选项D正确,答案选B。
本题难度:一般
2、选择题 某化学教师设计了“氯气与金属反应”的装置与操作来替代相关的课本试验。实验操作:先给钠预热,到钠熔融或圆球时,撤去酒精灯,通入氯气,即可见钠着火燃烧,并产生大量白烟。以下叙述错误的是

[? ]
A.钠着火燃烧产生苍白色火焰 ?
B.反应生成的大量白烟是氯化钠晶体?
C.管中部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气 ?
D.根据管右端棉球颜色变化情况可判断氯气是否被碱液完全吸收
参考答案:A
本题解析:
本题难度:简单
3、填空题 某学生利用以下装置探究纯净干燥的氯气与氨气之间的反应.
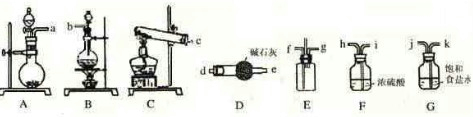
回答下列问题:
(1)根据下列所给试剂,选择制取氨气的装置是(填对应字母)______;写出制备氯气的离子反应方程式______.
二氧化锰、碱石灰、浓盐酸、浓氨水、烧碱、生石灰
(2)已知,E装置是用于使纯净干燥的氯气与氨气发生反应的装置,试说明该装置的设计意图:______.
(3)根据实验目的,所选装置的连接顺序为(填装置的接口字母):______接______,______接(?f?),(?g?)接______,______接______,______接______;其中,G装置的作用是______.
(4)氯气和氨气在常温下相混合就会发生反应生成氯化铵和氮气,该反应的化学方程式为:______;其中,氧化剂与还原剂的物质的量之比是______.
(5)请你评价此套装置有何缺点______.
参考答案:(1)根据提供的药品,应用浓氨水和碱石灰或生石灰反应制备氨气,可用A装置,实验室用二氧化锰和浓盐酸反应制备氯气,反应的离子方程式
为MnO2+4H++2C1-?△?.?Mn2++C12↑+2H2O,故答案为:A;?MnO2+4H++2C1-?△?.?Mn2++C12↑+2H2O;
(2)由于氨气的密度小,氯气的密度大,密度小氨气的从长管进入向上扩散,密度大的氯气从短管进入向下扩散,这样能较快的充分的混合,具体操作为将比空气轻的氨气从长管口f进入,比空气重的氯气从短管口g进入,使反应气体逆流接触充分反应,中间导管用于排出空气以减少内部压力,
故答案为:将比空气轻的氨气从长管口f进入,比空气重的氯气从短管口g进入,使反应气体逆流接触充分反应,中间导管用于排出空气以减少内部压力;
(3)装置A制取氨气,可用浓氨水与碱石灰(或烧碱或生石灰等),B装置中盛放的碱石灰,用来干燥氨气;G装置中盛放的饱和食盐水,用来除去氯气中混有的氯化氢气体;F装置用来干燥氯气,然后在E中混合反应,则连接顺序为a接d,e接f,g接h,i接j,k接b,
故答案为:a;d;e;h;i;j;k;b;除去C12中的HCl气体;
(4)氯气和氨气在常温下相混合就会发生反应生成氯化铵和氮气,反应的化学方程式为3C12+8NH3=6NH4Cl+N2,由化合价的变化可以看出,当3mol氯气参加反应时,有2mol氨气被氧化,所以氧化剂和还原剂的物质的量之比为3:2,
故答案为:3C12+8NH3=6NH4Cl+N2;3:2;
(5)氯气和氨气都污染空气,不能直接排放到空气中,实验缺少尾气处理装置,
故答案为:缺少尾气处理装置,造成空气污染.
本题解析:
本题难度:一般
4、选择题 下列说法正确的是
A.氯气中含有少量的氯化氢,可以用NaOH溶液除去
B.漂白粉的有效成分是CaCl2和Ca(ClO)2
C.潮湿的氯气可用浓硫酸进行干燥
D.实验室制取氯气时可用向上排空气法收集
参考答案:CD
本题解析:A错,氢氧化钠既能与氯气反应又能与氯化氢反应;B错,漂白粉的有效成分是Ca(ClO)2
本题难度:简单
5、选择题 下列实验现象的描述错误的是( )
A.新制氯水使淀粉试纸呈蓝色
B.向NaHCO3固体加入新制氯水,有无色气体产生
C.向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,呈血红色
D.在新制氯水中滴加AgNO3溶液有白色沉淀生成
参考答案:A.氯水中含有氯气,与淀粉不发生颜色反应,故A错误;
B.新制氯水中含有盐酸,可与碳酸氢钠反应生成无色二氧化碳气体,故B正确;
C.氯水中氯气可与氯化亚铁反应生成氯化铁,滴加KSCN溶液,呈血红色,故C正确;
D.氯气与水发生Cl2+H2O=H++Cl-+HClO,溶液中含有Cl-,则滴加AgNO3溶液中出现白色沉淀,故D正确.
故选A.
本题解析:
本题难度:一般