1������� ��7�֣���ͼΪһ����AlCl3��Һ�м���NaOH��Һ����Al(OH)3��ɫ������������NaOH�����ʵ���֮��Ĺ�ϵ���ߣ��Իش�
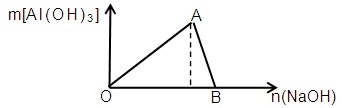
(1) A��ʱ�Ѳμӷ�Ӧ��AlCl3��NaOH�����ʵ���֮����?
(2) OA����������ʾ�ķ�Ӧ�����ӷ���ʽ��?
(3) AB����������ʾ�ķ�Ӧ�����ӷ���ʽ��?
(4) B����Һ�д��ڵ�Ũ������������?�������ӷ��ţ�����B�������ɵ���Һ��ͨ��CO2���ɼ�����������?
�ο��𰸣���7�֣�
�� 1:3��1�֣�
�� Al3����3OH-==Al(OH)3��(2��)
�� Al(OH)3��OH�D==AlO2����2H2O (2��)
�� Na�� ; ���ɰ�ɫ��������1�֣�
�����������
�����Ѷȣ�һ��
2��ѡ���� ȡͬ�����pH = 2������ʹ��ᣬ�ֱ�ϡ��10����������������ȷ����
[? ]
A��ϡ�ͺ������pH���ڴ�����Һ��pH
B��ϡ�ͺ����������Һ�ֱ���뵽������̼���Ʒ�ĩ��Ӧ����ͬ��ͬѹ�£���������Ķ�����̼�������
C��ϡ�ͺ������Һ�ֱ���ͬŨ�ȵ�����������Һ��Ӧʱ�������������ƻ�����Һ�� �����ͬ
D��ϡ�ͺ�����Һ��pH�ֱ��Ϊ3
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� ��ֲ�ﻨ�п���ȡһ�ּ�дΪHIn���л������ˮ��Һ�����������ƽ�⣺HIn����Һ����ɫ��
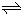
H+����Һ����ɫ��+In-����Һ����ɫ��?���������ָʾ����������Һ�м���Na202��ĩ������Һ��ɫΪ��������
A����ɫ����
B����ɫ��dz
C����ɫ����
D����Ϊ��ɫ
�ο��𰸣�������������ˮ����ǿ���������ƣ���Һ�Լ��ԣ�ָʾ���ȱ�ƣ�Ȼ������Ϊ�������Ƶ�ǿ������ʹָʾ����ɫ����Ϊ��ɫ��
��ѡD��
���������
�����Ѷȣ���
4��ѡ���� ����ձ��м������ᣬ���ձ��м�����ᣬ������Һ�������pH ����ȡ��������ձ���ͬʱ�����������ȵ�п������Ӧ������õ�����������������˵������ȷ����
[? ]
A�����ձ��з���п�����������ձ��з���п������С
B�����ձ��е������
C�����ձ��вμӷ�Ӧ��п����
D����Ӧ��ʼ�����ձ��е�c(H+)ʼ�ձȼ��ձ��е�c(H+)С
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5��ѡ���� ijһԪ����HA�ĵ����Ϊa����Ũ��Ϊ1 mol��L-1��HA��Һ�У�H+���ӡ�A-���Ӻ�δ�����HA���ӵ��ܸ����ǰ����ӵ�������?
A��a��
B����1-a����
C����1+a����
D��2a��
�ο��𰸣�C
�����������HA����Һ�����Ϊ1L����HA���ʵ���Ϊ1mol
HA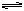 H+?+A-
H+?+A-
��ʼʱ���ʵ���(mol)1? 0? 0
��������ʵ���(mol)��?��?��
ƽ��ʱ���ʵ���(mol)1-��?��?��?��1+��
��֪��ƽ��ʱH+��A-��δ�����HA���������ʵ���Ϊ(1����)mol����Ϊ�����ӵ�������(1����)����
�����Ѷȣ�һ��