1、选择题 含有相同分子数的下列物质,质量最小的是
A.O2
B.CH4
C.CO2
D.SO2
参考答案:B
本题解析:根据阿伏加德罗定律可知,含有相同分子数,则物质的物质的量是相等的。因此根据n=m/M可知,质量最小的是甲烷,答案选B。
本题难度:简单
2、选择题 下列哪种试剂一次性实验就能鉴别四种溶液:Na2CO3、(NH4)2SO4、NH4Cl、KNO3
A.AgNO3溶液
B.NaOH溶液
C.Ba(OH)2溶液
D.盐酸
参考答案:C
本题解析:略
本题难度:一般
3、填空题 (10分)为了除去NaCl溶液中少量的MgCl2、Na2SO4,从稀盐酸,Na2CO3,K2CO3,Ba(NO3)2,Ba(OH)2溶液中,选择A、B、C? 3种试剂,按图中步骤进行操作:

(1)下列试剂的化学式A??C?
(2)加入过量A的原因是?,有关反应的离子方程式是?,?
(3)加入过量B有关反应的离子方程式是?。
参考答案:(1)A:Ba(OH)2?C:HCl
(2) 除尽溶液中的Mg2+和 SO42- , Mg2+ + 2OH- = Mg(OH)2↓? Ba2+ + SO42- = BaSO4↓
(3) Ba2+ + CO32-= BaCO3↓
本题解析:本题实质是除去Mg2+和SO42-。加过量氢氧化钡溶液可同时除去这两种离子,但又引入了Ba2+和OH-,加过量碳酸钠溶液除去Ba2+,加适量盐酸除去OH-和CO32-。
(1)A、B、C分别为氢氧化钡溶液、碳酸钠溶液、盐酸。
(2)加过量氢氧化钡溶液的目的是使Mg2+和SO42-沉淀完全,离子方程式为Mg2+ + 2OH- = Mg(OH)2↓、Ba2+ + SO42- = BaSO4↓。
(3)加入过量碳酸钠溶液的离子方程式为Ba2+ + CO32- = BaCO3↓。
点评:除杂时加入的试剂要过量,过量的试剂在后续的步骤中要除去。
本题难度:一般
4、实验题 MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。某研究性学习小组设计了将粗MnO2(含有较多的MnO2和MnCO3)样品转化为纯MnO2实验,其流程如下

(1)第①步加稀H2SO4时,粗MnO2样品中的_________(写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、________、________、________,已知蒸发得到的固体中有NaClO3和NaOH,则一定还有含有________(写化学式)。
(4)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7gMnO2,并收集到0.224L CO2(标准状况下),则在第②步反应中至少需要________mol NaClO3。
参考答案:(1)MnO2和MnCO3
(2)5Mn2+、2、4H2O、5、8H+
(3)蒸发皿;酒精灯;玻璃棒;NaCl
(4)0.02
本题解析:
本题难度:一般
5、实验题 FeCl3常用作印刷电路铜板腐蚀剂。腐蚀铜板后的混合溶液中,若Cu2+ 、Fe3+和Fe2+的浓度均为0.10mol/L,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和 Fe2+的实验步骤___________。
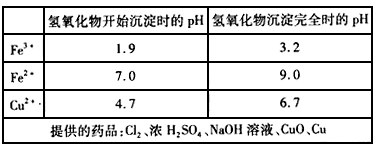
参考答案:①通入足量氯气将Fe2+氧化成Fe3+;
②加入CuO 调节溶液的pH至3.2~4.7;
③过滤[除去Fe( OH)3]
本题解析:
本题难度:一般