1��ѡ���� ��0.1mol?L-1NaOH��Һ��ͨ�������CO2����Һ�д��ڵ���Ҫ���������еģ�������
A��Na+��CO32-
B��Na+��HCO3-
C��HCO3-��CO32-
D��Na+��OH-
�ο��𰸣��������ƺ����Ķ�����̼��Ӧ����̼������NaOH+CO2=NaHCO3��̼��������ǿ��������ʽ�Σ���ˮ��Һ�����������ƶ��������Ӻ�̼��������ӣ�̼�������ˮ��Ҳ�ܵ��룬�����Ƚ�����������Һ�д��ڵ���Ҫ�����������Ӻ�̼��������ӣ���ѡB��
���������
�����Ѷȣ�һ��
2��ѡ���� ������������Һ���ܴ����������
A.H����NO3����Fe3����Na��
B.Ag����NO3����Cl����K��
C.K����Ba2����OH����SO42��
D.Cu2����NH4����Br����OH��
�ο��𰸣�A
���������A��ȷ��
B���������Ӻ������Ӳ��ܹ��档
C�������Ӻ���������ӹ��档
D����ͭ���Ӻ����������Ӳ��ܴ������档
�����Ѷȣ�����
3������� ij��ɫ��Һ�������п��ܴ��ڵ��������£�Na+��Ag+��Ba2+��Al3+��AlO2-��S2-��CO32-��SO32- ��SO42-����ȡ����Һ�����й�ʵ�飬ʵ��������ͼ��ʾ��
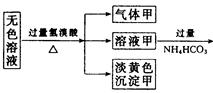
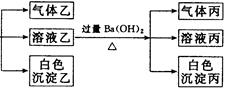
��1����������??�����ɳ��������ӷ���ʽ??��
��2����������??������Һ�����ɳ����ҵ����ӷ���ʽ??��
��3����������??��
��4���ۺ�������Ϣ�����Կ϶����ڵ�������??��
�ο��𰸣�(1)S;? 2S2-+SO32��+6H+=3S��+3H2O
(2)Al(OH)3; Al3++3HCO =Al(OH)3��+3CO2��
=Al(OH)3��+3CO2��
(3)BaCO3, ������BaSO4;?�ڳ������м����������ᣬ����������ȫ���ܽ⣬˵����BaCO3���BaSO4����ȫ���ܽ⣬�����BaCO3.
(4) S2-��SO ��AlO
��AlO ��Na+
��Na+
��������������ͻ�ƿ��dz����ס��ҡ����ijɷ֣�������������������ɵ���ɫ�����ף��ع���ѧ��ѧ�г����ĵ���ɫ������AgBr��S��Ag3PO4�ȡ�����Ӧ���ų��ų�Ag3PO4�ģ��ؼ�����AgBr����S������AgBr�����Ļ�������Ag+������е�4�������Ӿ����ܴ������棬�Ӷ������Ag+����֪����S����Ȼ�˴���S����Һ��S2-��SO32-�����������·����Ĺ��з�Ӧ���ɵġ��ɴ��Ƴ�ԭ��Һ�д���S2-��SO32-��������SO32-������һ��������Ba2+��Fe3+�����ݵ�����ԭ����Һ�б����������ӣ���һ������Na+�����������HBr�������S2-��Ӧ���ɵ�H2S��Ҳ������HBr�������SO32-��Ӧ���ɵ�SO2��Ҳ������HBr��ԭ��Һ�п��ܴ��ڵ�CO32-��Ӧ���ɵ�CO2��������NH4HCO3�кͶ����H+���ַ�Ӧ���ɰ�ɫ�����ң���������е����ӣ�Ag+��Ba2+��Fe3+�������ڣ����Ƴ�������ֻ������AlԪ�������Al(OH)3��������HCO3-��Al3+����˫ˮ������ɵģ���Al3+������AlO2-������������ᷴӦ���ɵģ�����ԭ��Һ��һ������AlO2-����������HCO3-��ʣ���H+�Լ�Al3+��Ӧ�����ģ�ֻ����CO2��Ba(OH)2���ϲ�������NH4HCO3��Ӧ�����ɰ�ɫ����������BaCO3���������⣬Ҳ���ܴ���BaSO4����������ȷ��ԭ��Һ���Ƿ���CO32-��SO42-�������һ����NH4+�������Ba(OH)2��Ӧ���ɵ�NH3��
�����������϶����ڵ������У�Na+��AlO2-��S2-��SO32-��һ�������ڵ������У�Ag+��Ba2+��Fe3+�����ܴ��ڵ������У�CO32-��SO42-��
�����Ѷȣ�һ��
4������� ����Ӧ����㷺�Ľ���������±����������Լ������ĺ������ξ�Ϊ��Ҫ�����
(1)Ҫȷ������ij�Ȼ���FeClx�Ļ�ѧʽ���������ӽ����͵ζ��ķ�����ʵ���г�ȡ0.54 g��FeClx��Ʒ���ܽ���Ƚ��������ӽ���Ԥ��������ͨ�����б���OH���������ӽ�������ʹCl����OH������������������ɺ�������Һ��OH����0.40 mol��L��1������ζ��������յ�ʱ��������25.0 mL���������Ʒ���ȵ����ʵ����������FeClx��xֵ��________(�г��������)��
(2)����һ����FeCl2��FeCl3�Ļ������Ʒ�����������������n(Fe)��n(Cl)��1��2.1�������Ʒ��FeCl3�����ʵ�������Ϊ________����ʵ�����У�FeCl2�������ۺ�________��Ӧ�Ʊ���FeCl3�������ۺ�________��Ӧ�Ʊ���
(3)FeCl3������ᷴӦʱ��������ɫ���ʣ��÷�Ӧ�����ӷ���ʽΪ______��
(4)�������(K2FeO4)��һ��ǿ������������Ϊˮ��������������ز��ϡ�FeCl3��KClO��ǿ���������·�Ӧ����ȡK2FeO4���䷴Ӧ�����ӷ���ʽΪ________����MnO2��Zn������ƣ�K2FeO4��ZnҲ������ɼ��Ե�أ�K2FeO4�ڵ������Ϊ�������ϣ���缫��ӦʽΪ________���õ���ܷ�Ӧ�����ӷ���ʽΪ________��
�ο��𰸣�(1)n(Cl)��0.0250 L��0.40 mol��L��1��0.010 mol,0.54 g��0.010 mol��35.5 g��mol��1��0.185 g��n(Fe)�� ��0.0033 mol��n(Fe)��n(Cl)��0.0033��0.010��1��3��x��3
��0.0033 mol��n(Fe)��n(Cl)��0.0033��0.010��1��3��x��3
(2)0.1��HCl��Cl2
(3)2Fe3����2I��=2Fe2����I2��(4)2Fe(OH)3��4OH����3ClO��=2FeO42-��3Cl����5H2O��
FeO42-��3e����4H2O=Fe(OH)3��5OH����
3Zn��2FeO42-��8H2O=3Zn(OH)2��2Fe(OH)3��4OH��
���������(1)n(H��)��n(OH��)��n(Cl��)��0.40 mol��L��1��25.0��10��3 L��0.010 mol,0.54 g��Ʒ��m(Cl)��0.010 mol��35.5 g��mol��1��0.355 g����m(Fe)��0.54 g��0.355 g��0.185 g��n(Fe)�� ��0.0033 mol����n(Fe)��n(Cl)��0.0033��0.010��1��3������x��3��(2)���������
��0.0033 mol����n(Fe)��n(Cl)��0.0033��0.010��1��3������x��3��(2)��������� ��
�� ��0.1����������ǿ�����ԣ��ɽ���ֱ������Ϊ��3�ۣ�������������Խ�����(3)Fe3���н�ǿ�������ԣ��ܽ�I�������ɵ��ʣ���Ӧ���ӷ���ʽΪ��2Fe3����2I��=I2��2Fe2����(4)��ǿ������Һ�У�Fe3����Fe(OH)3��ʽ���ڣ�KClO����Fe(OH)3�����ᱻ��ԭΪCl������������������д����Fe(OH)3��ClO���D��FeO42-��Cl�������ݵ�ʧ�����غ���ƽ�����������ӣ�2Fe(OH)3��3ClO���D��2FeO42-��3Cl����H2O���ٽ�ϵ���غ㼰�����Ǽ��ԵĿɵõ���2Fe(OH)3��3ClO����4OH��=2FeO42-��3Cl����5H2O��K2FeO4�������ϵõ����ӱ���ԭΪFe3����FeO42-��3e����4H2O=Fe(OH)3��5OH������ع�����пת��ΪZn(OH)2�����ܷ�ӦΪ��2FeO42-��3Zn��8H2O=2Fe(OH)3��3Zn(OH)2��4OH����
��0.1����������ǿ�����ԣ��ɽ���ֱ������Ϊ��3�ۣ�������������Խ�����(3)Fe3���н�ǿ�������ԣ��ܽ�I�������ɵ��ʣ���Ӧ���ӷ���ʽΪ��2Fe3����2I��=I2��2Fe2����(4)��ǿ������Һ�У�Fe3����Fe(OH)3��ʽ���ڣ�KClO����Fe(OH)3�����ᱻ��ԭΪCl������������������д����Fe(OH)3��ClO���D��FeO42-��Cl�������ݵ�ʧ�����غ���ƽ�����������ӣ�2Fe(OH)3��3ClO���D��2FeO42-��3Cl����H2O���ٽ�ϵ���غ㼰�����Ǽ��ԵĿɵõ���2Fe(OH)3��3ClO����4OH��=2FeO42-��3Cl����5H2O��K2FeO4�������ϵõ����ӱ���ԭΪFe3����FeO42-��3e����4H2O=Fe(OH)3��5OH������ع�����пת��ΪZn(OH)2�����ܷ�ӦΪ��2FeO42-��3Zn��8H2O=2Fe(OH)3��3Zn(OH)2��4OH����
�����Ѷȣ�һ��
5��ʵ���� ��11�֣�ij������Һ���ܺ���������NO3����CO32����SO32����SO42-��Cl����Br����I����Ϊ�˼�����Щ���ӣ��ֱ�ȡ������Һ��������ʵ�飺
��������Һ�ʼ��ԣ�
�ڼ�HCl��������ɫ��ζ�����塣��������ʹ����ʯ��ˮ����ǡ�
�ۼ�CCl4���μ�������ˮ����CCl4��δ��ɫ��
�ܼ�BaCl2��Һ������ɫ���������룬�ڳ����м������������ᣬ����������ȫ�ܽ⡣
�ݼ�HNO3�ữ���ټӹ�����AgNO3����Һ��������ɫ������
(1)��������5��ʵ�� ��д��ÿһʵ��������ӵĽ��������ɡ�
��д��ÿһʵ��������ӵĽ��������ɡ�
ʵ���________________________________________��
ʵ���_______________________________________��
ʵ���____ ____________________________________��
____________________________________��
ʵ���________________________________________��
ʵ���________________________________________��
(2)����5��ʵ�鲻��ȷ���Ƿ��������___________________��
�ο��𰸣�

�����������
�����Ѷȣ�һ��