1��ѡ���� ��֪�����£�Ksp��Mg(OH)2����1.2��10-11mol3��L-3��Ksp(AgCl)��1.8��10-10mol2��L-2 Ksp(Ag2CrO4)��
1.9��10-12 mol3��L-3��Ksp(CH3COOAg)��2.3��10-3mol2��L-2����������ȷ����
[? ]
A����������Ũ�Ⱦ�Ϊ0.2 mol��L-1��AgNO3��Һ��CH3COONa��Һһ������CH3COOAg����
B����0.001 mol��L-1��AgNO3��Һ����0.001 mol��L-1��KCl��0.001 mol��L-1��K2CrO4��Һ���Ȳ���Ag2CrO4����
C����Mg2+Ϊ0.121 mol��L-1����Һ��Ҫ����Mg(OH)2��������Һ��pH����Ҫ������9����
D����AgClˮ��Һ�м���NaCl��Һ��Ksp(AgCl)���
�ο��𰸣�AC
���������
�����Ѷȣ�һ��
2��ѡ���� �����й����ʵ����ʻ�Ӧ��˵����ȷ���ǣ�������
A�����ࡢ��֬����������һ�������¾�����ˮ��
B��ҽ���Ͽ���BaCO3��X�����ӳ�θ���ڷ�ҩ��
C���Ӻ�ˮ�еõ��Ȼ�þ���壬����Ȼ�þ����ɻ�ý���Mg
D����¯ˮ���к��е�CaSO4��������Na2CO3��Һ�������������ȥ
�ο��𰸣�A������ֵ��ǡ����ǺͶ��ǣ����Dz�ˮ�⣬���ǡ����ǡ���֬����������һ�������¾�����ˮ�⣬��A����
B��̼�ᱵ�������Σ��ܺ����ᷴӦ�������ᱵ�Ȳ����ᷴӦҲ���ͼӦ������ҽ���Ͽ���BaSO4��X�����ӳ�θ���ڷ�ҩ������B����
C��þ�ǻ��ý���������þ��ұ�������ǵ���Ȼ�þ���������ǵ������̬���Ȼ�þ�����Ȼ�þ���壬��C����
D������������Ե����ʣ��ܺ�̼���Ʒ�Ӧ���������Ե�̼��ƣ�̼��ƺ������ܷ�Ӧ�����Թ�¯ˮ���к��е�CaSO4��������Na2CO3��Һ�������������ȥ����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
3��ѡ���� ��һ�����������У�����Ca��OH��2����Һ����ƽ�⣺Ca��OH��2��s��?Ca2+��aq��+2OH-��aq����H��0����֪��CaO��s��+H2O��l���TCa��OH��2��s����H��0������˵����ȷ���ǣ�������
A������Һ�м�����CaO������ƽ�����Һ��pH����
B������Һ�м�����CaO������ƽ�����Һ��pH����
C������Һ�м���Na2CO3��Һ������Ca��OH��2������������
D������Һ�м�������NaOH���壬Ca��OH��2������������
�ο��𰸣�A����ʯ��ˮ�м�������ʯ�Һ�����ˮ����Һ���¶�Ҳ���ߣ��������Ƶ��ܽ�������¶ȵ����߶����ͣ���Һ������������Ũ��ԽС����Һ��pHԽС����A����
B����ʯ��ˮ�м�������ʯ�Һ�����ˮ����Һ���¶�Ҳ���ߣ��������Ƶ��ܶȻ�ԽС������Һ������������Ũ��ԽС����Һ��pHԽС����B��ȷ��
C������Һ�м���Na2CO3��Һ�������Ӻ�̼��������γ�̼��Ƴ�����Ca��OH��2��s��?Ca2+��aq��+2OH-��aq����H��0��ƽ��������У�����Ca��OH��2����������С����C����
D������Һ�м�������NaOH���壬��Һ������������Ũ������Ca��OH��2��s��?Ca2+��aq��+2OH-��aq����H��0��ƽ��������У�Ca��OH��2������������D����
��ѡB��
���������
�����Ѷȣ���
4��ѡ���� ��֪ͬ�¶��µ��ܽ�ȣ�Zn(OH)2��ZnS��MgCO3��Mg(OH)2�����ܽ������S2�����������ԣ�FeS��H2S��CuS�����������ӷ���ʽ������ǣ�?��
A��Mg2����2HCO3-��2Ca2����4OH��=Mg(OH)2����2CaCO3����2H2O
B��Cu2����H2S=CuS����2H��
C��Zn2����S2����2H2O=Zn(OH)2����H2S��
D��FeS��2H��=Fe2����H2S��
�ο��𰸣�C
�����������ΪMgCO3���ܽ�ȴ���Mg(OH)2�ģ����Ի��γ�Mg(OH)2��A��ȷ��H2S��������S2������������CuS�ģ�С��FeS�ģ�����H2S��Cu2����Ӧ���ɸ��ѵ����CuS��FeS��H����Ӧ���ɸ��ѵ����H2S��B��D��ȷ�����ܽ��Zn(OH)2��ZnS����֪Ӧ���������ܵ�ZnS��C����
�����Ѷȣ���
5������� (16��)������һ����Ҫ�Ļ�����Ʒ����ҵԭ�ϡ�
I��ij�¶��£��ϳɰ���Ӧ��ƽ�ⳣ��K=3.0��103(mol��L)-1��
��1��д�����Ӧ�Ļ�ѧ����ʽ____________________________________________________ ��
��2��ij�¶��£����������㶨Ϊ10L���ܱ������г��룺0.1molN2��0.1molH2��2molNH3��Ӧ_______(�������С���������С��ﵽƽ�⡱)��
��3�����¶��£�������㶨Ϊ10L���ĸ��ܱ������зֱ�����������ʣ���Ӧ�ﵽƽ���N2��ת����������___________________��
a��10molN2��30molH2��20molNH3 b��10molN2��30molH2
c��20molN2��60molH2 d��10molN2��28molH2
II��������������ˮ����ˮ�ǰ�������ˮ���γɵ���Һ,�ش��������⣺
��4���ڰ�ˮ��Һ�м�ˮϡ�͵Ĺ��̣�NH3��H2O�ĵ���̶�___________(�������С�����䡱)��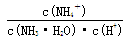 ___________��ͬ�ϣ���
___________��ͬ�ϣ���
��5�������£�a mol/L��(NH4)2SO4ˮ��Һ��pH=5��ԭ������Һ�д���ƽ��________________________(�����ӷ���ʽ��ʾ)���������ƽ���ƽ�ⳣ������ʽΪ________________________(�ú�����a�Ľ�Ϊ��ȷ����ѧ����ʽ��ʾ�����ػ�������������)��
��6�������£���Ũ�Ⱦ�Ϊ0.1mol/L��MgCl2��CuCl2�����Һ����μ��백ˮ��������__________����(�ѧʽ)�����ɸó��������ӷ���ʽΪ_________________________________________��
(��֪������ʱ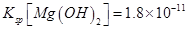 mol3
mol3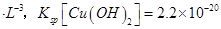 mol3.L-3).
mol3.L-3).
�ο��𰸣��� ��1��1/2 N2 + 3/2 H2 NH3��2�֣� ��2��������У�2�֣� ��3��c��2�֣�
NH3��2�֣� ��2��������У�2�֣� ��3��c��2�֣�
��4������1�֣� ���� ��2�֣�
��5��NH4++H2O NH3?H2O+H+��2�֣� 10-5(10-5-10-9)/2a+10-9-10-5 mol��L-1��2�֣�
NH3?H2O+H+��2�֣� 10-5(10-5-10-9)/2a+10-9-10-5 mol��L-1��2�֣�
��6��Cu(OH)2��1�֣� Cu2++2NH3��H2O=Cu(OH)2 ��+2NH4+��2�֣�
�����������1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�������ƽ�ⳣ����֪��Ӧ�Ļ�ѧ����ʽΪ1/2 N2 + 3/2 H2 NH3��
NH3��
��2��������㶨Ϊ10L���ܱ������г��룺0.1molN2��0.1molH2��2molNH3�����Ũ����Ϊ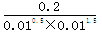 ��2000��3000�����Է�Ӧ������Ӧ������С�
��2000��3000�����Է�Ӧ������Ӧ������С�
��3��a��b��ȣ�a�к��д����İ��������b�а�����ת���ʴ���a�С�b��d��ȣ�b������Ũ�ȴ�ת���ʸߣ���������Ӧ�������С�Ŀ��淴Ӧ����������ѹǿƽ��������Ӧ������У�c��b��ȣ��൱������b�Ļ���������ѹǿ������ת��������ѡc��
��4��ϡ�ʹٽ���ˮ�ĵ��룬����̶�����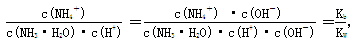 ����˱�ֵ���䡣
����˱�ֵ���䡣
��5��笠�ˮ����Һ�����ԣ�����ʽΪNH4++H2O NH3?H2O+H+�������£���a mol?L-1�ģ�NH4��2SO4ˮ��Һ��pH=5����Һ��c��H+��=10-5mol/L������Һ��c��OH-��=10-9mol/L�����ݵ���غ��У�c��NH4+��+c��H+��=c��OH-��+2c��SO42-������c��NH4+��+10-5mol/L=10-9mol/L+2amol/L����c��NH4+��=��2a+10-9-10-5��mol/L�����������غ������Һ��c��NH3?H2O��=2amol/L-��2a+10-9-10-5��mol/L=��10-5-10-9��mol/L����NH4++H2O
NH3?H2O+H+�������£���a mol?L-1�ģ�NH4��2SO4ˮ��Һ��pH=5����Һ��c��H+��=10-5mol/L������Һ��c��OH-��=10-9mol/L�����ݵ���غ��У�c��NH4+��+c��H+��=c��OH-��+2c��SO42-������c��NH4+��+10-5mol/L=10-9mol/L+2amol/L����c��NH4+��=��2a+10-9-10-5��mol/L�����������غ������Һ��c��NH3?H2O��=2amol/L-��2a+10-9-10-5��mol/L=��10-5-10-9��mol/L����NH4++H2O NH3?H2O+H+��ƽ�ⳣ���ı���ʽΪ
NH3?H2O+H+��ƽ�ⳣ���ı���ʽΪ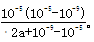 ��
��
��6���ܶȻ�����ԽС������Խ�ȳ�����������ͭ���ܶȻ�С��������þ���ܶȻ�������������ͭ�ȳ�����ͭ���ӺͰ�ˮ��Ӧ����������ͭ������笠����ӣ����ӷ���ʽΪCu2++2NH3?H2O��Cu��OH��2��+2NH4+��
���㣺����ƽ�ⳣ��������Ӧ�á���������Ե���ƽ���Ӱ�졢����ˮ���Լ��ܶȻ�����Ӧ�õ�
�����Ѷȣ�����