1��ѡ���� ij�¶��£���֪Ksp(AgCl)=1.56��10��10��Ksp(AgBr)=7.7��10��13��Ksp(Ag2CrO4)=9.0��10��12��ij��Һ�к���Cl����Br����CrO42����Ũ�Ⱦ�Ϊ0.010 mol/L�������Һ����μ���0.010 mol/L��AgNO3��Һʱ�����������Ӳ����������Ⱥ�˳��Ϊ
A��Cl����Br����CrO42��
B��CrO42����Br����Cl��
C��Br����Cl����CrO42��
D��Br����CrO42����Cl��
�ο��𰸣�C
����������� 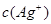 ��
��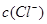 �Ļ�����1.56��10��10�г�������
�Ļ�����1.56��10��10�г�������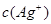 ��
��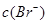 �Ļ�����7.7��10��13��ʱ�г�������
�Ļ�����7.7��10��13��ʱ�г�������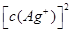 ��
�� �Ļ�����9.0��10��12ʱ�г�������ΪCl����Br����CrO42����Ũ����ȣ����Բ���������˳��ΪBr����Cl����CrO42������C��ȷ��sp��
�Ļ�����9.0��10��12ʱ�г�������ΪCl����Br����CrO42����Ũ����ȣ����Բ���������˳��ΪBr����Cl����CrO42������C��ȷ��sp��
�����Ѷȣ���
2��ѡ���� ����˵������ȷ����
[? ]
A�������¶ȣ�һ��Ũ�ȵĴ�����Һ�д���ĵ���ƽ�ⳣ���������Ǵ���ӷ���
B�����������ˮ��̼���������ˮ���ɴ���֪Ksp(CaCO3)>Ksp(CaS O4)
C����֪25��ʱKsp[Fe(OH)3]=4.0��10-36����������Һ��Fe3+�����ڣ���������ָ����Ũ��С��1��10-5 mol��L-1��
D��������þ����Һ�л��������������ƣ����������м��������Ȼ�þ��Һ��ֽ��衢���ˡ�ϴ�ӵõ�������þ
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3��ѡ���� ����˵����ȷ���ǣ�������
A�������ܵ�������Ƚ�ʱ��KspС�ģ��ܽ��һ��С
B����ʹ��Һ��ij���ӳ�����ȫ������ij�����Ӧ����Խ��Խ��
C����ν������ȫ�����ó���������Һ��ijһ���ӳ���
D����ʹCa2+���ӳ�������ȫ��ѡ��Na2CO3��������Ч����Na2SO4��
�ο��𰸣�A��ֻ�о�����ͬ�ṹ���������AgCl��AgBr��AgI��KspС���ܽ��С������ͬ�ṹ�ģ���Ag2SO4��AgI��KspС���ܽ�Ȳ�һ��С����A����
B��������ͬ����ЧӦ����������˵������������Խ�࣬���������Ӿ�Խ��ȫ������������������ЧӦ����ЧӦ����λЧӦ��������ЧӦ����ٽ������ܽ⣬��������λЧӦ��������ʹ������ȫ�ܽ⣬���Գ��������������Ǽӵ�Խ��Խ�ã������ʵ������Ϳ����ˣ���B����
C�����ܵ��������Һ�д����ܽ�ƽ�⣬�����ܼ������������Һ��ijһ���ӳ�������C����
D��̼��Ƶ��ܽ�ȱ������С������ʹCa2+���ӳ�������ȫ��ѡ��Na2CO3��������Ч����Na2SO4�ã���D��ȷ��
��ѡD��
���������
�����Ѷȣ���
4��ѡ���� �Ȼ�����ˮ�д��ڳ����ܽ�ƽ�⣬25��ʱ���Ȼ�����Ksp=1.8��10-10���ֽ������Ȼ����ֱ���룺��5mL����ˮ�У���20mL0.2mol?L-1MgCl2�У���10mL0.5mol?L-1NaCl��Һ�У���ֽ��������ͬ�¶��£�c��Ag+���ɴ�С��˳���ǣ�������
A���٢ڢ�
B���ۢڢ�
C���ڢ٢�
D���ڢۢ�
�ο��𰸣���AgCl������Һ�д��ڳ����ܽ�ƽ�⣺AgCl��s���TAg+��aq��+Cl-��aq��������Cl-ƽ�������ƶ����Ȼ����ܽ�ȼ�С������Cl-��Ũ��Խ���Ȼ����ܽ��ԽС����ͬ������Ag+ƽ�������ƶ����Ȼ����ܽ�ȼ�С������Ag+��Ũ��Խ���Ȼ����ܽ��ԽС��c��Ag+����c��Cl-����ƽ���Ӱ���ǵ�Ч�ģ�5mL����ˮ��û��Cl-��Ag+����֪����Cl-��Ag+Ũ�ȴӴ�С˳��Ϊ���ۢڢ٣����Ȼ����ܽ�ȴӴ�С˳���෴Ϊ���٢ڢۣ���A��ȷ��
��ѡ��A��
���������
�����Ѷȣ�һ��
5��ѡ���� ij�¶�ʱ��AgCl��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ����
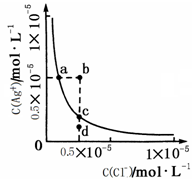
A������NaCl����ʹ��Һ��a��䵽b��
B����AgCl������Һ�м���ˮ�� C(Ag+)����
C��d����AgCl��������
D��a���Ӧ��Ksp����c���Ӧ��Ksp
�ο��𰸣�C
�����������AgCl��ˮ�еij����ܽ�ƽ�ⷽ��ʽΪ��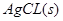 ?
?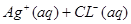 ������
������
A��������NaCl����Һ��������Ũ���������ܽ�ƽ�����淴Ӧ�����ƶ�����Һ�е�������Ũ�ȼ�С��B����������Һ�м���ˮ����ʱ��Ȼ�DZ�����Һ����Һ�и�����Ũ�Ȳ��䣻C��ȷ����Һ��Ũ�Ȼ�С���ܶȻ������ڲ�����״̬��D�����ܶȻ����¶�Ӱ�������������أ�
�����Ѷȣ�һ��