1、选择题 下列关于化工生产原理的叙述中,均符合目前工业生产实际的是
A.氯碱工业中,氢氧化钠在电解槽的阴极区产生
B.氯气和氢气混合在光照条件下生成氯化氢,用水吸收得到盐酸
C.二氧化硫在接触室被氧化成三氧化硫,三氧化硫在吸收塔内被水吸收制成浓硫酸
D.合成氨工业中,利用氨易液化,分离出N2、H2循环使用,总体上提高了氨的产率
参考答案:AD
本题解析:A、电解氯化钠溶液,正确;B、氯气和氢气混合在光照条件下会爆炸,危险,错误;C、三氧化硫在吸收塔内被水吸收制成浓硫酸,易形成酸雾,错误;D、合成氨是可逆反应,有平衡,正确。
本题难度:一般
2、选择题 下列关于钢铁冶炼的说法错误的是:
参考答案:B
本题解析:略
本题难度:一般
3、填空题 【化学一选修2化学与技术】(15分)
已知:①工业上用硫酸与锂辉矿(LiA1Si2O6和少量钙镁杂质)反应,生成Li2SO4、MgSO4等,最终制备金属锂。
②氢氧化锂在一定温度下可转化为氧化锂。用β锂辉矿与硫酸等物质制备金属锂的工业流程如下:
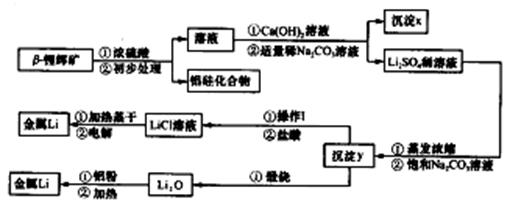
请回答:(1)沉淀y的主要成分的化学式是?。
(2)流程中使用了不同浓度的Na2CO3溶液,从物质溶解度大小的角度解释其浓度不同的原因是?。
(3)操作I涉及的实验方法是?。
(4)写出用铝粉还原法制取金属锂的化学方程式?。
(5)LiCl溶液加热蒸干后,所得固体在熔融状态下电解制备锂。电解时产生的氯气中混有少量氧气,产生氧气的原因是?。
(6)目前电池通常使用金属锂的优点是???。
参考答案:(1)Li2CO3(2分)
(2)加稀Na2CO3溶液既能除去溶液中的Ca2+,又不生成Li2CO3沉淀;(2分)
加饱和Na2CO3溶液的目的是使Li +转化生成Li2CO3沉淀。(1分)(其他合理答案参照给分)
(3)过滤、洗涤(各1分)
(4)3 Li2O +4Al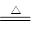 2 Al2O3+3Li (3分)
2 Al2O3+3Li (3分)
(5)LiCl溶液在加热蒸干过程中有部分LiOH生成,LiOH受热分解为Li2O,熔融的Li2O电解生成氧气。(3分)
(6)锂的密度小,质能比高;锂电池为可充电绿色环保电池。(2分,其它合理答案也给分)
本题解析:(1)硫酸锂和碳酸钠反应的生成物是硫酸钠和碳酸锂,根据Y灼烧的产物是氧化锂可知,Y是碳酸锂。
(2)第一次用稀碳酸钠溶液,是为了防止生成碳酸锂,同时又可以除去钙离子。而第二次是为了生成碳酸锂,所以浓度要大。
(3)从溶液中分离出固体的方法应是过滤,过滤后晶体必须洗涤。
(4)在加热的条件下,铝可以发生铝热反应,方程式为3 Li2O +4Al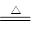 2 Al2O3+3Li。
2 Al2O3+3Li。
(5)电解池中氯离子在阳极放电,有氧气生成,说明氧离子在阳极也放电,这是由于LiCl溶液在加热蒸干过程中有部分LiOH生成,LiOH受热分解为Li2O,熔融的Li2O电解生成氧气。
6)锂的密度小,质能比高;锂电池为可充电绿色环保电池。
本题难度:一般
4、选择题 下列符合化学实验“绿色化学”的有( )
①在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水
②在铜和浓硝酸反应的实验中,将铜片改为可调节高度的铜丝
③将实验室的废酸液和废碱液中和后再排放.
A.①②
B.①③
C.②③
D.①②③
参考答案:D
本题解析:
本题难度:一般
5、填空题 太湖、巢湖、滇池是我国重点治理的三大湖,三大湖受到严重的富营养化污染,藻类疯狂繁殖,破坏了生态平衡,影响了人民的健康,必须迅速进行治理。请回答:
(1)藻类的狂长,说明水中哪些元素超标??这些元素从哪里引入的??
(2)您认为引起藻类大量繁殖最主要的是哪一种元素??以什么形态出现??请你设计一个测定此元素的方法。
(3)水质污染程度的重要标志之一为BOD(生物化学耗氧量),它是指由于水中微生物的繁殖或呼吸作用,或水中有机物分解时所消耗的溶解氧的量,单位为mgO2/L。现有巢湖沿岸某电镀厂,不遵守环境法规,每周向湖中排放一次含氰废水,使近岸湖水含CN-的浓度为7.5×10-5mol/L,CN-与O2作用生成CO2、N2等。试问此电镀厂每排放一次废水将使近岸湖水的BOD增大多少?
(4)水质污染程度的另一重要指标为COD(化学耗氧量),它是指水中还原性物质(有机的和无机的),在规定条件下被氧化时,1L水样所消耗的氧的毫克数。测定COD通常有KMnO4法、K2Cr2C7法等。酸性KMnO4法:KMnO4在酸性溶液中经沸水浴加热,将发生:
2KMnO4+3H2SO4==K2SO4+2MnSO4+3H2O+5[O]。
①若为0.01000mol/L KMnO4溶液,则1.00mL相当于?mgO2;
②若巢湖水样100mL,加入1:2 H2SO410mL,AgSO41g,混匀后,又加10mL 0.01000mol/L KMnO4溶液,在沸水中加热30min,取出加入10mL 0.02500mol/L Na2C2O4溶液,立即用0.01000mol/L KMnO4滴至微红色在15秒内不变色为终点,耗KMnO4液7.00mL,求巢湖水样的COD为多少?
参考答案:(1)N? P(2) N(3)BOD=3.0mgO2・dm-3(4)COD=28 mgO2・dm-3
本题解析:(1)藻类的狂长,主要是 N、P等元素含量超标。(1分)
这些元素,主要因氮肥、复合肥、农药的过量施用,流失到巢湖中造成污染。(2分)
(2)引起藻类大量繁殖的最主要元素是N,它以氨氮,即NH3或NH4+形态进入湖水中。测定氮量的方法:把水样碱化,将氨蒸出,用过量的硫酸标准液(或硼酸标准液)吸收,然后以氢氧化钠滴定剩余的硫酸(或用盐酸滴定(NH4)2B4O7)。(4分)
(3)4CN-+5O2+2H2O==4CO2+2N2+4OH- (H+参加反应代替水也可以)?
BOD=1.25×7.5×10-5×3.2×104=3.0mgO2・dm-3?(4分)
(4)① 0.40
KMnO4~2.5[O]~1.25O2?
② 2MnO4-+5C2O42-+16H+==2Mn2++10CO2↑+8H2O
Na2C2O4共消耗KMnO4 V=0.02500×10×0.4/0.01000=10.0cm3
与水中还原性物质反应的KMnO4为7.0cm3?
COD=0.40×7.0/0.1=28 mgO2・dm-3
本题难度:简单