1、填空题 (共8分) A、B、C、D四种可溶性盐,它们的阳离子分别可能是Ba2+、Ag+、
Na+、Cu2+中的某一种,阴离子分别可能是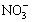 、S
、S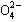 、Cl―、C
、Cl―、C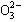 的某一种。
的某一种。
(1)若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色。
(2)若向(1)的四支试管中分别加盐酸,B盐溶液有沉淀产生,D盐溶液有无色无味气体逸出。
根据(1) 、(2)实验事实可推断它们的化学式为:
A.??B.??C.??D.??
参考答案:(8分)? BaCl2?AgNO3?CuSO4?Na2CO3
本题解析:略
本题难度:简单
2、选择题 0.5mol Na2SO4中含有Na+数目是
A.3.01x1023
B.6.02x1023
C.0.5
D.1
参考答案:B
本题解析:试题分析:0.5mol Na2SO4中钠离子的物质的量为0.5mol×2=1mol,
则由N=n×NA可知,
则钠离子的个数为1mol×NAmol-1=NA≈6.02×1023,
故选B。
考点:阿伏加德罗常数 电解质在水溶液中的电离
点评:有关阿伏伽德罗常数的计算,题目在注重对计算关系的考查的同时,又隐含对物质状态、物质结构、氧化还原反应、电离、水解知识的考查。
本题难度:一般
3、填空题 某化学兴趣小组利用某废弃的氧化铜锌矿制取活性ZnO实验流程如下:

请回答下列问题:
(1)加入铁粉后发生反应的离子方程式为__________。
(2)甲、乙两同学选用下列仪器,采用不同的方法来制取氨气。
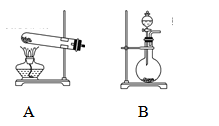
①甲同学使用的药品是熟石灰与氯化铵,则应选用装置______(填写装置代号),生成氨气的化学方程式为____________;
②乙同学选用了装置B,则使用的两种药品的名称为_______________。
(3)H2O2的作用是_____________。
(4)除铁过程中得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂(K2FeO4),该反应中氧化剂与还原剂的物质的量之比为____________。
(5)乙知溶液a中含有CO32-、SO42-两种酸根阴离子,若只允许取用一次样品,检验这种离子存在的实验操作过程为___________________。
参考答案:
(1)Fe+Cu2+= Fe2++Cu
(2)A?浓氨水和碱石灰(或生石灰或氢氧化钠固体)
(3)将Fe2+氧化成Fe3+
(4)3:2
(5)取少量溶液a于试管中,滴加稍过量的盐酸,有无色气泡产生,则说明有CO32-,继续滴加氯化钡溶液,产生白色沉淀,说明有SO42-
本题解析:该试题是制ZnO,第一步加入稀硫酸酸溶,矿物质溶解生成Zn2+、Cu2+;第二步加入还原性铁粉后,过滤,Cu2+被还原出来,同时溶液中增加了Fe2+;第三步加入绿色氧化剂H2O2,把Fe2+氧化成Fe3+,通入氨水调节溶液的pH,使Fe3+转化为Fe(OH)3;第四步,再次通入氨气,加入NH4HCO3,使溶液中Zn2+生成碱式碳酸锌,过滤,焙烧,就可以得到活性ZnO。分析出工艺流程用意,是解答本题的关键。第(4)问要利用价态守恒去做,氧化剂与还原剂的物质的量之比等于它们1mol得到、失去电子的反比;至于第(5)问,要注意的是“一次”的含意,正确选择试剂和设计检验的步骤,本题具有开放性,只要合理就行。
本题难度:困难
4、选择题 下列各组物质仅用水就能鉴别的是
①NO2和Br2蒸气?②硝基苯和苯?③固体NaOH和KNO3.
A.①②
B.②③
C.①③
D.①②③
参考答案:D
本题解析:分析:①根据二氧化氮和水反应以及溴蒸气溶于水分析;
②根据硝基苯不溶于水密度比水大以及苯不溶于水且密度比水小分析;
③根据氢氧化钠溶于水放热和硝酸钾溶于水吸热分析.
解答:①二氧化氮和溴蒸气都是红棕色气体,二氧化氮与水反应生成硝酸和无色的一氧化氮气体,而溴蒸气溶于水,溶液颜色为橙红色,二者现象不同,故可鉴别;
②硝基苯不溶于水密度比水大,油状液体在下层,苯不溶于水密度比水小,油状液体在上层,二者现象不同,可鉴别;
③氢氧化钠溶于水放热,硝酸钾溶于水吸热,二者溶于水后烧杯的温度不同,故可鉴别.
故①②③都可鉴别.
故选D.
点评:本题考查物质的鉴别,分别涉及物质的化学性质和物理性质,题目难度不大,注意物质的性质的区别.
本题难度:一般
5、选择题 除去括号内杂质所用试剂和方法,正确的是
A.乙醇(乙酸)生石灰过滤
B.乙醇(乙醛)通入水蒸汽催化加热
C.乙酸乙酯(乙酸)碳酸钠溶液分液
D.乙酸(乙醛)通入O2气常温常压
参考答案:C
本题解析:A错,乙醇(乙酸)?生石灰?蒸馏;B错,乙醛与乙醇均易挥发;C正确;D错,常温下乙醛与氧气不反应,需加热才能反应;
本题难度:一般