?
参考答案:(20分)(1)MnO2?MnCO3(每个2分)
(2)5Mn2++2ClO3-+4H2O=5MnO2↓+Cl2↑+8H+( 4分,补充物质全对给2分,配平2分), 4分,补充物质全对给2分,配平2分),
(3)蒸发皿?酒精灯(4分);?
(4)0.05(4分);
(5)①放热(2分),②图略(2分)
本题解析:略
本题难度:一般
2、选择题 下列有关物质分离提纯方法的说法中正确的是( )
①过滤--适用于不溶性固体和液体的分离
②蒸馏--适用于互溶性且沸点相差较大的液体的分离
③分液--适用于不溶性液体的分离
④纸上层析--适用于用一般的化学方法分离十分困难的分子或离子混合溶液的分离.
A.①②③
B.①③④
C.②③④
D.①②③④
参考答案:①不溶性固体和液体的分离用过滤,故①正确;
②互溶性且沸点相差较大的液体的分离用蒸馏,故②正确;
③不溶性液体的分离用分液,故③正确;
④对于一般的化学方法分离十分困难的分子或离子混合溶液的分离用纸上层析,故④正确;
故选D.
本题解析:
本题难度:简单
3、实验题 一定浓度NaHCO3溶液与CuSO4溶液反应后生成了蓝绿色颗粒状沉淀。就沉淀成分提出了如下三种假设:
假设一:沉淀是CuCO3;假设二:沉淀是Cu(OH)2;
假设三:沉淀是CuCO3和Cu(OH)2的混合物。
(1)写出假设二,沉淀是Cu(OH)2生成的理由??(用离子方程式表示);
(2)为了探究沉淀的成分,取出了一部分沉淀,滴加稀盐酸,有气体放出。凭此现象,判断沉淀中含有?;
(3)为了进一步探究沉淀的成分,进而确定假设中何种假设成立,设计实验,装置图如下:
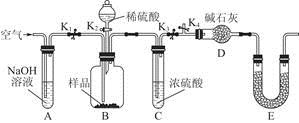
①研究沉淀物组成前,须将沉淀从溶液中分离并净化。具体操作依次为??、洗涤、干燥;
②装置E中药品的名称是?作用为?;
③实验过程中有以下操作步骤:a.打开K1、K3,关闭K2、K4,通入过量空气。此步骤的作用是?。
b.关闭K1、K3,打开K2、K4,充分反应,c.再通入过量空气时,活塞处于打开的是?,关闭的是?。
④若沉淀样品的质量为m g,装置D的质量增加了n g;若沉淀样品为纯净物,m、 n之间的关系为?。
若假设三成立,则Cu(OH)2的质量分数为?;若不进行步骤c,则会使测得结果?(填“偏高”“无影响”“偏低”)。
参考答案:(1)Cu2++2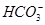 =Cu (OH)2↓+2CO2↑(2)CuCO3 =Cu (OH)2↓+2CO2↑(2)CuCO3
(3)①过滤 ②碱石灰 防止空气中的水蒸气和CO2进入装置D
③排除整套装置中的CO2,使测得结果更准确 K1、K4 K2、K3
④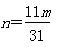 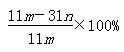 偏低 偏低
本题解析:(1)Cu2+和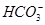 的水解相互促进,可以生成Cu(OH)2沉淀和CO2气体;(2)CuCO3可以和稀盐酸反应生成CO2气体而Cu(OH)2与稀盐酸的反应中没有气体生成;(3)①分离不溶性固体与液体的操作为过滤;②CO2和H2O会影响实验结果的准确性,所以应避免空气中的水蒸气和CO2进入装置D,可以用碱石灰吸收;③a.实验装置中的CO2会影响实验结果的准确性,故应在反应前排除;b.再通入过量空气的目的是将装置中残余的气体赶入D中充分吸收;④若沉淀样品为纯净物,装置D质量增加则沉淀为CuCO3,其物质的量与生成CO2的物质的量相等,故 的水解相互促进,可以生成Cu(OH)2沉淀和CO2气体;(2)CuCO3可以和稀盐酸反应生成CO2气体而Cu(OH)2与稀盐酸的反应中没有气体生成;(3)①分离不溶性固体与液体的操作为过滤;②CO2和H2O会影响实验结果的准确性,所以应避免空气中的水蒸气和CO2进入装置D,可以用碱石灰吸收;③a.实验装置中的CO2会影响实验结果的准确性,故应在反应前排除;b.再通入过量空气的目的是将装置中残余的气体赶入D中充分吸收;④若沉淀样品为纯净物,装置D质量增加则沉淀为CuCO3,其物质的量与生成CO2的物质的量相等,故
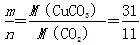 ;若沉淀是CuCO3和Cu(OH)2的混合物,则 ;若沉淀是CuCO3和Cu(OH)2的混合物,则
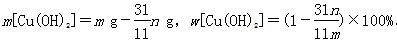
本题难度:一般
4、填空题 【10分】取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的化学方程式为___________,
反应后得到的FeCl3溶液呈棕黄色。用此溶液进行以下实验:
(1)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为__________________,此反应属于_________反应。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈_________色,即可制得Fe(OH)3胶体。
(3)取另一小烧杯也加入20 mL蒸馏水后,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置暗处:分别用激光笔照射烧杯中的液体,可以看到_________烧杯中的液体会产生丁达尔效应。这个实验可用来区别_________。
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,可看到溶液红褐色逐渐变浅,最终又得到黄色的FeCl3溶液,发生此变化的化学方程式为____
_________________________,此反应也属于________________反应。
参考答案:Fe2O3+6HCl====2FeCl3+3H2O
(1)FeCl3+3NaOH====Fe(OH)3↓+3NaCl?复分解
(2)红褐? (3)乙?胶体和溶液
(4)Fe(OH)3+3HCl====FeCl3+3H2O复分解
本题解析:本题考查Fe(OH)3胶体的制备及性质。
Fe2O3粉末(红棕色)加入适量盐酸,反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O
(1)?在FeCl3溶液滴入NaOH溶液,反应的化学方程式为:FeCl3+3NaOH=Fe(OH)3↓+3NaCl?
此反应属于复分解反应
(2)?溶液呈红褐色,这是Fe(OH)3胶体的颜色
(3)?可以看到乙烧杯中的液体会产生丁达尔效应,这个实验可用来区别胶体和溶液
(4)?此变化的化学方程式为:Fe(OH)3+3HCl=FeCl3+3H2O?此反应也属于复分解反应。
本题难度:简单
5、选择题 下列选项操作错误或不能达到实验目的的是
A.可用25ml酸式滴定管量取20.00ml KMnO4溶液
B.从碘水中提取单质碘,不能用无水乙醇代替CCl4
C.石蕊试纸和PH试纸使用前用蒸馏水润湿
D.CO2中混有少量SO2,除杂试剂和方法为:KMnO4(H+)、浓硫酸,洗气
参考答案:C
本题解析:A.KMnO4溶液有强氧化性,容易腐蚀橡胶管,因此可用25ml酸式滴定管量取20.00ml KMnO4溶液。正确。B.由于乙醇与水互溶,所以从碘水中提取单质碘,不能用无水乙醇代替CCl4。正确。C.若使用石蕊试纸和PH试纸检验气体,则在使用前必须用蒸馏水润湿;若是检验溶液的pH或酸碱性,则不能湿润。错误。D.由于SO2有还原性,能够与酸性KMnO4溶液发生反应而被氧化为硫酸,因此CO2中混有少量SO2,除杂试剂和方法为:KMnO4(H+)、浓硫酸,洗气。正确。
本题难度:一般
|