1、选择题 下列常见金属的冶炼原理中不合理的是(?)
?
2、选择题 下列物质属于硅酸盐材料的是
[? ]
A.碳纤维
B.石灰石
C.普通水泥
D.石英玻璃
3、选择题 要使3.2 g氧化铁完全还原,事先应准备的CO在标准状况下的体积为( )。
A.1 344 mL
B.672 mL
C.大于1 344 mL
D.小于672 mL
4、选择题 阅读下列材料,回答有关问题。
锡、铅两种元素的主要化合价是+2价和+4价,其中+2价锡元素和+4价铅元素的化合物均是不稳定的,+2价锡离子有强还原性,+4价铅元素的化合物有强氧化性。例如:Sn2+还原性比Fe2+还原性强。PbO2的氧化性比Cl2氧化性强。
(1)写出下列反应的化学方程式:
①氯气跟锡共热:_____________________________________________________________;
②氯气跟铅共热:_____________________________________________________________;
③二氧化铅跟浓盐酸共热:_____________________________________________________。
(2)能说明Sn2+还原性比Fe2+还原性强的离子方程式是___________________________。
5、填空题 锰锌铁氧体可用于隐形飞机上吸收雷达波涂料。现以废旧锌锰电池为原料制备锰锌铁氧体的主要流程如下:

(1)酸浸时,二氧化锰被双氧水还原的化学方程式为_______。
(2)活性铁粉除汞时,铁粉的作用是______ (填“氧化剂”或“还原剂”或“吸附剂”)。
(3)除汞是以氮气为载气吹入滤液带出汞蒸汽经KMnO4溶液进行吸收而实现的。如下图是KMnO4溶液处于不同pH时对应的Hg去除率变化图,图中物质为Hg与 MnO4-在该pH范围内的主要产物。
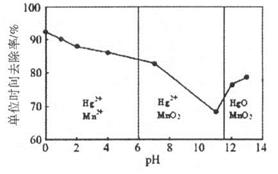
①请根据该图给出pH对汞去除率影响的变化规律:______。
②试猜想在强酸性环境下汞的单位时间去除率高的原因:______。
(4)当x=0.2时,所得到的锰锌铁氧体对雷达波的吸收能力特别强,试用氧化物的形式表示该铁氧体组成____________。
(5)经测定滤液成分后同时加入一定量的MnSO4和铁粉的目的是______。