|
|
|
高中化学知识点总结《盐类水解的原理》考点巩固(2017年最新版)(九)
2018-03-17 06:57:02
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、填空题 聚合铝(PAC)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铝灰、铝土矿、铝渣等为原料(主要成分为Al、Al2O3)可制取聚合铝。实验步骤如下:

聚合过程主要利用了Al3+的性质是 。
2、选择题 下列说法正确的是:
A.常温下醋酸分子不可能存在于pH>7的碱性溶液中
B.在0.1mol/LNa2SO3的溶液中加入少量NaOH固体,c(Na+)增大,c(SO32
|
3、填空题 (6分)
(1)下列化学原理的应用,主要用沉淀溶解平衡原理来解释的是 :
①热纯碱溶液洗涤油污的能力比冷纯碱溶液强;②误将钡盐[BaCl2、Ba(NO3)2]当作食盐食用时,常用0.5%的Na2SO4溶液解毒;③石灰岩(喀斯特地貌)的溶洞形成;④BaCO3不能做“钡餐”,而BaSO4则可以;⑤使用泡沫灭火器时“泡沫”生成的原理。
A.②③④
B.①②③
C.③④⑤
D.①②③④⑤
|
(2)氯化铝水溶液呈
性 ,其离子方程式表示为
;
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
。
4、填空题 下表中列出五种短周期元素A、B、C、D、E的信息,请推断后回答:
元素
| 有 关 信 息
|
A
| 元素主要化合价为-2,原子半径为0.074 nm
|
B
| 所在主族序数与所在周期序数之差为4
|
C
| 原子半径为0.102 nm,其单质为黄色晶体,可在A的单质中燃烧
|
D
| 最高价氧化物的水化物能按1
|
5、简答题 I、(1)NaHCO3是一种______(填“强”或“弱”)电解质;
(2)写出HCO3-水解的离子方程式:______;
(3)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH-五种微粒的浓度由大到小的顺序为:______.
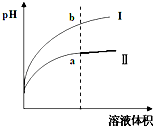
Ⅱ、醋酸是一种弱电解质.某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示.则图______(填“I”或“Ⅱ”)为醋酸稀释的图象.
Ⅲ、Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液.
(1)溶液中由水电离出c(OH-)=______;
(2)与某浓度盐酸溶液按体积比(碱与酸之比)1:9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=______.