1、填空题 (8分)在世纪之交,罗马尼亚的炼金废水汇入尼罗河,导致大量鱼类等水生物死亡,造成世界级 的水污染事件。炼金废水中含有络离子[Au(CN)2]-,它能电离出有毒的CN-,当CN-与H+结
的水污染事件。炼金废水中含有络离子[Au(CN)2]-,它能电离出有毒的CN-,当CN-与H+结 合时生成剧毒的HCN。完成下列问题:
合时生成剧毒的HCN。完成下列问题:
(1)HCN的水溶液酸性很弱,其电离方程式为_________________,NaCN的水溶液呈碱性是因为_________________(用离子方程式表示)。
(2)室温下,如果将0.1mol NaCN和0.05mol HCl全部溶于水,形成混合溶液(假设无损失),
①__?_和_?__两种粒子的物质的量之和等于0.1mol。
②_?__和_?__两种粒子的物质的量之和比H+多0.05mol。
参考答案:(共8分,2+2+1+1+1+1)
(1)HCN H++CN-? CN-+H2O
H++CN-? CN-+H2O HCN+OH
HCN+OH -
-
(2)①HCN和CN -?②CN -和OH -
本题解析:略
本题难度:一般
2、选择题 下列物质的溶液加热蒸干、灼烧后,所得的固体成份不相同的是(?)
A.FeCl2、FeCl3
B.NaHCO3、Na2CO3
C.Al2(SO4)3、AlCl3
D.NH4HCO3、NH4Cl
参考答案:C
本题解析:A、最后得到的为Fe2O3;B,最后得到Na2CO3;C、分别得到Al2(SO4)3和Al2O3;
D全部变为气体。
本题难度:一般
3、填空题 已知在室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,回答下列问题:
(1)两溶液中c(H+)・c(OH-)=________。
(2)各取5 mL上述溶液,分别加水稀释至50 mL,pH较大的是________溶液。
(3)各取5 mL上述溶液,分别加热到90℃,pH较小的是________溶液。
(4)两溶液中由水电离出的c(H+)分别为:H2SO4溶液________;NH4Cl溶液________。
(5)取5 mL NH4Cl溶液,加水稀释至50 mL,c(H+)________10-6 mol・L-1(填“>”、“<”或“=”),c(NH4+)/c(H+)________(填“增大”、“减小”或“不变”)
参考答案:(1)1×10-14 (2)H2SO4 (3)NH4Cl (4)1×10-9 mol/L 1×10-5 mol/L (5)> 减小
本题解析:(1)在室温时,水的离子积常数为1×10-14。
(2)加水稀释后H2SO4溶液中H+直接稀释,而NH4Cl溶液中NH4++H2O NH3・H2O+H+平衡右移,溶液中H+被稀释同时,又增加,故pH较大的是H2SO4溶液。
NH3・H2O+H+平衡右移,溶液中H+被稀释同时,又增加,故pH较大的是H2SO4溶液。
(3)升高温度促进NH4+的水解,H+浓度增大,故pH较小的是NH4Cl溶液。
(4)由水电离的c(H+)等于由水电离出的c(OH-),故H2SO4溶液中由水电离出的c(H+)= =10-9 mol/L,NH4Cl溶液中水电离出的c(H+)=1×10-5 mol/L。
=10-9 mol/L,NH4Cl溶液中水电离出的c(H+)=1×10-5 mol/L。
(5)加水稀释后使平衡NH4++H2O NH3・H2O+H+右移,故c(H+)>10-6 mol/L,
NH3・H2O+H+右移,故c(H+)>10-6 mol/L, 减小。
减小。
本题难度:一般
4、选择题 下列比较中,正确的是(? )
A.同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的pH比NaCN溶液大
B.物质的量浓度相等的NH4Cl和 NaOH溶液等体积混合后:
c(NH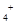 )>c(Cl
)>c(Cl )>c(Na
)>c(Na )>c(OH
)>c(OH )>c(H
)>c(H )
)
C.物质的量浓度相等的H2S和NaHS混合溶液中:
c(Na )+ c(H
)+ c(H )=c(S
)=c(S )+ c(HS
)+ c(HS )+ c(OH
)+ c(OH )
)
D.同物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3・H2O;c(NH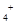 )由大到小的顺序是:①>②>③>④
)由大到小的顺序是:①>②>③>④
参考答案:D
本题解析:A、同温度同物质的量浓度时,HF比HCN易电离,说明HF的酸性比HCN的酸性强,根据盐的水解规律“越弱越水解”,二者的钠盐的水溶液均呈碱性,但NaCN的水解程度大于NaF的水解程度,所以NaCN溶液的pH值大,错误;B、物质的量浓度相等的NH4Cl和 NaOH溶液等体积混合后生成一水合氨与氯化钠,溶液呈碱性,离子浓度的大小关系是c(Cl )=c(Na
)=c(Na )> c(OH
)> c(OH )> c(NH
)> c(NH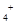 )> c(H
)> c(H ),错误;C、物质的量浓度相等的H2S和NaHS混合溶液,根据电荷守恒规律有c(Na
),错误;C、物质的量浓度相等的H2S和NaHS混合溶液,根据电荷守恒规律有c(Na )+ c(H
)+ c(H )=2c(S
)=2c(S )+ c(HS
)+ c(HS )+ c(OH
)+ c(OH ),错误;D、同物质的量浓度的4种溶液中,①的铵根离子与铝离子水解都使溶液呈酸性,所以铝离子的存在抑制铵根离子的水解,铵根离子浓度最大;②中只发生铵根离子的水解;③中的醋酸根离子水解使溶液呈碱性,所以对铵根离子的水解起促进作用;④中只发生一水合氨的电离,电离程度很小,所以铵根离子浓度最小,因此c(NH
),错误;D、同物质的量浓度的4种溶液中,①的铵根离子与铝离子水解都使溶液呈酸性,所以铝离子的存在抑制铵根离子的水解,铵根离子浓度最大;②中只发生铵根离子的水解;③中的醋酸根离子水解使溶液呈碱性,所以对铵根离子的水解起促进作用;④中只发生一水合氨的电离,电离程度很小,所以铵根离子浓度最小,因此c(NH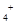 )由大到小的顺序是:①>②>③>④,正确,答案选D。
)由大到小的顺序是:①>②>③>④,正确,答案选D。
本题难度:一般
5、选择题 下列溶液中各微粒浓度关系判定不正确的是
A.10mL 0.2 mol・L-1的氨水与l0mL 0.1 mol・L-1的盐酸充分反应混合后的溶液中,存在c(NH4+)+c(NH3・H2O)=2c(Cl-)= 0.1 mol・L-1
B.已知酸性HF > CH3COOH,物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+) - c(F-) >c(K+) - c(CH3COO-)
C.CH3COOK溶液中加入少量NaNO3固体后的碱性溶液一定有:c(K+)+c(H+)=c(CH3COO- )+c(OH-)
D.已知NaHS03溶液pH<7,该溶液中一定有:c(Na+)> c(HSO3-)> c(SO32-)>c(H2SO3)
参考答案:B
本题解析:A. n(Cl-)=c・V=0.1mol/L×0.01L=0.001mol.在反应的过程中没有消耗。反应后c(Cl-)="n/L" ="0.001mol" ÷0.02L="0.05mol/L." n(NH3)= c・V=0.1mol/L×0.02L=0.002mol.反应后 n(NH3) ="n/L=0.002mol" ÷0.02L=" 0.1" mol/L根据物料守恒可得c(NH3)= c(NH4+)+c(NH3・H2O)= 0.1mol/L="2" c(Cl-).正确。B. HF、CH3COOH都是弱酸,所以NaF与CH3COOK都是强碱弱酸盐。由于酸性HF > CH3COOH,所以根据盐的水解规律:有弱才水解,越弱越水解,谁强显谁性。水解程度CH3COO->F-。n(NaF)=n(CH3COOK).水解程度越大,剩余离子的浓度就越小。所以c(K+) ?―c(CH3COO-) >c(Na+) ―c(F-)。错误。C. 在任何溶液中都存在着电荷守恒。即阳离子所带的正电荷总数与阴离子所带的负电荷总数相等。可得c(Na+)+c(K+)+c(H+)=c(CH3COO-)+c(OH-)+ c(NO3-)。由于NaNO3是强酸强碱盐,在溶液中不水解,所以c(Na+)=c(NO3-)。两式相减可得:c(K+)+c(H+)=c(CH3COO-)+c(OH-)。正确。D. NaHSO3是强碱弱酸的酸式盐。在溶液中存在电离平衡HSO3-- H++ SO32--,和水解平衡:HSO3+H2O--
H++ SO32--,和水解平衡:HSO3+H2O-- OH-+H2SO3。电离使溶液显酸性,水解使溶液显碱性。由于NaHSO3溶液pH<7,说明电离>水解。c(SO32-)>c(H2SO3).则根据物料守恒可得:c(Na+)= c(HSO3-) +c(SO32-)+ c(H2SO3)。由于c(HSO3-)的电离和水解消耗,所以c(Na+)> c(HSO3-)。因此在该溶液中一定有:c(Na+)> c(HSO3-)> c(SO32-) >c(H2SO3)。正确。
OH-+H2SO3。电离使溶液显酸性,水解使溶液显碱性。由于NaHSO3溶液pH<7,说明电离>水解。c(SO32-)>c(H2SO3).则根据物料守恒可得:c(Na+)= c(HSO3-) +c(SO32-)+ c(H2SO3)。由于c(HSO3-)的电离和水解消耗,所以c(Na+)> c(HSO3-)。因此在该溶液中一定有:c(Na+)> c(HSO3-)> c(SO32-) >c(H2SO3)。正确。
本题难度:一般