1������� (15��)��ˮ�и���þ���ɾ����Ӽ���������ˡ����ܡ��ᾧ����ˮ�Ȳ���õ���ˮ�Ȼ�þ��
�����õ�����þ��
��1���Ӽ����þ����ʱ�����ɵ�Mg(OH)2�ڷ�ɢϵ�д��ڳ����ܽ�ƽ�⣬���ܶȻ���������ʽ
Ksp=?��
��2��MgCl2��Һ�����ԣ���ˮ������ӷ���ʽΪ?��
��3����ȥMgCl2������Һ��������FeCl3���ɼ�����Լ���?
a��MgO? b��Mg(OH)2? c��MgCO3? d��MgSO4
��4�����ڿ����м���MgCl2��6H2O��������Mg(OH)Cl��MgO��д����صĻ�ѧ����ʽ֮һ
?��
��5��MgCl2��6H2O�ڸ����HCl�����м��ȿɵõ���ˮ�Ȼ�þ����ԭ����?��
��6��������ڵ�MgCl2�������ĵ缫��ӦʽΪ��?�������ĵ缫��ӦʽΪ?��
�ο��𰸣���1��Ksp=c(Mg2+)��c2(OH��) ��3�֣�
��2��Mg2+ + 2H2O  ?Mg(OH)2 +2H+��2�֣�
?Mg(OH)2 +2H+��2�֣�
��3��abc��2�֣�
��4��MgCl2��6H2O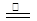 Mg(OH)Cl + HCl��+5H2O����MgCl2��6H2O
Mg(OH)Cl + HCl��+5H2O����MgCl2��6H2O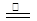 MgO + 2HCl��+5H2O����2�֣�
MgO + 2HCl��+5H2O����2�֣�
��5��HCl����������Mg2+ˮ�⣨2�֣�
��6��2Cl�D�D2e��=Cl2����2�֣���Mg2++2e��=Mg��2�֣�
����������Ÿ���Mg(OH)2���ܽ�ƽ��ʽ��Mg(OH)2(s) Mg2+(aq)+2OH- (aq)��д�����ܶȻ���������ʽ��
Mg2+(aq)+2OH- (aq)��д�����ܶȻ���������ʽ��
��MgCl2��Һ��Mg2+ˮ�⣺Mg2+ + 2H2O  ?Mg(OH)2 +2H+��ʹ��Һ�����ԣ�
?Mg(OH)2 +2H+��ʹ��Һ�����ԣ�
�Ǹ���FeCl3��ˮ�⣺FeCl3+3H2O Fe(OH)3+3HCl������MgO��Mg(OH)2��MgCO3���ܴٽ�FeCl3��ˮ�⣬ʹ��ת��Fe(OH)3��������ȥ��ͬʱ������MgO��Mg(OH)2��MgCO3��ͨ�����˳�ȥ��
Fe(OH)3+3HCl������MgO��Mg(OH)2��MgCO3���ܴٽ�FeCl3��ˮ�⣬ʹ��ת��Fe(OH)3��������ȥ��ͬʱ������MgO��Mg(OH)2��MgCO3��ͨ�����˳�ȥ��
���ڿ����м���MgCl2��6H2O���ٽ�MgCl2��ˮ�⣬��HCl��H2O�ݳ���������Mg(OH)Clʱ�䷴Ӧ����ʽΪMgCl2��6H2O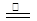 Mg(OH)Cl + HCl��+5H2O����������MgOʱ�䷴Ӧ����ʽΪMgCl2��6H2O
Mg(OH)Cl + HCl��+5H2O����������MgOʱ�䷴Ӧ����ʽΪMgCl2��6H2O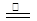 MgO + 2HCl��+5H2O����
MgO + 2HCl��+5H2O����
��MgCl2��6H2O�ڸ����HCl�����м��ȣ�HCl����������Mg2+ˮ�⣬�����ɵõ���ˮ�Ȼ�þ��
�ʵ�����ڵ�MgCl2����������������Ӧ����缫��ӦʽΪ2Cl�D�D2e��=Cl2��������������ԭ��Ӧ����缫��ӦʽΪMg2++2e��=Mg��
�����Ѷȣ�һ��
2��ѡ���� ������������ȷ����
A��pH��ͬ��CH3COONa��Һ��C6H5ONa��Һ��Na2CO3��Һ��NaOH��Һ��
c(CH3COONa)��c(C6H5ONa )��c(Na2CO3)��c(NaOH )
B����pH = 3��һԪ����HA��pH = 11��NaOH��Һ��Ϻ���Һ�Լ��ԣ�һ���У�
c(H+) �� c(OH- )�� c(A-) ��c(Na+)
C���ڳ����£�10 mL 0.02 mol��L��1 HCl��Һ��10 mL 0.02 mol��L��1 Ba(OH)2��Һ��ֻ�ϣ����Ϊ20 mL������Һ��pH = 12+lg2
D����0.2 mol��L��1��������0.1 mol��L��1��NaAlO2��Һ�������ϣ�����Һ������Ũ����С�����˳��Ϊ��c(OH-)��c(Al3+)��c(H+)��c(Na+)��c(Cl-)
�ο��𰸣�A
�����������Խ������Ӧ������Խ����ˮ�⣬�����Ǵ��̼����ӣ�̼�����ƣ�����̼���Ƶ�ˮ��̶��������ǿ����������������ǿ������pH��ͬ�������£��������Ƶ�Ũ����С������ѡ��A��ȷ��B��HA�����ǿ�ᣬ���������ƹ�������Һ�����Լ��ԡ������HA�����ᣬ��Ҫʹ��Һ�Լ��ԣ�����������Ҳ�ǹ����ģ�����c(OH- )�Ϳ��Դ���c(A-) �ģ�B����ȷ��
C�м���������Է�Ӧ�����Һ��c(OH- )��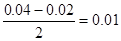 mol/L������pH��12��C����ȷ��
mol/L������pH��12��C����ȷ��
D���������������������Ȼ������Ȼ��ƣ�����c(Al3+)��c(H+)��D����ȷ����ѡA��
�����Ѷȣ�һ��
3��ѡ���� �����£�������Һ�е���Ũ�ȹ�ϵ��ȷ����(����)
A��������ˮ�м������NaOH��c(Na��)��c(Cl��)��c(ClO��)��c(OH��)
B��pH��8��3��NaHCO3��Һ��c(Na��)>c(HCO3-)>c(CO32-)>c(H2CO3)
C�������£�pH��7��NH4Cl�백ˮ�Ļ����Һ�У�c(Cl��)��c(NH4+)>c(OH��)��c(H��)
D��0��1 mol��L��1CH3COONa��Һ�У�c(OH��)��c(CH3COOH)��c(H��)
�ο��𰸣�CD
���������������ˮ�м����������ƺ�Ӧ������Һ���е���غ�ʽΪc(Na��)+ c(H��)��c(Cl��)��c(ClO��)��c(OH��)����A����̼��������Һ�Լ��ԣ�˵��ˮ����ڵ��룬����ˮ�������c(H2CO3) ���ڵ��������c(CO32-)����B����NH4Cl�백ˮ�Ļ����Һ�����ԣ���c(OH��)��c(H��)����˱�Ȼ��c(Cl��)��c(NH)��C��ȷ��CH3COONa��Һ�������غ�c(OH��)��c(CH3COOH)��c(H��)����D��ȷ����ѡCD��
�����Ѷȣ�һ��
4��ѡ���� 100mL0.1mol/L��������Һ�У��������������ٵ�����˳����ȷ����
��CaCl2?��CH3COONa?��NaCl?��Na2CO3
A���٣��ܣ��ۣ���
B���٣��ܣ���=��
C���٣���=��=��
D���٣��ܣ��ڣ���
�ο��𰸣�A
������������Ȼ��������ӵ����ʵ���Ϊ��0.1L��0.1mol/L��2=0.02mol���ڴ������������ӵ����ʵ���Ϊ��0.1L��0.1mol/L=0.01mol������Ϊ�����ˮ�⣬��С��0.01mol�����Ȼ��������������ʵ���Ϊ��0.1L��0.1mol/L=0.01mol����̼�����������ӵ����ʵ���Ϊ��0.1L��0.1mol/L=0.01mol������̼���ˮ�⣬CO32-+H2O HCO3-+OH-�ʴ���0.01mol���ʢ٣��ܣ��ۣ��ڡ�
HCO3-+OH-�ʴ���0.01mol���ʢ٣��ܣ��ۣ��ڡ�
�����Ѷȣ�һ��
5��ѡ���� 30��ʱ����0.1mol/L��Na2S��NaHS����Һ�о����ڵĹ�ϵ��(���� )��
A��c(H+)��c(OH-)��1��10-14
B��c(Na+)=c(S2-)+c(HS-)+c(H2S)
C��c(OH-)=c(H+)+c(HS-)+2c(H2S)
D��c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)
�ο��𰸣�D
���������A ����30�����25�棬���ԣ�c(H+)��c(OH-)>1��10-14
B ����Na2S��c(Na+)=2c(S2-)+2c(HS-)+2c(H2S)
NaHS�У�c(Na+)=c(S2-)+c(HS-)+c(H2S)
C ����ֻ��Na2S��Һ�д���
D ��ȷ��������Һ�ж����ڵ���غ�
��ѡD
�����Ѷȣ�һ��