1、选择题 下列离子方程式书写正确的是
[? ]
A.向水玻璃中加入过量醋酸:2H++SiO32-=H2SiO3↓
B.硅酸钠溶液与澄清石灰水反应:SiO32-+Ca2+=CaSiO3↓
C.酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+ 5I-+3H2O=3I2↓+6OH-
D.AgNO3溶液中加入过量的氨水:Ag++NH3・H2O= AgOH↓+NH4+
参考答案:B
本题解析:
本题难度:一般
2、选择题 下列离子方程式不正确的是?



A.向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
B.在亚硫酸中加入过量的次氯酸钠溶液:H2SO3+ClO-=Cl-+2H++SO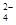
C.在碳酸氢镁溶液中加入过量氢氧化钠溶液:
Mg2++2HCO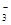 +4OH-=Mg(OH)2 ↓+2CO
+4OH-=Mg(OH)2 ↓+2CO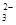 +2H2O
+2H2O
D.在过氧化钠中加入稀硫酸:2Na2O2+4H+=4Na++2H2O+O2↑
参考答案:B
本题解析:反应物量的不同生成产物就不同:
1.亚硫酸与过量次氯酸钠:溶液呈碱性
ClO- + H2SO3 + 2OH- = SO42- + Cl- + 2H2O
若两者恰好等物质的量
ClO- + H2SO3 = SO42- + Cl- + 2H+
若亚硫酸过量,溶液呈酸性
ClO- + H2SO3 = SO42- + Cl- + 2HClO
本题难度:一般
3、实验题 高铁酸钾广泛应用于净水、电池工业等领域。工业上以钛白粉生产的副产品FeSO4制备高铁酸钾的生产流程如下:
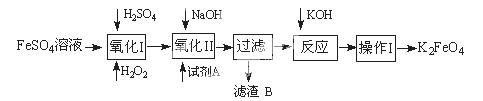
查资料得知K2FeO4的一些性质:
①在碱性环境中稳定,在中性和酸性条件下不稳定
②溶解度很大,难溶于无水乙醇等有机溶剂
③具有强氧化性,能氧化有机烃、苯胺和80%以下乙醇溶液
回答下列问题:
(1)写出“氧化I”中,生成Fe3+的离子反应方程式?。
(2)氧化II中,试剂A为? (填“H2O2”或“HNO3”或“NaClO”);过滤操作中,得到的滤渣B中除NaCl还有?
(3)操作I中包括冷却结晶、过滤、洗涤干燥几个步骤。洗涤干燥的目的是脱碱脱水,进行该操作时最好用?洗涤。
(4)净水时高铁酸钾能逐渐与水反应生成絮状的Fe(OH)3,请补充并配平该反应方程式:?K2FeO4 + ??H2O = ?Fe(OH)3↓ + ?KOH + ??
(5)将一定量的K2FeO4投入一定浓度的FeCl3溶液中,测得剩余K2FeO4浓度如下图所示,推测产生曲线I和曲线II差异的原因是?。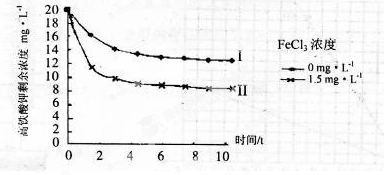
参考答案:(16分)
(1)H2O2+2H++2Fe2+=2Fe3++2H2O(3分,配平错扣1分)
(2)NaClO? Na2SO4(各2分,共4分)
(3)无水乙醇(3分)
(4)4? 10? 4? 8? 3O2 ↑?(产物正确1分,共3分)
(5)FeCl3溶液水解显酸性,促进K2FeO4与水反应,从而降低K2FeO4浓度(3分)
本题解析:(1)原料为硫酸亚铁溶液,所含亚铁离子具有还原性,硫酸是强酸,提供氢离子,不仅能抑制亚铁离子和铁离子的水解,而且能增强过氧化氢的氧化能力,使亚铁离子氧化为铁离子,根据化合价升降法、电荷守恒、原子守恒配平,则氧化I中生成铁离子的离子方程式为H2O2+2H++2Fe2+=2Fe3++2H2O;(2)由于目标产物是K2FeO4,它在碱性环境中稳定,在中性和酸性条件下不稳定,则氧化II中加入的氧化剂不能使H2O2,因为H2O2在碱性条件下的氧化性比酸性条件下弱,试剂A也不能是HNO3,因为酸性条件下Na2FeO4不稳定,试剂A只能是 NaClO,氧化II中反应为2NaOH+H2SO4=Na2SO4+2H2O、Fe2(SO4)3+3NaClO+10NaOH==2Na2FeO4+3NaCl+3Na2SO4+5H2O;根据已知信息可知,K2FeO4的溶解度很大,由此类推Na2FeO4的溶解度很大,为了从Na2FeO4、NaCl、Na2SO4、NaClO(过量)、NaOH(过量)组成的混合溶液中分离出Na2FeO4、NaOH(过量),则过滤所得滤渣的主要成分为NaCl、Na2SO4、NaClO(过量),除去它们之后所得的Na2FeO4、NaOH(过量)溶液用于制备K2FeO4;(3)Na2FeO4、NaOH(过量)溶液中加入过量KOH时的反应为:Na2FeO4+2KOH= K2FeO4+2NaOH,所得溶液经过蒸发浓缩、冷却结晶、过滤、洗涤可得K2FeO4晶体;由于K2FeO4的溶解度很大,难溶于无水乙醇等有机溶剂,且具有强氧化性,能氧化有机烃、苯胺和80%以下乙醇溶液,除去碱的同时,为了减少洗涤晶体造成K2FeO4的损失,最好选择无水乙醇洗涤K2FeO4晶体;(4)观察可得,该反应中铁元素由+6价将为+3价,钾元素、氢元素的化合价都没有变化,根据氧化还原反应的特征推断,化合价升高的元素只能是氧,氧元素由―2价升为其相邻的0价,则缺项物质为氧气,根据化合价升降法、原子守恒配平可得:4K2FeO4+10H2O==4Fe(OH)3↓ +8KOH+3O2↑;(5)根据已知信息可知,K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定,氯化铁是强酸弱碱盐,能水解,导致其溶液显弱酸性,K2FeO4在酸性条件下不稳定,酸性越强,K2FeO4越不稳定,反应速率越大,剩余K2FeO4的浓度越小。
本题难度:困难
4、选择题 下列离子方程式正确的是(? )
A.石灰石溶于醋酸: CaCO3 + 2CH3COOH = 2CH3COO-+ Ca2+ + CO2↑+ H2O
B.钠与硫酸铜溶液反应: Cu2+ + 2Na = 2Na+ + Cu
C.铁屑溶于过量稀硝酸:3Fe + 8H+ + 2NO3-=3Fe2+ + 2NO↑+ 4H2O
D.FeCl2溶液中通入少量氯气:Fe2+ + Cl2= Fe3+ + 2Cl-
参考答案:A
本题解析:A选项正确,B选项钠先与水发生反应,不会置换出铜单质。C选项过量硝酸会把二价铁氧化成三价铁。D选项等号两边电荷不守恒。
点评:本题考查基本离子方程式的书写,抓住离子方程式的书写规则。
本题难度:一般
5、选择题 下列有关化学用语使用正确的是
[? ]
A.稀盐酸与澄清石灰水发生中和反应的热化学方程式为:H+(aq) +OH-(aq)=H2O(l) △H=-57.3 kJ/mol
B.碳酸氢钠的水解方程式:HCO3-+H2O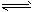 CO32-+H3O+
CO32-+H3O+
C.向NaHSO4溶液中加入过量Ba(OH)2溶液的离子方程式:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
D.用Na2CO3溶液吸收少量SO2的离子方程式:CO32-+SO2=CO2+SO32-
参考答案:A
本题解析:
本题难度:一般