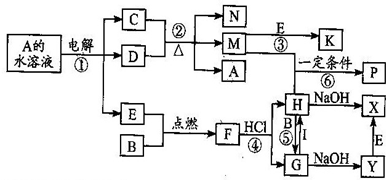
1������� ��֪B��CΪ���������ֽ������ʣ�E��IΪ���������ַǽ������ʣ�AΪ�����η�Ӧ��ΪD����Һ��C�ڼ��������µķ�Ӧ��P��Һ��G��Һ�о�����ͬ�������ӣ������Ҫ��ش��������⣮
��1��BԪ�������ڱ���λ�ã�______��
��2������I�ĵ���ʽ��______��
��3��Yת��ΪX�������ǣ�______���漰�ķ�Ӧ����ʽΪ��______��
��4��д����Ӧ�ܵĻ�ѧ��Ӧ����ʽ��______������F��HIˮ��Һ�����ӷ�Ӧ����ʽ?ʽ��______��
��5�����ˮ�м���H�ı�����Һ���ɵõ����ɫ��Һ������Һ����������______��
A�����ж����ЧӦ
B������ֱ����Դ����������Һ��ɫ����
C������������Һ�����ȳ������ܽ������
D��������Ĥ����������ֽ
��6����1molG����Һ�м���1molNa2O2�������������ӷ�Ӧ����ʽ��______��
�ο��𰸣�AΪ�����Σ������������Һ����������������E��������������������C��˵����������C�Ļ��С����Ԫ�أ���CΪ�����Ľ������ʣ�����C��ͭ����D�����ᣬA������ͭ�����������£�Ũ�����ͭ��Ӧ��������ͭ�����������ˮ��ˮ������ͭ������������Ӧ�����������������Ӧ����������������M�Ƕ�������N��ˮ��K����������B�ǽ�����H��B��Ӧ����G��G��I��Ӧ����H��˵��B�DZ�۽��������dz�������������B����������������Ӧ��������������F�����������������ᷴӦ�����Ȼ������Ȼ�������H������Ӧ����G������H���Ȼ�����G���Ȼ��������Ȼ�������I��Ӧ�����Ȼ�������I���������Ȼ������������Ʒ�Ӧ���������������Ȼ��ƣ��Ȼ��������������Ʒ�Ӧ�����Ȼ��ƺ�������������Y������������X������X������������Y������������������������Ȼ�����Һ��Ӧ������������ӡ��������ӣ�
��1���������ڱ���λ�ڵ������ڵڢ����壬�ʴ�Ϊ���������ڵڢ����壻
��2�������ĵ���ʽΪ��
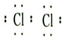
���ʴ�Ϊ��
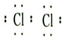
��
��3�������������ǰ�ɫ�����������ȶ���Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ����Ӧ����ʽΪ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
�ʴ�Ϊ����ɫ��״����Ѹ�ٱ�Ϊ����ɫ������ת��Ϊ���ɫ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��4�����������������ᷴӦ�����Ȼ��������Ȼ�����ˮ����Ӧ����ʽΪ��Fe3O4+8HCl=FeCl2+2FeCl3+4H2O������������������ᷴӦ�����������ӡ��ⵥ�ʺ�ˮ��
���ӷ���ʽΪFe3O4+2I-+8H+=I2+3Fe2++4H2O���ʴ�Ϊ��Fe3O4+8HCl=FeCl2+2FeCl3+4H2O��Fe3O4+2I-+8H+=I2+3Fe2++4H2O��
��5�����ˮ�м���H�ı�����Һ�����Ƶ������������壬����������У������ЧӦ����Ӿ�������۳�����������Ĥ��
A����������������ж����ЧӦ������ȷ��
B�������������������磬��ֱ����Դ������������Һ��ɫ����ʴ���
C������������Һ�ȳ��־۳��������������������Ӧ�����Ȼ��������Գ��ֵ��������ȳ������ܽ⣬����ȷ��
D���������Ӳ�������Ĥ��������ֽ���ʴ���
��ѡAC��
��5����1mol�Ȼ�������Һ�м���1molNa2O2�����ݵ�ʧ���������֪���������ƹ������������ƺ�ˮ��Ӧ�����������ƺ���������Ӧ����ʽΪNa2O2+H2O�T2NaOH+12O2�����Ȼ��������������ơ�������Ӧ���������������Ȼ��ƣ���Ӧ����ʽΪ��2FeCl2+4NaOH+12O2+H2O�T2Fe��OH��3��+4NaCl�������ܵķ�Ӧ����ʽΪ��4FeCl2+4Na2O2+6H2O�T4Fe��OH��3��+8NaCl+O2�������ӷ���ʽΪ��4Fe 2++4Na2O2+6H2O�T4Fe��OH��3��+8Na++O2�����ʴ�Ϊ��4Fe 2++4Na2O2+6H2O�T4Fe��OH��3��+8Na++O2����
���������
�����Ѷȣ�һ��
2������� ��8�֣�A��B��C��D��E��F��G��H��I��J��K������ѧ�α��������ʣ�������X������ͼ�ת����ϵ��
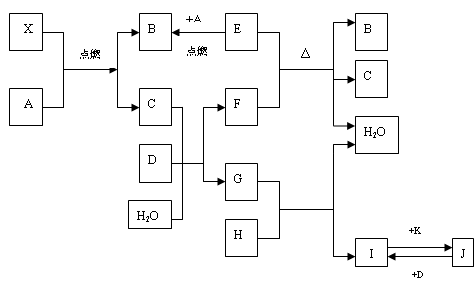
��֪����A��D��E��KΪ���ʣ�����EΪ��ɫ���壻
��X��A��B��C��DΪ���壬B��C����ʹ����ʯ��ˮ����ǣ�C��D����ʹƷ����Һ��ɫ��
��H��һ�ֺ���ɫ���������
��ش��������⣺
��1��B���ӵĵ���ʽ��_______________��
��2��J�백ˮ��Ӧ�����ӷ���ʽ��_______________________________________��
��Ӧȫ���̵������ǣ�_____________________________________________��
��3��E��F��Ӧ�Ļ�ѧ����ʽ��__________________________________________��
��4������X�к�������Ԫ�أ������и�ԭ�Ӿ��ﵽ8�����ȶ��ṹ�����H2������ܶ�Ϊ30�����ƶ�X�ķ���ʽ��___________��X�Ľṹʽ��____________��
�ο��𰸣���1��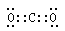
��2��Fe2++2NH3��H2O= Fe��OH��2��+2NH4+
�����ɰ�ɫ������������Ϊ����ɫ�����ճʺ��ɫ
��3��C+2H2SO4��Ũ��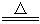 CO2��+2 SO2��+ 2H2O
CO2��+2 SO2��+ 2H2O
��4��SCO? S=C=O
���������B��C��Ϊ�����Ҿ���ʹ����ʯ��ˮ����ǣ�C��ʹƷ����Һ��ɫ���ۺϿ��ж�BΪCO2��CΪSO2����AΪ���嵥�ʣ���X����ȼ�տ�����CO2��SO2����֪AΪ��������X�����к��������뺬��̼����Ԫ�أ�
C��SO2����D����ʹƷ����Һ��ɫ���Ҿ�Ϊ���壬�²�DΪ������������ȣ���Cl2��SO2��2H2O=H2SO4��2HCl������ɫ���嵥��E����A��������ȼ������CO2����EΪ̼��̼��F������CO2��SO2��ˮ������ж�FΪ���ᣬ��GΪ���
H��һ�ֺ���ɫ���������Ҳ����Fe2O3�������ᷴӦ����I����FeCl3��Fe2O3��6HCl=2FeCl3��3H2O��J���ʿ���D������������FeCl3����֪JΪFeCl2��KΪ������
��1��CO2Ϊֱ���ͷ��ӣ�����̼��˫����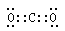
��2����ȡ Fe��OH��2��Fe2++2NH3��H2O= Fe��OH��2��+2NH4+
Fe��OH��2�ױ������������ɰ�ɫ������������Ϊ����ɫ�����ճʺ��ɫ Fe��OH��3
��3��C+2H2SO4��Ũ�� CO2��+2 SO2��+ 2H2O
CO2��+2 SO2��+ 2H2O
��4��������֪��������һ������S��Cԭ�ӣ�����ȼ������SO2��CO2���ʵ�����Ԫ��ֻ��ΪOԪ�أ���Է�������Ϊ30��2=60��˵������ʽֻ��ΪSCO��
�����и�ԭ�Ӿ��ﵽ8�����ȶ��ṹ����C�γ��ļ���O��S��Ϊ��������ϵCO2�Ľṹ�ɵ�X�ĽṹʽΪ��S=C=O
�����Ѷȣ���
3������� ���й����ʴ�����ͼ��ʾ��ת����ϵ(���ֲ�����ʡ��)��ͨ��BΪ��ɫ��ĩ��CΪ���嵥�ʣ�GΪ�Ϻ�ɫ���嵥�ʡ�ʵ�����У����ù���E��B�Ĵ��¼�����ȡ���嵥��H��

��ش��������⣺
��1����Ӧ�ٵĻ�ѧ����ʽΪ________________________________��
��2����Ӧ�ڵ����ӷ���ʽΪ________________________________ ��
��3��D��Һ��Pb(NO3)2��Һ��Ͽ��γɳ������˳�����Ksp=7.0��10��9��Ũ��Ϊ0.01mo1/L��D��Һ��a mo1/L��Pb(NO3)2��Һ�������ϣ������ɳ�����������СֵΪ____________��
��4�����F����Һ����ʵ�ֵ���ת��Ϊ��ѧ�ܣ���д�����Ե缫���������F��Һ�����ӷ���ʽ________________________________��
��ͭ��Cu2S���ɷ�����Ӧ2Cu2S+2H2SO4+5O2=4CuSO4+2 H2O���÷�Ӧ�Ļ�ԭ����___________����1mol O2������Ӧʱ����ԭ����ʧ���ӵ����ʵ���Ϊ______mol����CuSO4��Һ�м���þ��ʱ���������ɣ���������____________��
�ο��𰸣���1�� MnO2 + 4HCl��Ũ�� MnCl2 + H2O + Cl2��?��2�� 6I-+ClO3-+6H+=3I2+Cl-+3H2O
MnCl2 + H2O + Cl2��?��2�� 6I-+ClO3-+6H+=3I2+Cl-+3H2O
��3��5.6��10-4?��4�� 2Cl-+ 2H2O  ?2OH- + H2�� + Cl2��
?2OH- + H2�� + Cl2��
��Cu2S��? 4��?����
���������GΪ�Ϻ�ɫ���嵥�ʣ�һ���Ԥ��Ϊ�ⵥ�ʣ����Ƶ�C����Ϊ��������AΪ���ᡢBΪ�������̣�E�ڶ������̵Ĵ�����ȡH����EΪ����ء�HΪ������FΪ�Ȼ��أ�����Dһ��Ϊ�⻯�ء������Ƴ�A���ᡢB�������̡�C������D�⻯�ء�E����ء�F�Ȼ��ء�G�⡢H������
����ӦΪ�⻯ǦPbO2��Ksp=������Ũ�ȵ�ƽ������Ǧ����Ũ�ȣ���Ϻ������Ũ��Ϊ0.005mo1/L,���ݴ�ʽ�����Pb(NO3)2�����ʵ���Ũ��Ϊ5.6? �� 10-4 mo1/L
��4��2Cl-+ 2H2O  ?2OH- + H2�� + Cl2��
?2OH- + H2�� + Cl2��
�����Ѷȣ�һ��
4���ƶ��� ���й�ϵͼ�У�A��һ�����Σ�D����Է���������C����Է���������16��E���ᡣ��X������ǿ�ỹ��ǿ��ʱ����������ת����ϵ
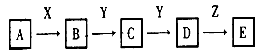
��X��ǿ��ʱ��A��B��C��D��E������ͬһԪ�أ���X��ǿ��ʱ��A��B��C��D��E��������һ��Ԫ�ء�
�ش��������⣺
��1��A��_______________��Y��______________��Z��_____________��
��2����X��ǿ��ʱ��E��_______________����X��ǿ�ᣬE��____________��
��3��д��A��X��Ӧ�����ӷ���ʽ��
��______________________�� ��_______________________��
�ο��𰸣���1��A��(NH4)2S��Y��O2��Z��H2O
��2��E��HNO3��E��H2SO4
��3��NH4++OH-==NH3��H2O����NH4++OH-==NH3��+H2O����S2-+2H+=H2S��
���������
�����Ѷȣ�һ��
5������� ijЩ��ѧ��Ӧ������ʽ��ʾ:A+B��C+D+H2O
��ش��������⣨��Ӧ�����ǹ���֮��ķ�Ӧ��Ҳ��������ˮ��Һ�н��еķ�Ӧ����
��1����A�Ƿǽ�����̬���ʣ���Ӧ��������Һ������������ɱ������AΪ?���ѧʽ��ͬ������Ӧ�Ļ�ѧ����ʽΪ?��
��2����AΪ�ǽ�����̬���ʣ�C��D��Ϊ�����Ҷ���ʹ����ʯ��ˮ����ǡ���AΪ?����Ӧ�Ļ�ѧ����ʽΪ?��
��3����AΪ�Ϻ�ɫ������DΪ��ɫ���塣��AΪ?����Ӧ�����ӷ���ʽΪ?��
��4����AΪ�ռ���Һ��C����Է�������Ϊ100�İ�ɫ������DΪ���Ρ���CΪ?����Ӧ�����ӷ���ʽΪ?��
��5����A��BΪ���壬C��ˮ��Һ��ʹ��̪��Һ��Ϊ��ɫ��ʵ���ҳ��ô˷�Ӧ�Ʊ�C���塣��CΪ?����Ӧ�Ļ�ѧ����ʽΪ?��
�ο��𰸣���1��Cl2��2NaOH+Cl2��NaCl+NaClO+H2O
��2��C��C+2H2SO4(Ũ) CO2��+2SO2��+2H2O ��3��Cu��Cu+4H++2NO3-��Cu2++2H2O+2NO2��
CO2��+2SO2��+2H2O ��3��Cu��Cu+4H++2NO3-��Cu2++2H2O+2NO2��
��4��CaCO3��2OH-+Ca2++2HCO3-=2H2O+CaCO3��+CO32-
��5��NH3��Ca(OH)2+2NH4Cl CaCl2+2NH3��+2H2O����ˮ�������ͷ����Ҫ��
CaCl2+2NH3��+2H2O����ˮ�������ͷ����Ҫ��
�����������1����A�Ƿǽ�����̬���ʣ���Ӧ��������Һ������������ɱ������AΪCl2��B���������ƣ���÷�Ӧ�Ļ�ѧ����ʽΪ2NaOH+Cl2��NaCl+NaClO+H2O��
��2����AΪ�ǽ�����̬���ʣ�C��D��Ϊ�����Ҷ���ʹ����ʯ��ˮ����ǣ�������Ӧ����CO2��SO2������AΪC��B��Ũ���ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪC+2H2SO4(Ũ) CO2��+2SO2��+2H2O��
CO2��+2SO2��+2H2O��
��3����AΪ�Ϻ�ɫ��������A��Cu��DΪ��ɫ���壬��D������NO2����˸���Ũ������ͭ������������ԭ��Ӧ�����Ը÷�Ӧ�����ӷ���ʽΪCu+4H++2NO3-��Cu2++2H2O+2NO2����
��4����AΪ�ռ���Һ��C����Է�������Ϊ100�İ�ɫ��������C��̼��ƣ���ѧʽΪCaCO3��DΪ���Σ���DΪ̼���Σ�B����̼�������Σ����Ը÷�Ӧ�����ӷ���ʽΪ2OH-+Ca2++2HCO3-=2H2O+CaCO3��+CO32-��
��5����A��BΪ���壬C��ˮ��Һ��ʹ��̪��Һ��Ϊ��ɫ��˵��C��Һ�Լ��ԡ�ʵ���ҳ��ô˷�Ӧ�Ʊ�C���壬��CΪNH3����˸÷�Ӧ�Ļ�ѧ����ʽΪCa(OH)2+2NH4Cl CaCl2+2NH3��+2H2O��
CaCl2+2NH3��+2H2O��
�����Ѷȣ�һ��