1、选择题 某实验小组只领取下列仪器和用品:铁架台、铁夹、铁圈、三角架、石棉网、烧杯、漏斗、分液漏斗、酒精灯、玻璃棒、量筒、蒸发皿、圆底烧瓶、火柴。不能进行的实验操作是
A.蒸馏
B.萃取
C.过滤
D.蒸发
参考答案:A
本题解析:
考查常见仪器的使用。
根据仪器可知,没有冷凝管,因此不能蒸馏,答案选A。
本题难度:简单
2、选择题 试管中盛有少量白色固体,可能是铵盐,检验的方法是?
A.加水,将湿润的红色石蕊试纸放在试管口
B.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口
C.加氢氧化钠溶液,加热,用蘸有浓硫酸的玻璃棒靠近瓶口
D.加氢氧化钠溶液,滴入紫色石蕊试剂
参考答案:B
本题解析:铵盐能和强碱反应生成氨气,而氨气是一种碱性气体,所以检验钠盐的方法是加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口,答案选B。
点评:该题是中等难度的试题,也是高考中的重要考点之一。该类试题学生需要明确的是进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。
本题难度:简单
3、选择题 下列化学实验事实及其解释都正确的是( )
A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.某气体能使湿润的红色石恋试纸变蓝,该气体水溶液一定显碱性
C.加入AgN03溶液,生成白色沉淀,再加入稀盐酸沉淀不溶解,可确定有CI-存在
D.用量筒取5.00mL 1.00mol?L-1盐酸于50mL容量瓶中,加水稀释至刻度,可配制0.100mol?L-1盐酸
参考答案:B
本题解析:
本题难度:一般
4、实验题 铁触媒(铁的氧化物)是合成氨工业的催化剂。某同学设计了以下两种方案研究铁触媒的组成。
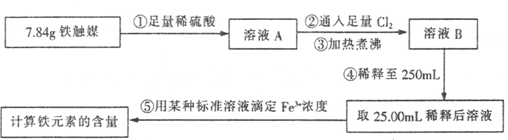
方案一:用下列实验方法测定铁触媒的含铁量,确定其组成。
(1)步骤④中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和?。
(2)若通入Cl2不足量,溶液B中还含有?会影响测定结果。
(3) 若通入Cl2过量且加热煮沸不充分,溶液B中可能含有Cl2。请设计实验方案检验Cl2,完成下列实验报告。
限选试剂:0.1mol L-1酸性KMnO4溶液、紫色石蕊试液、淀粉-KI溶液、0.1mol L-1 KSCN溶液、 品红稀溶液
实验操作
| 实验现象与结论
|
取适量溶液B于试管中,滴加?,振荡
,放置一段时间后,观察现象。
| 若溶液?,则溶液B中含Cl2;
若溶液?,则溶液B中不含Cl2。
|
方案二 :用下列装置测定铁触媒的含铁量,确定其组成。
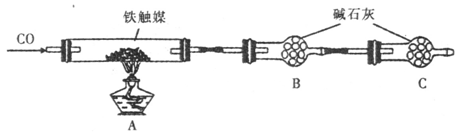
(4)干燥管C的作用是?。
(5)称取15.2g铁触媒进行上述实验。充分反应后,测得干燥管B增重ll.0g,则该铁触媒的化学式可表示为?。
参考答案:
(1)250mL容量瓶?(2分)
(2)FeCl2或者FeSO4或者Fe2+?(2分)
(3)2-3滴紫色石蕊试液(或者是品红溶液)(2分)溶液显红色后,红色褪去。(品红溶液只需要答红色褪去)?(2分)?溶液不褪色(2分)
(4)防止空气中的CO2和水蒸气进入B中?(2分)
(5)Fe4O5或2FeO・Fe2O3或FeO・Fe3O4(其他合理答案均可)?(3分)
本题解析:⑴配制一定物质的量浓度的溶液,要用到的仪器一定要有容量瓶,并且要指明规格。在此题中,必需说明是250mL容量瓶。⑵如若氯气不足,则溶液A中的二价铁离子就会氧化不完全,影响后续实验。⑶可以使用紫色石蕊试液来检验。⑷防止空气中的二扣化碳和水蒸汽进入B中,影响实验结果。⑸干燥管B增加的质量是二氧化碳的质量,二氧化碳是一氧化碳结合一个氧原子生成的,因此铁触媒中的氧元素的质量就等于干燥管中增加的二氧化碳的物质的量,由此可以计算:n(O)=11g/44g/mol=0.25mol,那么15.2g铁触媒中铁的物质的量就可以用下列的方式来进行计算: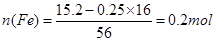 ;所以
;所以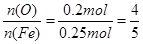
本题难度:困难
5、选择题 下列除杂方法正确的是( )
A.除去氯化钠溶液中混有的碳酸钠,加过量的氯化钡溶液后过滤
B.除去CO中混有的CO2,通过足量的灼热的氧化铜
C.通过分液除去酒精中混有的水
D.通过蒸馏除去自来水中混有的各种盐获取蒸馏水
参考答案:A、氯化钡溶液与碳酸钠反应生成碳酸钡沉淀和氯化钠,但加入过量的氯化钡溶液又引入了新杂质,故A错误;
B、氧化铜会将一氧化碳氧化成二氧化碳,故B错误;
C、酒精和水是互溶的两种液体,不能用分液除去酒精中混有的水,故C错误;
D、水中的杂质难挥发,可用蒸馏除去自来水中混有的各种盐获取蒸馏水,故D正确;
故选:D.
本题解析:
本题难度:一般