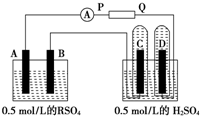
1������� ��ͼ��ʾ�DZ�ʾ������Һ���е���װ�ã�
�缫A�ɽ���R�Ƴɣ�R�������εĻ�ѧʽΪRSO4��B��C��D����Pt��P��Q�ǵ�ص���������·��ͨ��R�����ڵ缫B�ϣ�ͬʱ�缫C��D�ϲ������ݣ�
��1����ص�������______��
��2��A�缫�ϵķ�Ӧʽ��______��
��3�����ڵ缫C��D�ϵ����Թ����ռ���������������______��
��4��������ǿ��Ϊ2A��ͨ��3min13s�缫B�����ɽ���R0.127g����֪1mol���ӵĵ���Ϊ96500C����R�����ԭ������Ϊ______������______����Ԫ�ط��ţ���
��5����P��Q�任λ�ý��ߣ�ʹ����������������ǿ��Ϊ2A��5min����B���Ͽ�����______��______��������
�ο��𰸣���1����·��ͨ��R�����ڵ缫B�ϣ�˵��B�缫�ϵõ��ӷ�����ԭ��Ӧ������B���ǵ��ص�������A��������P�ǵ�Դ��������Q�ǵ�Դ�ĸ�����
�ʴ�Ϊ��P��
��2��A�缫�Ͻ���ʧ�������ɽ��������Ӷ�����������Ӧ���缫��ӦʽΪR-2e-�TR2+��
�ʴ�Ϊ��R-2e-�TR2+��
��3��C��D�缫����Pt�����������Һ��C��D�ֱ��ǵ��ص��������������ֱ�ų�O2��H2�����ǵ������Ϊ1��2���ʴ�Ϊ��1��2��
��4������Q=It=2A����3��60+13��s=386C��1mol���ӵĵ���Ϊ96500C��������������ʱת�Ƶ��ӵ����ʵ���=386C96500C/mol=0.004mol�������������εĻ�ѧʽ֪��R�ڻ���������+2�ۣ����������������ʵ���=0.04mol2=0.02mol��R�����ԭ������=0.127g0.02mol=63.5g/mol���������ԭ������Ϊ63.5��������Cu��
�ʴ�Ϊ��63.5��Cu��
��5����P��Q�任λ�ý��ߺ�B����Ϊ���ص���������ǰ3min13sԭ��������Cu������ӦCu-2e-�TCu2+���ܽ⣬��1min47s������Ӧ4OH--4e-�T2H2O+O2�����������������Կ����������ǽ���R��Cu���ܽ⣻B�����������ݳ����ʴ�Ϊ������R��Cu���ܽ⣻B�����������ݳ���
���������
�����Ѷȣ���
2��ѡ���� ��ͼ��һ�����͵����ӽ���Ĥ������ȼ�ϵ��(DDFC)������ܷ�ӦΪ��CH3OCH3+3O2=2CO2+3H2O������˵������ȷ����
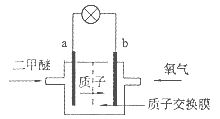
A��a��Ϊ��صĸ���
B����ع���ʱ������b���ص��߾������ٵ�a��
C����������ĵ缫��ӦΪ��4H++O2+4e-=2H2O
D����ع���ʱ��1 mol�����ѱ�����ʱ����6 mol����ת��
�ο��𰸣�D
������������⿼��ȼ�ϵ�ء�ͨ��ȼ�ϼ��ѵ�a�缫��ԭ��صĸ���������ʧ���ӷ���������Ӧ��ͨ��������b�缫�������������õ��ӷ�����ԭ��Ӧ�������������ص���������A��ȼ�ϵ���У�ͨ��ȼ�ϼ��ѵĵ缫a�Ǹ�������ȷ��B����ع���ʱ����������b�ص��ߵ�����a����ȷ��C��ͨ�������ĵ缫�������������Ի����µĵ缫��ӦΪ��4H++O2+4e-=2H2O����ȷ��D�����ݵ�ط�ӦCH3OCH3+3O2=2CO2+3H2O��֪��1mol���ѱ�����ʱ����12mol����ת�ƣ�����
�����Ѷȣ�һ��
3��ʵ���� ��13�֣�ij����С��̽���ơ���������ͭ���ʻ�ԭ��ǿ��������ػ�ѧ���ʣ���������ʵ�飺
ʵ��1
| ����ʱȡ���ֽ��������ֱ����װ������ˮ���Թ���
|
ʵ��2
| ��ȡ������������ͭ�ֱ����װ��ϡ������Թ���
|
��1��ʵ��1���ܷ�����Ӧ�����ӷ���ʽ ��
��2��ʵ��2���ܹ��жϳ���������ͭ��ԭ��ǿ���������� ��
���ۣ���ʵ��1��2�ó����ֽ����Ļ�ԭ��ǿ��˳��Ϊ �����ԭ�ӽṹ�ǶȽ����ƵĻ�ԭ��ǿ���� ��
��3��Ϊȷ��ʵ��2��Ӧ����Һ�еĽ��������ӣ��ٽ���ʵ�飺
��ȡAl��Ӧ�����Һ���������NaOH��Һ��д����Ӧ�����ӷ���ʽ ��
��һ��ʱ���ȡFe��Ӧ�����Һ������Fe2+������ȷ���� ��
a���μ�KSCN��Һ�������Ա仯���ټ���������ˮ����Һ���
b���μ�K3��Fe(CN)6����Һ������ɫ��������
c���μ�NaOH��Һ�������İ�ɫ����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ
��4����ʵ��2�У���������Ӧ����IJ��첢���Ǻ����ԣ���ͬѧ���������һ��ʵ����֤�������ֽ����Ļ�ԭ�Թ�ϵ�������һ��ʵ�鷽�� ��
��5����ʵ������У�����ͬѧΪ����֤����ͭ�Ļ�ԭ�ԣ�������ͭ�����ߡ��ձ����Ȼ�����Һ�����ԭ���װ�á�
�ٻ���ԭ��ص�װ��ͼ ��
�ڸõ�ص�������ӦΪ ��
�ο��𰸣���13�֣�
��1��2Na+2H2O=2Na++2OH-+H2�� ��2�֣�
��2�����������������������Կ�Щ��ͭ���������� ��1�֣�
Na>Al>Fe>Cu ��1�֣�
Na��Alͬ���ڵ�������Naԭ�Ӱ뾶����Al ��1�֣�
��3���� Al3++4OH-=AlO2-+2H2O ��2�֣�
��b ��1�֣�
��4����������������������Һ��Һ�У���Һ��ɫ��dz���������(�����𰸺�������) ��2�֣�
��5���� ��2Fe3++2e-=2Fe2+ ��1�֣�
��2Fe3++2e-=2Fe2+ ��1�֣�
�����������1���ơ���������ͭ���ֽ����г�����ֻ������ˮ��Ӧ����Ӧ�����ӷ���ʽΪ2Na+2H2O=2Na++2OH-+H2������2����������ϡ���ᷴӦ��������������Щ��ͭ��ϡ�����Ӧ�����ۣ���ʵ��1��2�ó����ֽ����Ļ�ԭ��ǿ��˳��ΪNa>Al>Fe>Cu��Na��Alͬ���ڵ�������Naԭ�Ӱ뾶����Al���Ƹ���ʧȥ���ӣ���3����Al3+�������NaOH��Һ��Ӧ�����ӷ���ʽAl3++4OH-=AlO2-+2H2O ����ͨ������K3��Fe(CN)6����Һ����Fe2+������ײ�������ѡb����4����ͨ��ԭ���ԭ����������ԭ��Ӧԭ�����м��飻��5����Ӧ��Fe��������ͭ���������Ȼ�����Һ���������Һ��װ��ͼ�ԣ��ڸõ�ص�����������ԭ��Ӧ���缫��ӦΪ2Fe3++2e-=2Fe2+��
���㣺�������������ʡ�ԭ���ԭ��
�����Ѷȣ�����
4��ѡ���� �ڳ�ʪ�Ŀ����У������ܿ췢���绯ѧ��ʴ���ڴ˹�����һ�������ڵĵ缫��Ӧ��
[? ]
A��2H++2e-==H2��
B��Fe-3e-==Fe3+
C��Fe-2e-==Fe2+
D��O2+2H2O+4e-==4OH-
�ο��𰸣�B
���������
�����Ѷȣ���
5������� ���Ȼ��غ���������ԭ����������غ������������ϣ�����Ҫ�������£�
��֪�� ��Һ�ʼ��ԣ�30��������Һ��
��Һ�ʼ��ԣ�30��������Һ�� �����ֽ⡣
�����ֽ⡣

��1��д�� ��Һ�е������غ�___________________________________
��Һ�е������غ�___________________________________
��2��д��������I�з�Ӧ�Ļ�ѧ����ʽ_______________________���÷�Ӧ������Ƶķ�Ӧ������___________________________��
��3���������I��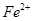 �����Ƿ���ȫ�ķ�����__________________________________��
�����Ƿ���ȫ�ķ�����__________________________________��
��4���ữ��Ŀ����___________________________��
��5���ڳ�����II�У�Ϊʹ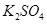 �����������õ����˲���������ʱ�õ�����Ҫ����������__________________________��
�����������õ����˲���������ʱ�õ�����Ҫ����������__________________________��
��6��N��P��K��S����ֲ�������������ҪԪ�ء���ҺA�������Ϸ��ϣ���Ϊ���к���___________��Ԫ�ء�
��7���й������ѧӦ�û�ѧ�о������Ҵ�ȼ�ϵ�ؼ���������ͻ�ƣ���װ�����Ժ�����ؼ�����ʽ��ѡ��Ҵ�ȼ�ϵ�صĹ���ԭ����ͼ��ʾ��
�ٸõ�ع���ʱ��c��ͨ�������Ϊ___________��
�ڸõ�ظ����ĵ缫��ӦʽΪ_____________________________________��

�ο��𰸣���1��[NH4+]+[NH3?H2O]=[CO32?]+[H2CO3]+[HCO3?] ��2�֣�
��2��2NH4HCO3 + FeSO4 = FeCO3��+ (NH4)2SO4 + CO2��+ H2O ��2�֣�����Ӧ�¶ȵ���30�� ��1�֣�
��3��ȡ�����آ����Һ���μ�KSCN��Һ��μ���ˮ������ɫ���֣�˵��������ȫ�����������ɣ���2�֣�
��4����ȥ��Һ�е�HCO3? ��2�֣�
��5����ͨ©�����ձ�����������2�� ��ȫ��1�֣���ͬ��
��6��K��S ��K?��2�֣�
��7��O2��1�֣���C2H6O �C 12e? + 3H2O = 2CO2 +12H+��2�֣�
�����������1�������غ��ʵ����Ԫ���غ㣬NH4HCO3��Һ��NԪ����CԪ�����ʵ�����ȣ�����[NH4+]+[NH3?H2O]=[CO32?]+[H2CO3]+[HCO3?]
��2��̼��������Ӻ���������֮�䷢��˫ˮ�ⷴӦ����̼���������������ų�������̼����Ӧ��ԭ������ʽΪ��2NH4HCO3+FeSO4=FeCO3��+��NH4?��2SO4+CO2��+H2O��Ϊ��ֹ�ϸ��¶���̼����淋ķֽ⣬Ҫע���¶ȵ�ѡ��Ӧ�¶ȵ���30�档
��3���������ӿ��Ա���������Ϊ���������ӣ�������������������ز���ɫ�������������������������ʾ��ɫ�����������I��Fe2+�����Ƿ���ȫ�ķ����ǣ�ȡ������I����Һ���μ�KSCN��Һ��μ���ˮ������ɫ���֣�˵��������ȫ��
��4�������آ��У��������ɵ�̼������֮�⣬��Һ���ܻẬ�й�����̼����泥������ᣬ�ữ��Ŀ���dz�ȥ��Һ�е�HCO3-��?
��5������Ŀ�����ڢ�Ӧ�����ɵ�K2SO4Ϊ���壬��K2SO4�����ܼ����ܽ���DZȽϴ�ģ�Ҫ��ʹK2SO4����ֻ�ܽ������ܽ�����Լ��봼���ܼ�Ŀ�Ľ���K2SO4���ܽ�ȡ�
��6����ҺA�ijɷ��к��У�NH4?��2SO4�Լ�KCl��������N��S��KԪ�أ����ڸ��Ϸ��ϡ�
��7������ͼ��H+�ƶ�����֪�Ҳ�缫Ϊȼ�ϵ�ص�����������c��ͨ�������ΪO2����ͼ��֪�������Һ�к�H+�������Ҵ���ˮ��Ӧ�����ݻ��ϼ۵ı仯��C2H5OHʧȥ12e?���ɵõ缫����ʽ��C2H6O �C 12e? + 3H2O = 2CO2 +12H+
�����Ѷȣ�һ��