1、填空题 原电池是把_______能转化为电能的装置。活泼金属是原电池_______极,发生_______反应(填“氧化”或“还原”);不活泼金属与其他导电材料是原电池的_______极,电解质中的阳离子在正极上_______(填“得”或“失”)电子。
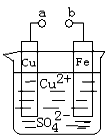
2、选择题 某小组为研究电化学原理,设计如图装置。下列叙述不正确的是
[? ]
A、a和b不连接时,铁片上会有金属铜析出
B、a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu
C、无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D、a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
3、填空题 利用反应:Fe+2Fe3+=3Fe2+制一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料,标出电子流动方向和电流方向,写出其电极反应式。_______________________________________
4、填空题 (1)甲醇是一种可再生能源,工业上一般采用下列两种反应合成甲醇:
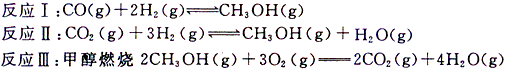
上述反应符合“原子经济”原则的是_______________(填“Ⅰ”、“Ⅱ”或“III”)。
(2)依据甲醇燃烧的反应原理,设计如图所示的电池装置。
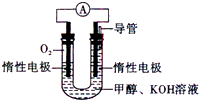
①该电池正极的电极反应为____________。
②工作一段时间后,测验得溶液的pH减小,该电池总反应的化学方式式为________________________。
(3)甲烷也是一种可再生的能源,如果用甲烷来制水煤气,反应方程式为:

在一体积恒定为1 L的密闭器中用1mol甲烷和1mol水蒸气进行以上反应,测得甲烷的物质的量浓度随反应时间的变化如图所示。
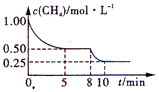
①反应在0~5min这段时间共吸收的热量为____________kJ;
②进行到5min时,反应达到平衡,这时平衡常数K的数值为____________;
③进行到8min时,只改变了影响平衡的一个条件:水蒸气的浓度。10min达到新的平衡,这时
c(H2O)=____________mol/L。(小数点后面保留一位数)
5、填空题 (7分)一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,假定放电过程中,甲醇完全氧化产生的CO2被充分吸收生成CO32-。。
(1)该电池反应的总离子方程式为____________________________________________;
(2)甲醇在_________极发生反应(填正或负),电池在放电过程中溶液的pH将__________(填降低或上升、不变);
(3)最近,又有科学家制造出一种固体电解质的燃料电池,其效率更高。一个电极通入空气,另一电极通入汽油蒸气。其中固体电解质是掺杂了Y2O3(Y:钇)的ZrO2(Zr:锆)固体,它在高温下能传导O2-离子(其中氧化反应发生完全)。以丁烷(C4H10)代表汽油。
①放电时固体电解质里的O2-离子的移动方向是向____________极移动(填正或负)。
②电池的正极反应式为____________________________________________?。