1、实验题 实验室用如图所示装置制备Cl2,并进行Cl2的性质实验。
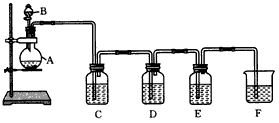
(1)A中加入KMnO4固体(反应后产物是MnCl2),B中盛有浓盐酸,烧瓶中发生反应的化学方程式为________________________
(2)C中盛有紫色石蕊试液,C中的现象是____________;D中有白色沉淀生成,D中盛放的试剂可能是
____________;E中溶液由无色变为蓝色,E中盛放的试剂可能是___________________。
(3)F的作用是______________________。
参考答案:(1)2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(2)先变红后褪色;AgNO3溶液;淀粉KI溶液
(3)吸收尾气
本题解析:
本题难度:一般
2、简答题 喷泉是一种常见的自然现象,其产生的原因是存在压强差.制取氨气并完成喷泉实验(图中夹持装置均已略去).
(1)写出实验室制取氨气的化学方程式:______.
(2)收集氨气应使用______法.
(3)要得到干燥的氨气可选用下列______?做干燥剂.
A.浓硫酸?B.碱石灰?C.NaOH固体?D.P2O5固体
(4)用图1装置进行喷泉实验,烧瓶已装满干燥氨气,引发水上喷的操作是______.该实验的原理是______.
(5)如果只提供如图2的装置,请举例说明引发喷泉法______.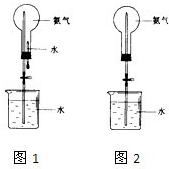
参考答案:(1)实验室用加热氯化氨和消石灰的固体混合物制取氨气,方程式为2NH4Cl+Ca(OH)2??△?.?CaCl2+2NH3+2H2O,
故答案为:2NH4Cl+Ca(OH)2??△?.?CaCl2+2NH3+2H2O;?
(2)氨气的密度比空气小,极易溶于水,只能用向下排气法收集,故答案为:向下排空气法;
(3)浓硫酸具有酸性,五氧化二磷为酸性氧化物,氨气是碱性气体,所以,浓硫酸和五氧化二磷都不能干燥氨气,
故答案为:BC;
(4)氨气是一种极易溶于水的气体,将胶头滴管中的水挤入烧瓶中,瓶内压强减小,在外界气压的作用下,水被压到瓶内,形成喷泉现象,
故答案为:将胶头滴管中的水挤入烧瓶中,松开弹簧夹;挤出的水溶解了烧瓶中的NH3,使瓶内压强减小,烧瓶内外形成了气压差;
(5)要形成喷泉,需把烧杯中的液体压入烧瓶,可以利用吸收热量使烧瓶中的压强减小,
故答案为:用冰毛巾捂住烧瓶一段时间,再松开弹簧夹.
本题解析:
本题难度:一般
3、简答题 某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验.请回答下列问题:
(1)仪器a的名称为______;仪器b中可选择的试剂为______.
(2)实验室中,利用装置A,还可制取的无色气体是______(填字母).
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有______性,写出相应的化学方程式______
(4)E装置中浓硫酸的作用______.
(5)读取气体体积前,应对装置F进行的操作:______
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为______(用含m、n字母的代数式表示)
参考答案:(1)装置中仪器a为分液漏斗;仪器b是利用分液漏斗中滴入的氨水使锥形瓶中的固体溶解放热促进一水合氨分解生成氨气,氢氧化钠固体、氧化钙固体、碱石灰固体,
故答案为:分液漏斗;固体氢氧化钠或氧化钙或碱石灰;
(2)利用装置A,可制取的无色气体;
A.制备氯气Cl2需要加热,且氯气为黄绿色气体,故A不符合;
B.可以制备O2,利用固体过氧化钠和水的反应,故B符合;
C.可以制备CO2 气体,利用稀盐酸滴入大理石上反应生成,故C符合;
D.NO2是红棕色气体,故D不符合;
故选BC;
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,说明氨气和氧化铜反应生成铜和氮气与水,氨气被氧化铜氧化表现还原性,结合原子守恒配平写出的化学方程式为:3CuO+2NH3△.3Cu+3H2O+N2 ,故答案为:还原;3CuO+2NH3△.3Cu+3H2O+N2 ;
(4)依据流程分析,浓硫酸是吸收过量的氨气,阻止F中水蒸气进入D影响实验效果,故答案为:吸收未反应的氨气,阻止F中水蒸气进入D;
(5)读取气体体积前,应对装置F进行的操作是慢慢上下移动右边漏斗,使左右两管液面相平,保持压强平衡再读数,故答案为:慢慢上下移动右边漏斗,使左右两管液面相平;
(6)若测得干燥管D增重mg为水物质的量=mg18g/mol,装置F测得气体的体积为nL(已折算成标准状况)为N2,物质的量=nL22.4L/mol,依据元素守恒得到氮原子和氢原子物质的量之比=nL22.4L/mol×2:mg18g/mol×2=9n11.2m,则氨分子中氮、氢的原子个数比为9n11.2m,故答案为:9n11.2m.
本题解析:
本题难度:一般
4、实验题 熟悉和使用中学化学实验中常见仪器及用品,是化学学习的基本要求。试回答以下问题:
(1)在仪器:a.分液漏斗b.试剂瓶c.集气瓶d.滴定管e.容量瓶f.量筒 g.托盘天平中,标有“0”刻度的是(填序号)____。
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺。在下列仪器中,没有用到“磨砂”工艺处理的有(填序号)____。
a.试管b.分液漏斗c.带滴管的试剂瓶(滴瓶)d.集气瓶e.酸式滴定管 f.碱式滴定管
(3)用装置甲、乙、丙和乳胶管组成一套装置(气密性已检查),可用于制取并收集NH3或HCl气体。可供选择的液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。请回答下列问题:
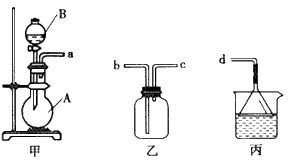
①若制取某气体的过程中,丙中的石蕊溶液变红,且烧瓶中的试剂A与分液漏斗中的试剂B均为无色液体,则试剂A为________,制取该气体利用了B的性质有__________、__________。通过丙中紫色石蕊溶液变红或变蓝,说明乙中气体己集满。若石蕊溶液变蓝,则烧瓶甲中应加入的固体试剂A为__________;
②若在乙中收集氨气,气体流经装置的顺序是:a→_____→_____ →d (填接口代号)。
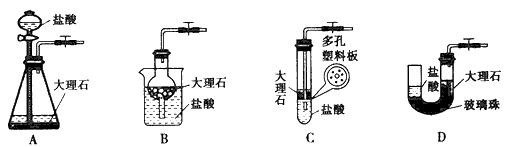
(4)下图中的装置D是实验室制备CO2的简易装置图,用该装置制备CO2可起到随时使反应发生,也可以随时使反应停止的效果。下图中的装置A、B、C也可起到相同效果的有________ (填写编号)。
参考答案:(1)dg
(2)af
(3)①浓盐酸 ;吸水性 ;溶于水放出大量热 ;NaOH或CaO或碱石灰 ;②c ;b
(4)B
本题解析:
本题难度:一般
5、填空题 如图表示在没有通风橱的条件下制备氯气时设计的装置,图中a.b是可控制的弹簧铁夹.(氯气在饱和氯化钠溶液中的溶解度较小.)
(1)仪器A的名称是______;水槽中应盛放的是______;烧杯中盛放的是______;烧瓶中反应的化学方程式______;
(2)在收集氯气时,应______.(填如何控制a.b)
(3)若要制得标准状况下的Cl20.672L,理论上需要MnO2的质量是______g被氧化盐酸的物质的量______mol
(4)若要增大新制氯水中HClO的浓度可加入______
A.食盐B.水C.CaCO3D.NaOH.

参考答案:(1)根据仪器特点可知A为分液漏斗;因为氯气有毒,可污染空气,要进行尾气吸收,并且氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以常用氢氧化钠溶液吸收尾气中,烧杯中盛放氢氧化钠溶液收,集完毕,关闭a,打开b,多余的气体通入氢氧化钠溶液进行吸收,防止污染空气;Cl2+2NaOH=NaCl+NaClO+H2O;氯气在饱和氯化钠溶液中的溶解度较小,实验室常用排饱和食盐水法收集氯气,实验室常用二氧化锰和浓盐酸在加热条件下生成氯气,反应的化学方程式为MnO2+4HCl△.MnCl2+Cl2↑+2H2O,
故答案为:分液漏斗;饱和食盐水;氢氧化钠溶液;MnO2+4HCl△.MnCl2+Cl2↑+2H2O;
(2)氯气在饱和氯化钠溶液中的溶解度较小,实验室常用排饱和食盐水法收集氯气,收集时,应关闭b,打开a,故答案为:关闭b,打开a;
(3)n(Cl2)=VVm=0.672L22.4L/mol=0.03mol;
生成0.03molCl2参加反应的HCl的物质的量为x,反应的二氧化锰物质的量为Y;
MnO2+4HCl△.MnCl2+Cl2↑+2H2O
1 4 1
y x 0.03mol
x=0.12mol
y=0.03mol
被氧化的HCl的物质的量=0.12mol×12=0.06mol.
理论上反应的二氧化锰质量=0.03mol×87g/mol=2.61g;
故答案为:2.61;0.06;
(4)氯水中氯气和水反应生成盐酸和次氯酸,Cl2+H2O=HClO+HCl,
A、食盐加入,增大氯离子浓度,平衡左移,次氯酸浓度减小,故A不符合;
B、水加入平衡状态物质浓度减小,次氯酸浓度减小,故B不符合;
C、加入碳酸钙和盐酸反应促进平衡正向进行,次氯酸浓度增大,故C符合;
D、加入氢氧化钠会和盐酸、次氯酸发生反应,次氯酸浓度减小,故D不符合;
故答案为:C.
本题解析:
本题难度:一般