1ΓΔ―Γ‘ώΧβ œ¬Ν–»»Μ·―ßΖΫ≥Χ ΫΜράκΉ”ΖΫ≥Χ Ϋ÷–Θ§’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°œΓ»ή“Κ÷–Θ§H+Θ®aqΘ©+OH-Θ®aqΘ©®TH2OΘ®lΘ©ΓςH=-57.3?kJ?mol-1Θ§œΓ¥ΉΥα”κœΓNaOH»ή“ΚΖ¥”Π…ζ≥…1?molΥ°Θ§Ζ≈≥ωΒΡ»»ΝΩ…Ό”Ύ57.3?kJ
BΘ°500ΓφΓΔ30?MPaœ¬Θ§ΫΪ0.5?mol?N2ΚΆ1.5?mol?H2÷Ο”ΎΟή±’»ίΤς÷–≥δΖ÷Ζ¥”Π…ζ≥…NH3Θ®gΘ©Θ§Ζ≈»»19.3?kJΘ§Τδ»»Μ·―ßΖΫ≥Χ ΫΈΣΘΚ
N2Θ®gΘ©+3H2Θ®gΘ©?
2NH3Θ®gΘ©ΓςH=-38.6?kJ?mol-1
CΘ°¬»Μ·ΟΨ»ή“Κ”κΑ±Υ°Ζ¥”ΠΘΚMg2++2OH-®TMgΘ®OHΘ©2Γΐ
DΘ°―θΜ·¬Ν»ή”ΎNaOH»ή“ΚΘΚAl2O3+2OH-®T2AlO2-+H2O
2ΓΔ―Γ‘ώΧβ œ¬Ν–άκΉ”ΖΫ≥Χ Ϋ”κΥυ ω ¬ ΒœύΖϊ«“’ΐ»ΖΒΡ «
AΘ°Fe(OH)3»ή”Ύ«βΒβΥαΘΚFe(OH)3 + 3HΘΪΘΫFe3ΘΪ+ 3H2O
BΘ°œρNaAlO2»ή“Κ÷–Ά®»κΙΐΝΩCO2÷ΤAl(OH)3ΘΚ
2AlO2Θ≠+ CO2 + 3H2OΘΫΘΫ 2Al(OH)3Γΐ+ CO32Θ≠
CΘ°”ΟΕη–‘ΒγΦΪΒγΫβœθΥα“χ»ή“ΚΘΚ4Ag+ + 2H2O  4Ag+O2Γϋ+4H
4Ag+O2Γϋ+4H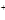
DΘ°œρAgCl–ϋΉ«“Κ÷–Φ”»κ±ΞΚΆNaI»ή“ΚΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚAg+ + I- ΘΫΘΫAgIΓΐ
3ΓΔ―Γ‘ώΧβ œ¬Ν–άκΉ”ΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°«β―θΜ·±Β»ή“Κ”κ―ΈΥαΒΡΖ¥”ΠΘΚOH-+H+=H2O
BΘ°≥Έ«εΒΡ ·Μ“Υ°”κœΓ―ΈΥαΖ¥”ΠΘΚCaΘ®OHΘ©2+2H+=Ca2++2H2O
CΘ°Ά≠Τ§≤ε»κœθΥα“χ»ή“Κ÷–ΘΚCu+Ag+=Cu2++Ag
DΘ°ΧΦΥαΗΤ»ή”ΎœΓ―ΈΥα÷–ΘΚCO32-+2H+=H2O+CO2Γϋ
4ΓΔ―Γ‘ώΧβ œ¬Ν–Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ ι–¥’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°¬»ΤχΆ®»κ«β―θΜ·ΡΤ»ή“Κ÷–ΘΚCl2+2OH-=Cl-+ClO-+H2O
BΘ°œΓΝρΥα”κΧζΖέΖ¥”ΠΘΚ2Fe+6H+=2Fe3++3H2Γϋ
CΘ°«β―θΜ·±Β»ή“Κ”κœΓΝρΥαΖ¥”ΠΘΚBa2++SO42-=BaSO4Γΐ
DΘ°¬»Μ·Χζ»ή“Κ”κΆ≠ΖέΖ¥”ΠΘΚCu+Fe3+=Fe2++Cu2+
5ΓΔ―Γ‘ώΧβ œ¬Ν–άκΉ”ΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°–Ω”κœΓΝρΥαΖ¥”ΠZn+2H+=Zn2++H2Γϋ
BΘ°Ά≠”κœθΥα“χ»ή“ΚΖ¥”ΠCu+Ag+=Cu2++Ag
CΘ°ΧΦΥαΗΤ”κ―ΈΥαΖ¥”ΠCaCO3+2H+=Ca2++CO2+H2O
DΘ°ΝρΥα”κ«β―θΜ·±Β»ή“ΚΜλΚœSO42-+Ba2+=BaSO4